每年全球新增肺癌患者约180万,占所有恶性肿瘤的13%,也是死亡率最高的恶性肿瘤之一[1]。肺癌的发病率在中国也是第1位,且越来越年轻化[2],其中约85%的患者为非小细胞肺癌,鳞状细胞癌是非小细胞肺癌中最常见的一种类型[3]。肺癌的5年生存率极低,可能与患者术后复发与转移有关,肿瘤组织的血管形成可能与患者术后预后不良相关。血管生成抑制蛋白家族是近年来才被发现的一种血管生成负反馈调节因子[4],该家族成员主要有两种:vasohibin-1和vasohibin-2[5]。vasohibin-1是最重要的家族成员,主要表达于血管内皮细胞,与肿瘤细胞中的血管内皮细胞生长因子(VEGF)和成纤维细胞生长因子2(FGF-2)密切相关[4, 6]。vasohibin-1高表达意味着肿瘤患者预后不良[7]。结肠癌转移相关蛋白-1(MACC1)首先是从结肠癌中发现的一种癌基因[8],是肝细胞生长因子/间质上皮转化(HGF/ MET)信号途径的关键调控因子[9]。MACC1主要通过结合MET基因的启动子而控制其转录活性,从而促进肿瘤细胞的迁徙和浸润,并诱导肿瘤的增殖和转移[10]。MACC1蛋白的表达异常增高往往意味着患者预后不良。目前关于vasohibin-1与MACC1蛋白在LSCC中的临床意义及其相互之间的关系未见有报道,本研究通过免疫组织化学ElivisionTM plus方法检测160例LSCC患者肿瘤组织vasohibin-1和MACC1蛋白的表达,分析它们与LSCC患者肿瘤组织浸润、转移及预后的关系以及它们相互之间的关系。
1 资料和方法 1.1 一般资料收集蚌埠医学院第一附属医院病理科2009年1月~2010年12月存档石蜡包埋肺鳞状细胞癌(LSCC)组织标本160例(术前未行任何抗肿瘤及相关治疗)和正常肺组织80例,所有患者均有完整的临床病理资料及随访资料,入选患者随访至患者死亡或截止至2015年12月,随访时间为8~71月。本研究组中男性患者有122例,女性患者有38例;年龄29~79岁,中位年龄59.6岁,其余资料见表 1。80例正常对照组肺组织均取自远离LSCC肿块>5.0 cm,并经病理HE染色证实为正常肺组织。
| 表 1 LSCC中Vasohibin-1和MACC1的表达及其与临床各病理因素之间的关系 Table 1 Correlations of the vasohibin-1 and MACC1 expression with the clinicopathological characteristics of patients with LSCC |
兔抗人vasohibin-1多克隆抗体(ab199732)及兔抗人MACC1多克隆抗体(ab106579)均购自美国Abcam公司;ElivisionTM plus试剂盒以及DAB显色试剂盒均购自中国福州迈新生物技术有限公司。
1.3 实验方法所有LSCC组织标本均经4%中性福尔马林溶液固定、石蜡包埋,4 μm厚连续切片等系列过程,然后再与二甲苯溶液及浓度梯度的乙醇溶液中脱蜡至水洗。vasohibin-1和MACC1抗体染色步骤均按照试剂盒说明书进行,同时用已知阳性片作阳性对照,空白对照用PBS液替代一抗进行。
1.4 结果判定vasohibin-1主要是以细胞浆和膜内出现黄色或棕黄色颗粒为阳性;MACC1主要是以细胞浆出现黄色或棕黄色颗粒为阳性。阳性结果的判定是根据着色强度和着色范围来分别计分的,具体办法参见相关文献[11]。最后根据阳性强度和阳性范围的乘积,得出一个积分介于0~12的值,若积分≥3分为阳性,< 3分为阴性。免疫组化抗体结果的判定是由两位病理医生通过独立双盲法得出的。
1.5 统计分析采用SPSS20.0统计软件包进行数据分析。在LSCC组织中vasohibin-1和MACC1蛋白的表达与正常肺组织、各临床病理因数之间以及它们相互之间的关系采用χ2、Spearman等级相关检验;vasohibin-1和MACC1蛋白阳性组和阴性组患者生存分析采用Kaplan-Meier方法,组间比较采用log-rank法检验,P < 0.05为差异有统计学意义。
2 结果 2.1 LSCC组织中vasohibin-1蛋白的表达及其临床意义Vasohibin-1蛋白在对照组肺组织中的阳性表达率为11.3%(9/80),在LSCC组织中的阳性率为59.4%(99/ 160),差异在两组之间有统计学意义(P < 0.05,图 1A,B)。vasohibin-1蛋白的阳性表达率在LSCC患者的不同年龄、性别、肿瘤大小、肿瘤类型及肿瘤位置等之间差异均无统计学意义(P>0.05,表 1)。进一步分析发现,随着LSCC组织的分化越差,vasohibin-1蛋白的阳性率表达越高,差异有统计学意义;淋巴结转移组中vasohibin-1蛋白的阳性表达率明显高于其在淋巴结无转移组中的阳性表达率;TNM分期高组中的vasohibin-1蛋白的阳性表达率显著高于其在低TNM分期中的阳性表达率,差异均有统计学意义(P < 0.05,表 1)。
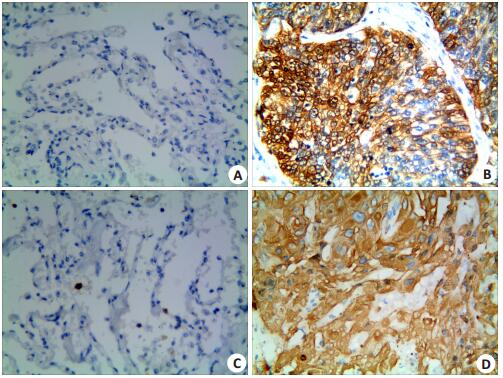
|
图 1 Vasohibin-1和MACC1在LSCC中的阳性表达 Figure 1 Expression of vasohibin-1 and MACC1 in LSCC and normal lung tissue (ElivisionTM, original magnification: ×400). A, B: Negative staining of vasohibin-1 in the normal lung tissue and positive staining in the membrane of moderately differentiated LSCC, respectively; C, D: Negative staining of MACC1 in the normal lung tissue specimen and positive staining in the cytoplasm of moderately differentiated LSCC, respectively. |
MACC1蛋白在对照组肺组织中的阳性表达率为8.8%(7/80),在LSCC组织中为57.5%(92/160),表达差异在两组之间有统计学意义(P < 0.001,图 1C、D)。随后的分析发现,随着LSCC组织的分化越差、TNM分期越高,MACC1蛋白的阳性表达率就越高,差异有统计学意义(P < 0.05);淋巴结转移组中MACC1的阳性表达率显著高于其在淋巴结无转移组中的阳性表达率(表 1)。另外,MACC1蛋白的阳性表达率在LSCC患者不同年龄、性别、肿瘤大小、肿瘤类型及肿瘤位置等之间差异无统计学意义。
2.3 LSCC组织中vasohibin-1和MACC1之间的关系Spearman相关分析显示,在LSCC组织中vasohibin-1的表达与MACC1的表达呈正相关关系(r= 0.550,P < 0.001,表 1)。
2.4 COX多因素多因素回归分析将LSCC患者的年龄(分为≥60岁组与 < 60岁组);性别(分为男性组与女性组);肿瘤的长径(分为 < 3.0 cm组、3.0 cm≤Size < 7.0 cm组和≥7.0 cm组);肿瘤的位置(分为左侧肺组和右侧肺组)、肿瘤的分类(分为中央型组和周围型组)、分化程度(分为高分化组、中分化组和低分化组);淋巴结转移(分为有转移组和无转移组);TNM分期(分为Ⅰ期组、Ⅱ期组和Ⅲ期组);vasohibin-1表达组(分为阳性组与阴性组);MACC1表达组(分为阳性组与阴性组)等因素带入COX多因素模型进行分析表明:vasohibin-1和MACC1的阳性表达以及TNM分期是影响LSCC患者术后生存的独立预后因素(表 2)。
| 表 2 160例LSCC患者的多因素分析 Table 2 Multivariate survival analysis of 160 patients with LSCC |
本组病例总的5年生存率为25.0%(40/160)。Kaplan-Meier生存分析显示vasohibin-1蛋白阳性组与阴性组的生存时间分别为31.7±16.5月和53.9±14.5月,log-rank分析总的生存时间差异在两组之间有统计学意义(P < 0.001,图 2A);MACC1蛋白阳性组与阴性组的生存时间分别为30.8±15.8月和54.2±14.4月,log-rank分析显示总的生存时间差异在两组之间有统计学意义(P < 0.001,图 2B)。
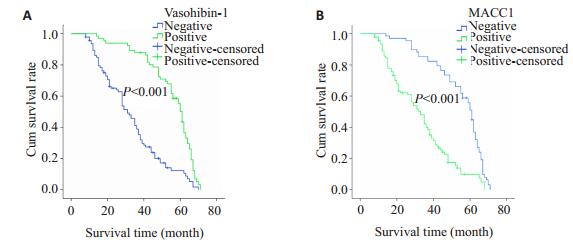
|
图 2 Vasohibin-1和MACC1阳性表达组与阴性表达组LSCC患者生存曲线 Figure 2 Survival curves of LSCC patients with positive or negative expressions of vasohibin-1 (A) and MACC1 (B). |
体外实验已经证实vasohibin-1可以抑制血管内皮细胞增殖、抑制血管及淋巴管生成[4, 12-13]。本研究通过免疫组化方法检测vasohibin-1蛋白在LSCC组织及其癌旁正常肺组织中表达,发现在LSCC组织中,vasohibin-1蛋白的阳性表达率显著高于其正常对照组中的阳性表达率,差异有统计学意义。进一步的研究发现,随着LSCC组织的分化越差,vasohibin-1蛋白的阳性表达率越高;淋巴结转移越多,vasohibin-1蛋白的阳性率也越高;且随着TNM的分期越高,其阳性率也越高,差异均有统计学意义。Kaplan-Meier生存分析结果显示,vasohibin-1蛋白阳性表达组患者的生存时间显著低于阴性组患者。上述研究结果表明,vasohibin-1蛋白表达异常增高的患者预后差,易于发生浸润及转移,这与国内外学者研究结果相一致[7, 14-16 1]。当肿瘤组织生长到一定大小时,肿瘤细胞就会通过分泌大量的VEGF、FGF2等因子促进血管形成以满足其快速生长所需的营养和氧,而VEGF和FGF-2又可以促进血管内皮细胞合成vasohibin-1,新合成的vasohibin-1可以负反馈的抑制肿瘤组织中的血管及淋巴管的进一步形成,在某种程度上抑制了肿瘤的进一步增殖。由于vasohibin-1蛋白和VEGF在血管生成调节中失衡,可以诱导形成许多结构和功能异常的血管,由于管壁结构的不完整以及基膜的缺乏致使血管通透性升高,从而促进肿瘤细胞的浸润和转移[15]。因此,正常情况下,vasohibin-1蛋白的高水平表达反而意味着患者预后不良[16-17]。
MACC1通过调控HGF/c-Met-丝裂原活化蛋白激酶(MAPK)信号通路,促进细胞的增殖、迁移及浸润,并影响肿瘤的糖代谢及微环境;此外,MACC1还可以通过HGF/c-Met-MAPK信号通路诱导肿瘤组织的上皮间质转化过程而促进肿瘤细致的增殖和浸润[18]。表达异常增高MACC1通常与恶性肿瘤的浸润、转移及预后密切相关[8]。在本研究中,我们发现MACC1蛋白在LSCC组中的阳性表达率显著高于其在对照组中的阳性率,差异有统计学意义;并且随着LSCC肿瘤组织的分化越差、淋巴结转移越多、TNM分期越高,MACC1蛋白的阳性表达率越高,差异均有统计学意义;生存分析也表明MACC1蛋白阳性表达组患者其术后总的生存时间明显低于其表达阴性组患者。上述结果表明,MACC1蛋白阳性表达的LSCC患者其肿瘤组织分化差、淋巴结转移越多、TNM分期高以及预后差,这与文献报道一致[8-9, 19-21]。
LSCC是一个高度异质性的肿瘤,这种异质性可能会影响生物标记物的全面评估[22]。因此,需要对候选的预后预测因子进行全面的评估是必要的。本研究多因素分析表明vasohibin-1和MACC1蛋白的阳性表达以及TNM分期是影响LSCC患者生存时间的独立预后因素。Spearman等级相关分析显示,vasohibin-1蛋白与MACC1蛋白的表达呈正相关关系。MACC1蛋白的异常增高促进肿瘤细胞的增殖,且参与了肿瘤组织新生血管的形成[23];MACC1还可以通过上调VEGF的表达而促进肿瘤组织的血管生成及快速增殖[18];另一方面快速增殖肿瘤细胞自身也可以通过分泌VEGF和FGF-2诱导新生血管的形成以满足其快速生长所需的营养和氧,同时合成更多的vasohibin-1蛋白,进一步促进了肿瘤组织的浸润和转移。
综上所述,vasohibin-1和MACC1的异常表达参与了LSCC的发展、侵袭及转移等过程。因此,可以通过联合检查LSCC患者vasohibin-1和MACC1蛋白的表达,作为预测LSCC患者浸润、转移及预后的指标之一。
| [1] | Torre LA, Bray F, Siegel RL, et al. Global cancer statistics, 2012[J]. CA Cancer J Clin, 2015, 65(2): 87-108. DOI: 10.3322/caac.21262. |
| [2] | Chen W, Zheng R, Baade PD, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-32. DOI: 10.3322/caac.21338. |
| [3] | Ramalingam SS, Owonikoko TK, Khuri FR. Lung cancer: new biological insights and recent therapeutic advances[J]. CA Cancer J Clin, 2011, 61(2): 91-112. DOI: 10.3322/caac.v61:2. |
| [4] | Watanabe K, Hasegawa Y, Yamashita H, et al. Vasohibin as an endothelium-derived negative feedback regulator of angiogenesis[J]. J Clin Invest, 2004, 114(7): 898-907. DOI: 10.1172/JCI200421152. |
| [5] | Kimura H, Miyashita H, Suzuki Y, et al. Distinctive localization and opposed roles of vasohibin-1 and vasohibin-2 in the regulation of angiogenesis[J]. Blood, 2009, 113(19): 4810-8. DOI: 10.1182/blood-2008-07-170316. |
| [6] | Affara M, Sanders D, Araki H, et al. Vasohibin-1 is identified as a master-regulator of endothelial cell apoptosis using gene network analysis[J]. BMC Genomics, 2013, 14: 23. DOI: 10.1186/1471-2164-14-23. |
| [7] | Kosaka T, Miyazaki Y, Miyajima A, et al. The prognostic significance of vasohibin-1 expression in patients with prostate cancer[J]. Br J Cancer, 2014, 32(15, S): 2123-9. |
| [8] | Stein U, Walther W, Arlt F, et al. MACC1, a newly identified key regulator of HGF-MET signaling, predicts colon cancer metastasis[J]. Nat Med, 2009, 15(1): 59-67. DOI: 10.1038/nm.1889. |
| [9] | Stein U, Smith J, Walther W, et al. MACC1 controls Met: what a difference an Sp1 site makes[J]. Cell Cycle, 2009, 8(15): 2467-9. DOI: 10.4161/cc.8.15.9018. |
| [10] | Ren B, Zakharov V, Yang Q, et al. MACC1 is related to colorectal cancer initiation and early-stage invasive growth[J]. Am J Clin Pathol, 2013, 140(5): 701-7. DOI: 10.1309/AJCPRH1H5RWWSXRB. |
| [11] | Wu S, Yu L, Wang D, et al. Aberrant expression of CD133 in non-small cell lung cancer and its relationship to vasculogenic mimicry[J]. BMC Cancer, 2012, 12: 535. DOI: 10.1186/1471-2407-12-535. |
| [12] | Heishi T, Hosaka T, Suzuki Y, et al. Endogenous angiogenesis inhibitor vasohibin1 exhibits Broad-Spectrum antilymphangiogenic activity and suppresses lymph node metastasis[J]. Am J Pathol, 2010, 176(4): 1950-8. DOI: 10.2353/ajpath.2010.090829. |
| [13] | Kern J, Bauer M, Rychli K, et al. Alternative splicing of vasohibin-1 generates an inhibitor of endothelial cell proliferation, migration, and capillary tube formation[J]. Arterioscler Thromb Vasc Biol, 2008, 28(3): 478-84. DOI: 10.1161/ATVBAHA.107.160432. |
| [14] | Hosaka T, Kimura H, Heishi T, et al. Vasohibin-1 expression in endothelium of tumor blood vessels regulates angiogenesis[J]. Am J Pathol, 2009, 175(1): 430-9. DOI: 10.2353/ajpath.2009.080788. |
| [15] | Li D, Zhou K, Wang S, et al. Recombinant adenovirus encoding vasohibin prevents tumor angiogenesis and inhibits tumor growth[J]. Cancer Sci, 2010, 101(2): 448-52. DOI: 10.1111/cas.2010.101.issue-2. |
| [16] | Miyazaki Y, Kosaka T, Mikami S, et al. The prognostic significance of vasohibin-1 expression in patients with upper urinary tract urothelial carcinoma[J]. Clin Cancer Res, 2012, 18(15): 4145-53. DOI: 10.1158/1078-0432.CCR-12-0073. |
| [17] | 周龙书, 李李, 史文静. Vasohibin-1、VEGF在子宫内膜腺癌中的表达及意义[J]. 中国妇幼保健, 2015, 30(3): 350-2. |
| [18] | Wang L, Zhou R, Zhao Y, et al. MACC-1 promotes Endothelium-Dependent angiogenesis in gastric cancer by activating TWIST1/ VEGF-A signal pathway[J]. PLoS One, 2016, 11(6): e0157137. DOI: 10.1371/journal.pone.0157137. |
| [19] | Wang Z, Li Z, Wu C, et al. MACC1 overexpression predicts a poor prognosis for non-small cell lung cancer[J]. Med Oncol, 2014, 31(1): 790. DOI: 10.1007/s12032-013-0790-6. |
| [20] | Zhen T, Dai S, Li H, et al. MACC1 promotes carcinogenesis of colorectal Cancer via β-catenin signaling pathway[J]. Oncotarget, 2014, 5(11): 3756-69. DOI: 10.18632/oncotarget.v5i11. |
| [21] | Zhou L, Yu L, Zhu B, et al. Metastasis-associated in colon cancer-1 and aldehyde dehydrogenase 1 are metastatic and prognostic biomarker for non-small cell lung cancer[J]. BMC Cancer, 2016, 16(1): 876. DOI: 10.1186/s12885-016-2903-z. |
| [22] | Koelzer VH, Herrmann P, Zlobec I, et al. Heterogeneity analysis of metastasis associated in colon cancer 1(MACC1) for survival prognosis of colorectal cancer patients: a retrospective cohort study[J]. BMC Cancer, 2015, 15: 160. DOI: 10.1186/s12885-015-1150-z. |
| [23] | Sun L, Duan J, Jiang Y, et al. Metastasis-associated in colon cancer-1 upregulates vascular endothelial growth factor-C/D to promote lymphangiogenesis in human gastric cancer[J]. Cancer Lett, 2015, 357(1): 242-53. DOI: 10.1016/j.canlet.2014.11.035. |
 2017, Vol. 37
2017, Vol. 37

