2. 中国人民解放军 458医院病理科,广东 广州 510602 ;
3. 南方医科大学基础医学院 肿瘤研究所,广东 广州 510515
2. Department of Pathology, 458 Hospital of PLA, Guangzhou 510602, China ;
3. Cancer Research Institute, School of Basic Medical Sciences, Southern Medical University, Guangzhou 510515, China
人上腭、肺及鼻咽上皮克隆(palate, lung and nasal epithelium clone, PLUNC)家族包含10个成员,该家族成员集中位于20号染色体上不到300 kb的一段狭窄区域[1]。因该家族所有成员蛋白质结构均含杀菌/通透性增强蛋白(bactericidal/permeability-increasing protein, BPI)结构域,因此PLUNC家族也被称为含BPI折叠结构蛋白家族,据此也推测该家族成员具有中和内毒素及杀菌的作用[2]。根据蛋白的相对分子质量,PLUNC家(SPLUNC1)也被称为SPURT、LUNX、NASG和BPIFA1,研究发现SPLUNC1主要表达在鼻咽及呼吸道的上皮组织中,在维持气道表面液体容量及压力[3-5]以及上呼吸道的炎症应答[6-8]中可能发挥重要作用。目前,关于SPLUNC1基因功能的研究主要集中在呼吸系统疾病中,但其确切生物学功能及其在人体内表达的精确细胞学定位仍不明确,因此,本文采用原位杂交的方法,检测人体内表达SPLUNC1基因的细胞类型,为深入揭示SPLUNC1基因的调控机制和生物学功能提供依据。
1 材料和方法 1.1 材料 1.1.1 组织标本收集2003~2005年间南方医院和中国人民解放军第458医院病理科存档的上腭、颌下腺、腮腺、鼻咽慢性炎、气管、支气管、食管、肺、胃、空肠、结肠、胆囊、前列腺、子宫内膜及相应肿瘤组织的石蜡标本,每种组织选取5例不同的病例。全部组织标本经10%中性福尔马林液固定,常规石蜡包埋,4μm厚切片,保存备用。
1.1.2 试剂敏感性加强型原位杂交试剂盒(MK1030)购自武汉博士德生物工程有限公司;DAB显色试剂盒(DAB-0031)购自福建迈新生物技术开发有限公司。
1.2 方法 1.2.1 探针设计采用Primer 5.0软件设计,序列为:5'-TGTGAGAGATAAGCAGGAGAG-3',由上海英俊生物公司合成并进行地高辛标记。
1.2.2 原位杂交按试剂盒操作说明进行。将石蜡切片常规二甲苯脱蜡至水,用新鲜配制的0.5%H2O2/甲醇溶液处理切片30 min,来灭活内源性过氧化物酶;然后将3%柠檬酸稀释的胃蛋白酶滴加于切片上,37℃消化30 min以暴露mRNA核酸片段;湿盒底部加入20%甘油20 mL,每张切片上滴加预杂交液,37℃孵育4 h进行预杂交;滴加20μL杂交液(探针浓度为8μg/mL)于40℃杂交过夜。用37℃左右的2×SSC、0.5×SSC和0.2×SSC液体分别洗涤切片1次;切片经封闭液封闭后,加生物素化鼠抗地高辛液体于37℃孵育60 min进行标记;经SABC-POD孵育后,滴加生物素过氧化物酶于37℃孵育30 min,用新鲜配置的DAB溶液进行显色;苏木素复染,二甲苯透明后,中性树胶封固。实验中以无探针的预杂交液作为阴性对照。
1.2.3 原位杂交结果判定根据染色结果,以无色为阴性,以棕黄色或棕褐色为阳性信号[9]。
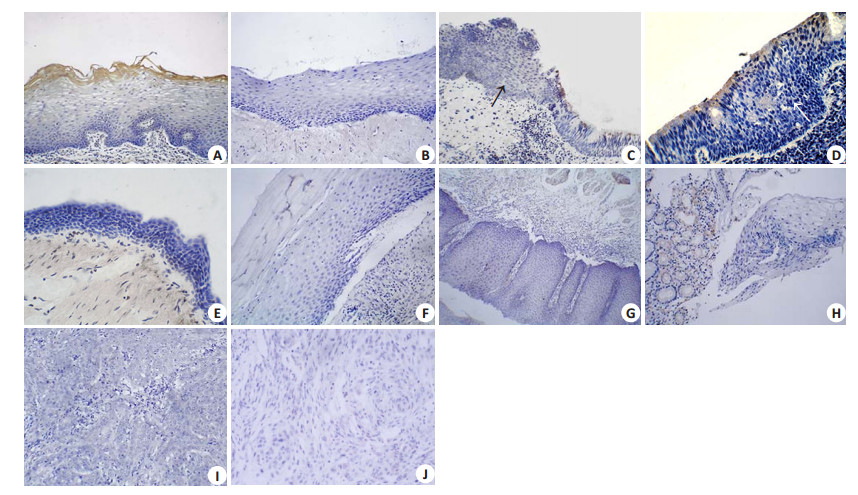
2 结果 2.1 鳞状上皮中SPLUNC1基因的表达原位杂交检测结果显示:在上腭、表皮、鼻咽部化生的鳞状上皮、气管部化生的鳞状上皮、食管及食管-贲门部的鳞状上皮、宫颈部化生的鳞状上皮组织中,全部病例均不表达SPLUNC1基因(图 1A~H)。上腭处的棕色信号定位在鳞状上皮上部的角化层,为非特异性染色。此外,在选取的食管和肺的鳞状细胞癌组织中,全部肿瘤细胞也不表达SPLUNC1基因(图 1I、J)。
|
图 1 原位杂交检测SPLUNC1基因在鳞状上皮细胞及鳞状细胞癌中的表达 Figure 1 Identification of SPLUNC1gene expression in squamous epithelium and squamous cell carcinoma by in situ hybridization. A: Palate (Original magnification:×200); B: Epidermis (×200); C, D: Metaplastic squamous epithelium in nasopharynx (×200); E: Metaplastic squamous epithelium in trachea (×200); F: Metaplastic squamous epithelium in cervix (×200); G: Esophagus (×100); H: Junctionof esophagus with cardiaof stomach (×200);I: Squamous cell carcinoma of esophagus (×100);J: Squamous cell carcinoma of lung (×200). |
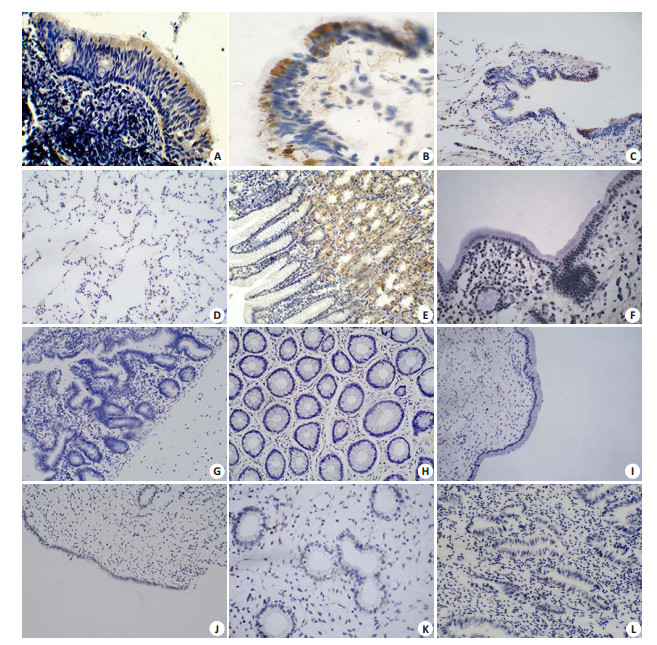
在选取的鼻咽部和气管的假复层纤毛柱状上皮细胞中,全部病例均显示有SPLUNC1基因的表达(图 2A、B),阳性信号定位在柱状上皮的胞浆内。SPLUNC1在支气管部的假复层纤毛柱状上皮细胞中也有表达,但与气管中的表达的程度相比有所减弱(图 2C);在肺组织中其表达水平显著下降,在肺泡上皮细胞中SPLUNC1基因完全不表达(图 2D)。在胃、胆囊、空肠、结肠的粘膜层以及子宫内膜和宫颈部的单层柱状上皮中均不表达SPLUNC1(图 2E~J)。此外,无论是在增生期样子宫内膜还是分泌期样子宫内膜组织中,SPLUNC1均呈阴性表达(图 2K、L)。
|
图 2 原位杂交检测SPLUNC1在柱状上皮细胞中的表达 Figure 2 Identification of SPLUNC1geneexpression in columnarepithelium by in situ hybridization. A and B: Pseudostratified ciliated columnar epithelium in nasopharynx and trachea (Original magnification:×400); C: Pseudostratified ciliated columnar epithelium in bronchus (×200); D: Pulmonaryalveoli epithelium(×200); E: Stomach (×200); F: Gallbladder (×400); G: Jejunum (×200); H: Colon (×200); I: Cervix (×200); G: Endometrium (×200); K: Proliferative phase of endometrium (×400); L: Secretory phase of endometrium (×400). |
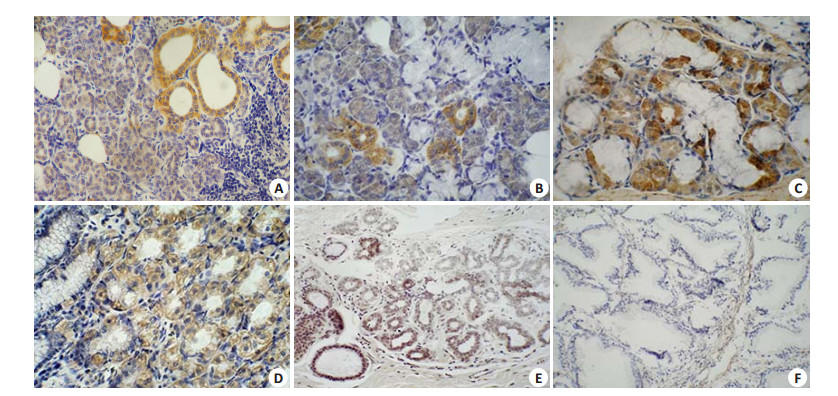
在腮腺和颌下腺组织中,SPLUNC1在腺导管上皮和浆液性腺细胞中也有阳性表达,而颌下腺的粘液腺细胞不表达SPLUNC1基因(图 3A、B)。在鼻咽部、和肺的腺体中,SPLUNC1表达的阳性信号也定位在浆液性腺体腺泡细胞中(图 3C)。胃粘膜固有层中胃底腺的壁细胞也存在SPLUNC1的阳性表达(图 3D)。乳腺小叶的腺泡和导管中均表达SPLUNC1,但在前列腺的腺体中却不表达SPLUNC1基因(图 3E、F)。
|
图 3 原位杂交检测SPLUNC1基因在腺上皮细胞中的表达 Figure 3 Identification of SPLUNC1geneexpression in glandular epithelium by in situ hybridization. A: Parotid gland (Original magnification:×200); B: Submandibular gland (×400); C: Submucosal gland of nasopharynx (×400); D: Stomach (×200); E: Mammary gland (×200); F: prostate (×200). |
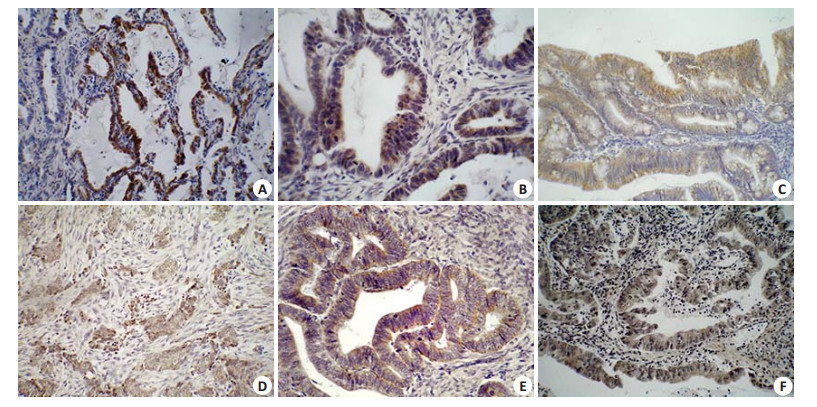
此外,在肺、胃、结肠、乳腺、子宫内膜和宫颈等部位的腺癌组织中,也证实有SPLUNC1基因的阳性表达(图 4)。
|
图 4 原位杂交检测SPLUNC1基因在腺癌中的表达 Figure 4 Identification of SPLUNC1geneexpression in well-differentiated adencarcinoma tissue by in situ hybridization. A: Adeno-carcinoma of lung (Original magnification:×200); B: Gastric adenocarcinoma (×400); C: Adenocarcinoma of colon (×200); D: Breast cancer (×200); E: Endometrialadenocarcinoma (×400);F: Adenocarcinoma of uterine cervix (×200). |
一个基因在某一生理过程中的表达变化往往对其功能有重要提示作用。已有多个研究小组采用cDNA微阵列杂交或RT-PCR方法对SPLUNC1基因的表达水平进行了研究,并在此基础上推测了SPLUNC1基因的功能[10-11]。但这些报道所选用的研究材料均为组织块(block),组织块是由各种类型的上皮细胞、成纤维细胞以及炎细胞等多种细胞成份构成的混杂体,因此,从组织块中提取的RNA所进行的后续研究不能特异地展示某一类型细胞中的表达情况,不可避免地会导致结果存在误差[12]。虽然Zhou等[13]通过自制抗体,结合免疫组织化学方法检测了SPLUNC1蛋白的组织学分布模式,但由于受组织材料选材的限制,研究结果也存在一定的局限性。因此,我们收集了人体37种组织,采用原位杂交的方法,检测SPLUNC1基因的表达情况,以期能更全面而准确的分析SPLUNC1基因在人体主要上皮组织中的表达分布特征。
本研究结果发现,在鼻咽、气管部的假复层纤毛柱状上皮表达SPLUNC1,在支气管的假复层纤毛柱状上皮中也有一定程度的SPLUNC1表达,但较气管中的表达减弱;在肺泡中检测不到SPLUNC1的表达,这些研究结果与以往的研究结论相一致[14]。此外,我们发现在唾液腺、乳腺等部位的导管上皮和浆液性腺上皮细胞以及胃固有层中的壁细胞中也存在SPLUNC1的表达,而粘液腺细胞不表达SPLUNC1基因,说明SPLUNC1的表达可能与这些腺上皮的蛋白质分泌功能有关。
我们还发现在上腭和食管被覆的鳞状上皮细胞中不表达SPLUNC1基因,甚至在鼻咽、气管和宫颈部鳞状上皮化生的细胞,以及食管和肺鳞状细胞癌的肿瘤细胞中也不表达SPLUNC1,说明SPLUNC1表达具有明显的细胞特异性,其特异地表达在呼吸道假复层纤毛柱状上皮以及导管上皮和浆液性腺上皮中,而不表达于鳞状细胞起源的组织,SPLUNC1在不同类型细胞中的表达差异可能与该类型细胞的特定功能有关,这一结果提示SPLUNC1基因的表达可能是一个与分化有关的基因,它的正确表达受到复杂而精密的调控程序控制,转录调控机制的研究将对其功能的全面揭示具有重要意义,值得深入研究。然而,既往采用组织块进行研究的结果显示,SPLUNC1在鼻咽部、鼻咽癌及肺鳞癌中均有所表达[15-16],与我们的研究结论不一致;由于我们的研究证实鼻咽和肺等部位粘膜下的浆液腺细胞中也存在SPLUNC1的阳性表达,我们推测这些研究结论的差异可能是由组织块中混杂的腺体等其他组织成分造成的,因此,采用原位杂交或免疫组化方法能更加准确地研究基因/蛋白的表达分布特征,避免组织块中多种细胞成份混杂所导致的误差出现。
除此之外,我们还发现,在胃粘膜、肠粘膜、宫颈及子宫内膜等部位的单层柱状上皮也不表达SPLUNC1,而在胃、结肠、宫颈及子宫内膜等腺癌组织中SPLUNC1呈阳性表达,这提示SPLUNC1很可能是这些肿瘤的潜在标志物之一,具有潜在的诊断价值,值得进一步研究。
总之,我们通过原位杂交的方法对SPLUNC1基因的表达进行了精确的细胞学定位研究,为进一步探讨该基因的表达调控机制和生物学功能奠定了良好的基础,也为肿瘤的诊断和治疗提供了新的理论依据。
| [1] |
Bingle CD, Leclair EE, Havard S, et al. Phylogenetic and evolutionary analysis of the PLUNC gene family[J].
Protein Science,2004, 13 (2) : 422-30.
DOI: 10.1110/ps.03332704. ( 0) 0)
|
| [2] |
Beamer LJ. Structure of human BPI (bactericidal/permeabilityincreasing protein) and implications for related proteins[J].
Biochem Soc Trans,2003, 31 (Pt 4) : 791-4.
( 0) 0)
|
| [3] |
Garcia-Caballero A, Rasmussen JE, Gaillard E, et al. SPLUNC1 regulates airway surface liquid volume by protecting ENaC from proteolytic cleavage[J].
Proc Natl Acad Sci USA,2009, 106 (27) : 11412-7.
DOI: 10.1073/pnas.0903609106. ( 0) 0)
|
| [4] |
Gakhar L, Bartlett JA, Penterman JA, et al. PLUNC is a novel airway surfactant protein with Anti-Biofilm activity[J].
PLoS One,2010, 5 (2) : e9098.
DOI: 10.1371/journal.pone.0009098. ( 0) 0)
|
| [5] |
Mcgillivary G, Bakaletz LO. The multifunctional host defense peptide SPLUNC1 is critical for homeostasis of the mammalian upper airway[J].
PLoS One,2010, 5 (10) : e13224.
DOI: 10.1371/journal.pone.0013224. ( 0) 0)
|
| [6] |
Bingle L, Barnes FA, Cross SS, et al. Differential epithelial expression of the putative innate immune molecule SPLUNC1 in Cystic Fibrosis[J].
Respir Res,2007, 8 : 79.
DOI: 10.1186/1465-9921-8-79. ( 0) 0)
|
| [7] |
Tsou YA, Lin CD, Chen HC, et al. Interleukin-13 inhibits Lipopolysaccharide-Induced BPIFA1 expression in nasal epithelial cells[J].
PLoS One,2015, 10 (12) : e0143484.
DOI: 10.1371/journal.pone.0143484. ( 0) 0)
|
| [8] |
Leeming GH, Kipar A, Hughes DJ, et al. Gammaherpesvirus infection modulates the temporal and spatial expression of SCGB1A1 (CCSP) and BPIFA1 (SPLUNC1) in the respiratory tract[J].
Lab Invest,2015, 95 (6) : 610-24.
DOI: 10.1038/labinvest.2014.162. ( 0) 0)
|
| [9] |
徐小艳, 刘红伟, 姜黄, 等. 联合检测细胞蜡块中的napsin A和甲状腺转录因子-1有助于肺腺癌胸水的诊断[J].
南方医科大学学报,2015, 35 (11) : 1610-3.
( 0) 0)
|
| [10] |
Bingle CD, Bingle L. Characterisation of the human plunc gene, a gene product with an upper airways and nasopharyngeal restricted expression pattern[J].
Biochim Biophys Acta,2000, 1493 (3) : 363-7.
DOI: 10.1016/S0167-4781(00)00196-2. ( 0) 0)
|
| [11] |
Zhang B, Nie X, Xiao B, et al. Identification of tissue-specific genes in nasopharyngeal epithelial tissue and differentially expressed genes in nasopharyngeal carcinoma by suppression subtractive hybridization and cDNA microarray[J].
Genes Chromosomes Cancer,2003, 38 (1) : 80-90.
DOI: 10.1002/(ISSN)1098-2264. ( 0) 0)
|
| [12] |
Donnem T, Lonvik K, Eklo K, et al. Independent and tissuespecific prognostic impact of miR-126 in nonsmall cell lung cancer: coexpression with vascular endothelial growth factor-A predicts poor survival[J].
Cancer,2011, 117 (14) : 3193-200.
DOI: 10.1002/cncr.25907. ( 0) 0)
|
| [13] |
Zhou HD, Fan SQ, Zhao J, et al. Tissue distribution of the secretory protein, SPLUNC1, in the human fetus[J].
Histochem Cell Biol,2006, 125 (3) : 315-24.
DOI: 10.1007/s00418-005-0070-4. ( 0) 0)
|
| [14] |
Di YP, Harper R, Zhao Y, et al. Molecular cloning and characterization of spurt, a human novel gene that is retinoic acid-inducible and encodes a secretory protein specific in upper respiratory tracts[J].
J Biol Chem,2003, 278 (2) : 1165-73.
DOI: 10.1074/jbc.M210523200. ( 0) 0)
|
| [15] |
何志巍, 谢鹭, 许亮国, 等. 一个与人鼻咽癌相关新基因的克隆[J].
科学通报,2000, 45 (11) : 1168-73.
( 0) 0)
|
| [16] |
Iwao K, Watanabe T, Fujiwara Y, et al. Isolation of a novel human lung-specific gene, LUNX, a potential molecular marker for detection of micrometastasis in non-small-cell lung cancer[J].
Inte J Cancer,2001, 91 (4) : 433-7.
DOI: 10.1002/(ISSN)1097-0215. ( 0) 0)
|
 2016, Vol. 36
2016, Vol. 36