2. 中山大学附属第三医院皮肤科,广东 广州 510630
2. Department of Dermatology and Venerology, Third Affiliated Hospital of Sun Yat-sen University, Guangzhou 510630, China
着色芽生菌病(CBM)是由暗色真菌引起的皮肤及皮下组织的慢性肉芽肿性疾病。该病治疗上尚无统一标准,具有复发率高、致残和致畸等特点,所以其临床治疗是非常棘手的难题[1-3]。CBM主要流行于热带和亚热带地区,着色霉为其最常见的病原菌,其中裴氏着色霉(Fonsecaea pedrosoi)主要分布于南美地区,而在中国南方地区F.monophora占75%,F.nubica占25% [4-5]。由F.nubica所致CBM病例具有详细临床资料的报道迄今国内外仅有7例[6-7]。CBM单一系统抗真菌药物治疗时间漫长、费用昂贵、菌株耐药,人们在不断地探索联合治疗的方法。基于长脉冲1064 nm Nd:YAG激光作用可深达表皮下4~6 mm,可被黑色素基团吸收,具有选择性的光热作用,我们推测它对产生黑色素的CBM病原菌有治疗作用。我们按照脱毛的治疗参数使用该激光联合特比萘芬及外科手术成功治愈CBM一例并申请到科研课题。本例从病原真菌鉴定、体外药物敏感试验、动物实验等方面对F.nubica进行系统研究,并首次采用长脉冲1064 nm Nd:YAG激光联合口服特比萘芬治疗,随访20个月无复发。现将临床和实验研究结果报道如下。
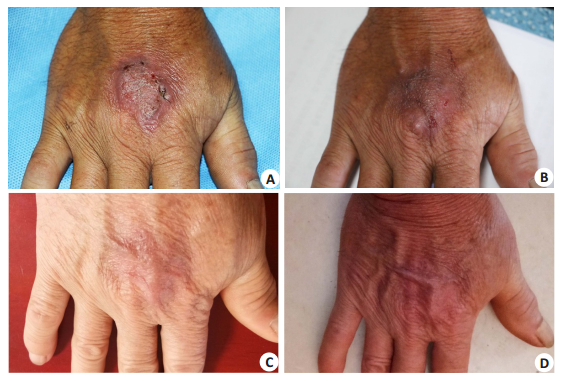
1 临床资料患者,男,60岁,2017年8月10日就诊于我院皮肤科门诊,诉右手背暗红色斑块10个月。起病前手部有外伤史。否认糖尿病等其他基础病史。体格检查:右手背约30 mm×40 mm大小暗红色斑块,表面疣状增生,部分破溃、结痂(图 1A)。
|
图 1 CBM患者皮损治疗和随访的临床表现 Fig.1 Clinical characteristics of the skin lesions before and after therapy. A: There is an erythematous plaque with verrucous hyperplasia surface on the back of the right hand, and ulceration can be observed; B: The lesion is obviously improved clinically after laser irradiation combined with terbinafine therapy for 8 weeks; C: The local skin is almost normal in appearance at 12-months after the treatment; D: Normal skin appearance at 20 months. |
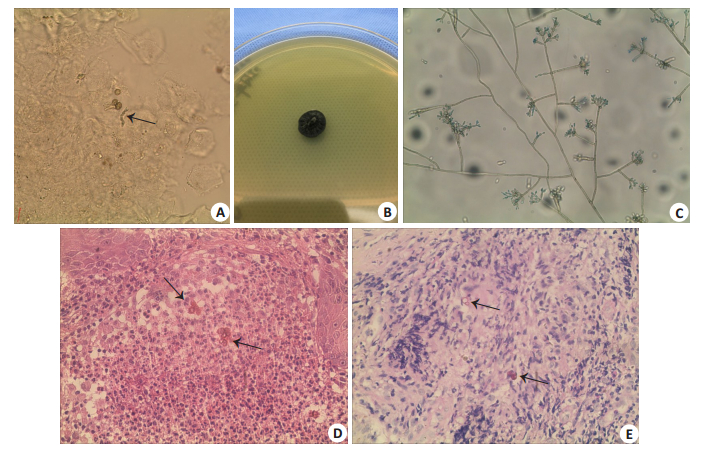
无菌钝刀刮取右手皮损点状黑痂及痂下分泌物加10% KOH溶液直接镜检,镜下见多个散在或成堆的棕色、圆形、厚壁的硬壳小体,部分有分隔(图 2A)。
|
图 2 患者皮损真菌直接镜检、培养及组织病理表现 Fig.2 Direct microscopic examination of the lesion, fungal culture, and histopathological examination. KOH wet mount of the sample and histopathological examination from the lesion showed muriform cells (A: ×400; D: HE staining, ×400; E: PAS staining, ×400). B: Macroscopic appearance of the colony; C: Microculture of the colony (×400). |
真皮乳头层小血管增生、扩张充血,可见由多量中性粒细胞、组织细胞及多核巨细胞构成的肉芽肿。组织中可见散在或成堆的棕色、圆形、厚壁的硬壳小体。PAS染色(+)(图 2D、E)。
2.3 真菌培养皮损组织接种于沙堡培养基,26 ℃培养2周后可见直径约2 cm大小灰黑色绒毛状菌落生长(图 2B)。小培养镜下可见枝孢型产孢,分生孢子链短,2~3个孢子,椭圆形或长椭圆形(图 2C)。形态学鉴定为着色霉属真菌。
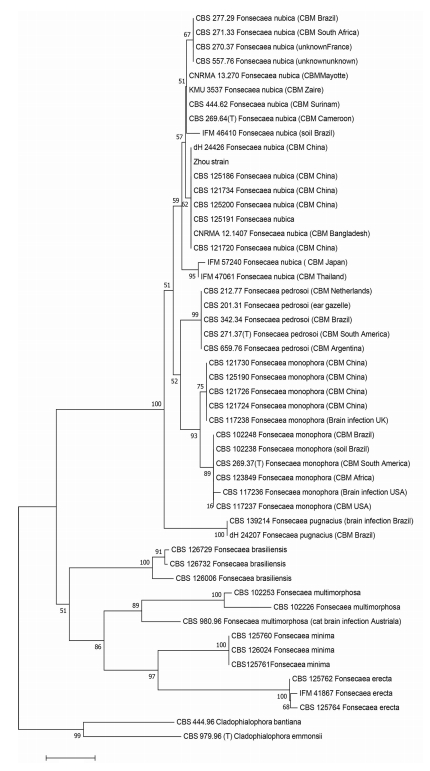
2.4 分子生物学鉴定用Biospin真菌基因组DNA提取试剂盒提取培养菌落的DNA,然后使用ITS1和ITS4作为引物对DNA进行PCR扩增和测序。结合NCBI和CBS数据库中所提交的着色霉临床菌株参比序列采用邻接法(NJ)建立种系发生树,结果提示本临床分离株在F.nubica类群(图 3),与F.nubica菌株KX078407具有99%的同源性。分子生物学鉴定致病菌为F.nubica。
|
图 3 Fonsecaea菌株的进化树 Fig.3 Phylogenetic trees of Fonsecaea species. |
参照美国国家临床实验室标准委员会(NCCLS)颁布的产孢丝状真菌液基微量法(M38-A2)对该菌株进行体外药敏试验[8]。将F.nubica菌株转种于PDA培养基上28 ℃培养7 d以保证其活力,用0.9%无菌生理盐水1 mL在培养基上冲刷洗脱纯化的菌落,制成菌悬液,静置3~5 min后,取上层均质液体至无菌小管,震荡15 s。用RPMI 1640培养基稀释,血细胞计数板计数,将菌液浓度调整至(1~5)×103 CFU/mL。
2.5.2 药敏反应板的制备将阿尼芬净、米卡芬净、卡泊芬净、氟康唑、5-氟胞嘧啶、伊曲康唑、特比萘芬、伏立康唑、两性霉素共9种抗真菌药物(美国Sigma公司)进行倍比稀释,将氟康唑的药物浓度调整为128、64、32、16、8、4、2、1、0.5和0.25 μg/mL,其余药物调整为32、16、8、4、2、1、0.5、0.25、0.125和0.0625 μg/mL。取2块无菌96孔板,在每一行的1号孔中加入RPMI 1640 100 μL作为空白对照;2~11号各孔均加入菌液50 μL,并按照浓度梯度分别加入对应的药物溶液各50 μL;12号孔只加100 μL菌液作为阳性对照。将药敏板置于28 ℃恒温培养箱中静止孵育48~72 h后,根据国际上公认的美国国家临床实验室标准化研究所(CLSI)制定的标准进行结果判读,将与生长对照孔相比较生长抑制率大于80%的最小药物浓度作为药物的最小抑菌浓度(MIC)值。
2.5.3 结果阳性对照组菌株(近平滑念珠菌)生长良好,各抗真菌药物的MIC值如下:阿尼芬净 > 8 μg/mL,米卡芬净 > 8 μg/mL,卡泊芬净 > 8 μg/mL,氟康唑 > 256 μg/mL,5-氟胞嘧啶8 μg/mL,伊曲康唑0.25 μg/mL,特比萘芬0.125 μg/mL,伏立康唑 > 8 ug/mL,两性霉素2 μg/mL。
2.6 长脉冲1064 nm Nd:YAG激光对大鼠模型的作用 2.6.1 主要材料20只7W-9W的SPF级雌性Wistar大鼠,由南方医科大学实验动物中心提供(许可证号SCXK(粤)2016-0041),已通过伦理委员会批准、并按实验室要求饲养;长脉冲1064 nm Nd:YAG激光治疗仪(吉林省科英激光技术有限责任公司)。
2.6.2 菌悬液制备方法同药敏试验,将菌液浓度调整至1×107/mL。
2.6.3 动物模型的制备参照既往文献[9-10]进行着色芽生菌病Wistar大鼠动物模型的制备。20只Wistar大鼠选取背部面积约4 cm×4 cm区域脱毛。麻醉后于背部脱毛区皮下注射0.2 mL菌悬液,复苏后放回笼中。测量皮损直径,选取第30 d皮损平均直径为8.0 mm的14只大鼠随机分为模型对照组和激光实验组,每组7只。模型对照组30、45、60、90 d,分别将大鼠安乐死后取皮损分为两部分,将一部分皮损研磨后接种至PDA平皿,置于26 ℃孵箱中培养,另一部分皮损置于10%甲醛溶液中固定24 h,进行制片、HE染色。30、45、60、90 d皮损组织真菌培养均可见暗色菌落生长,组织病理见棕色厚壁孢子、透亮短菌丝。真菌学和组织病理结果提示着色芽生菌病Wistar大鼠动物模型制备成功。
2.6.4 实验方法实验动物分两个组:实验组和对照组。实验组选择第30 d至60 d皮损较稳定时段进行长脉冲1064 nm Nd:YAG激光照射皮损。照射参数:脉宽3.0 ms,频率4 Hz,能量密度24 J/cm2,光斑直径3 mm。照射方法:每个皮损照射3轮,每轮照射确保光斑覆盖全部皮损,光斑可有小面积重叠,间隔时间30 s,2/W共8次。激光实验组45、60 d,即第5次激光治疗前4 d,第8次激光照射后3 d,分别行真菌培养、病理活检,方法同上。对照组不做激光照射。
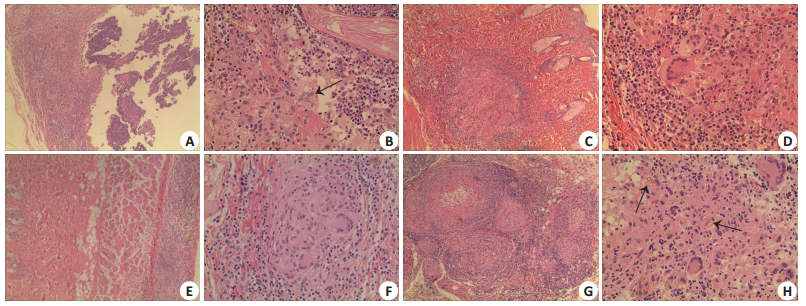
2.6.5 实验结果激光实验组45、60 d皮损真菌培养均阳性。45 d时,模型对照组真皮内脓肿形成,脓肿中央大量中性粒细胞聚集,部分组织坏死,可见棕色厚壁孢子、透亮短菌丝(图 2A、B);激光实验组真皮内炎性肉芽肿改变,较模型对照组多淋巴细胞浸润,中央多核巨细胞(图 2E、F)。60 d时,模型对照组脓肿范围较45 d时范围缩小,组织较致密,真皮内炎症反应区域见多核巨细胞,少量棕色厚壁孢子,脓肿周围少量淋巴细胞浸润(图 2C、D);激光实验组真皮内可见炎性肉芽肿被胶原纤维分割,间隔内大量淋巴细胞浸润,周围胶原纤维增生、中央有坏死,脓肿内见棕色厚壁孢子(图 2G、H)。
3 诊断与治疗结合临床资料和实验室检查结果,本例患者确诊为由F.nubica所致的着色芽生菌病。
根据体外药敏结果和动物实验初步结果,予以患者口服特比萘芬片0.25 bid,外涂萘替芬酮康唑乳膏Bid,以及长脉冲1064 nm Nd:YAG激光照射局部皮损治疗。激光照射参数同上动物实验,1次/周,连续照射8次后停用。治疗2周后,皮损真菌直接镜检阴性,此后连续复查6次均为阴性。8周后皮损明显变平好转(图 1B)。随访至12个月时原皮损部位皮肤接近正常(图 1C),至20个月时局部皮肤恢复正常(图 1D)。
4 讨论着色霉属是着色芽生菌病最常见的病原菌属之一,该属的临床致病菌种包括F.pedrosoi、F.monophora、F.nubica和F.pugnacius。传统的形态学难以将着色霉鉴定至菌种水平,需要分子生物学鉴定,而ITS是推荐的DNA条形码[11]。2010年Najafzadeh等[12]通过分子系统分类学方法首次提出F.nubica新的菌种,均分离自CBM病例,但是欠缺详细的临床资料。回顾文献,连同本病例目前国内外总共有8例由F.nubica引起的CBM详细病例报道[6-7, 13-17],最早是由Slesak等[18]在2011年报道的,系统口服抗真菌药物疗程多数超过3个月,仅2例完善药敏试验,其中1例伊曲康唑治疗16周,随访8个月无复发。另1例特比萘芬治疗1个月好转,无后续结果报道。Najafzadeh等[19]应用M38-A2方案对55株着色霉进行体外药敏试验,结果显示所有菌株对ITZ,VCZ,POS,ITZ和ISA均有较低的MIC值。欧洲ESCMID/ECMM的CBM治疗指南推荐伊曲康唑联合手术治疗(推荐级别AII)或者特比奈芬联合手术治疗(推荐级别BIII),个别顽固难治病例还推荐联合液氮冷冻治疗(推荐级别BIII)[20]。本病例采用M38-A2方案对致病F.nubica进行9种抗真菌药物的体外药敏试验,结果显示特比萘芬MIC值最小(0.125 μg/mL),其临床系统应用特比萘芬治疗效果显著,为F.nubica感染系统抗真菌治疗提供了依据。
目前已经有二氧化碳激光、光动力等激光用于治疗CBM的研究[21-24]。口服抗真菌药物联合以上激光治疗被公认为是治疗CBM的有效方法[1, 21]。二氧化碳激光碳化、气化皮损形成局部疤痕,光动力治疗光敏剂昂贵,促使我们寻找微创、经济、便于广泛开展的激光治疗。长脉冲1064 nm Nd:YAG激光在临床上广泛用于脱毛[25]、色素性、血管性[26]疾病,甚至用于皮肤肿瘤治疗[27],照射治疗过程表皮无损伤、产生的疼痛可以耐受。近几年运用范围延伸至甲真菌病,其有效性和安全性受到广泛肯定[28-30]。本研究成功制备CBM的Wistar大鼠动物模型,激光实验组皮损淋巴细胞浸润较模型对照组明显。淋巴细胞在限制CBM皮损进展中起着非常重要的作用[31],有研究显示无胸腺裸鼠CBM模型皮损可持续1年无变化[32],因此本研究提示长脉冲1064 nm Nd:YAG激光可能诱导Wistar大鼠CBM模型皮肤组织免疫反应类型发生改变,促进皮损修复。同时激光照射后皮损真菌培养阳性,提示该激光在我们使用的参数和方法条件下不能杀死病变中的真菌,必须联合敏感的抗真菌药物系统治疗。本例在药敏试验和动物实验的基础上采用长脉冲1064 nm Nd:YAG激光联合特比萘芬治疗疗程仅8周,疗程结束随访20个月无复发,局部皮肤恢复到正常。
|
图 4 长脉冲1064 nm Nd:YAG激光照射动物模型后病理表现 Fig.4 Histopathology of the lesions in the rat model after long-pulsed 1064 nm Nd: YAG laser irradiation. At 45 days, in the model control group, the dermal abscess formed, a large number of neutrophils gathered in the center of the abscess, and part of the tissue was necrotic. Arrow showed brown thick- walled spores with translucent short hyphae (A, B). In laser experimental group, inflammatory granuloma was seen in the dermis with increased infiltrating lymphocytes and multinucleated giant cells in the center (E, F). At 60 days, the lesion in the model control group showed reduced range of abscess (compared with that at 45 days) and the tissue was dense. The inflammatory reaction in the dermis was highlighted by multinucleated giant cells. A small number of brown thick-walled spores and a few infiltrating lymphocytes were observed around the abscess (C, D). In laser experimental group, the inflammatory granuloma in the dermis was divided by collagen fibers with a large number of infiltrating lymphocytes. The surrounding collagen fibers proliferated with necrotic changes in the center. Brown thick- walled spores were seen in the abscess (G, H)(A, C, E, G: ×100)(B, D, F, H: ×400). |
本研究尚存在一些不足之处,激光干预的能量、次数可做不同组别设置,也可以在实验中加入药物等其他治疗CBM的方法进行比较。同时,本实验可以进一步完善免疫组化及细胞因子的检测,以进一步明确免疫机制。尽管如此,激光治疗着色芽生菌病的积极作用还是令人鼓舞的,可以预见的是长脉冲1064 nm Nd:YAG激光具备对CBM产生免疫调控作用的潜力,该作用机制值得进一步验证及挖掘。而在真菌感染的临床治疗中,其不失为一种可供选择的辅助治疗方法。
| [1] |
Queiroz-Telles F, De HS, Santos DW, et al. Chromoblastomycosis[J]. Clin Microbiol Rev, 2017, 30(1): 233. DOI:10.1128/CMR.00032-16 |
| [2] |
Rasamoelina T, Raharolahy O, Rakotozandrindrainy N, et al. Chromoblastomycosis and sporotrichosis, two endemic but neglected fungal infections in Madagascar[J]. J Mycol Med, 2017, 27(3): 312-24. DOI:10.1016/j.mycmed.2017.08.003 |
| [3] |
Agarwal R, Singh G, Ghosh A, et al. Chromoblastomycosis in India:review of 169 cases[J]. PLoS Negl Trop Dis, 2017, 11(8): e0005534. DOI:10.1371/journal.pntd.0005534 |
| [4] |
Fransisca C, He Y, Chen Z, et al. Molecular identification of chromoblastomycosis clinical isolates in Guangdong[J]. Med Mycol, 2017, 55(8): 851-8. |
| [5] |
Najafzadeh MJ, Sun J, Vicente VA, et al. Molecular epidemiology of Fonsecaea species[J]. Emerg Infect Dis, 2011, 17(3): 464-9. DOI:10.3201/eid1703.100555 |
| [6] |
He LY, Ma JC, Mei X, et al. Successful treatment of chromoblastomycosis of 10-year duration due to Fonsecaea nubica[J]. Mycoses, 2018, 61(4): 231-6. DOI:10.1111/myc.2018.61.issue-4 |
| [7] |
You Z, Yang X, Yu J, et al. Chromoblastomycosis caused by fonsecaea nubica:first report in northern China and literature review[J]. Mycopathologia, 2019, 184(1): 97-105. DOI:10.1007/s11046-018-0307-0 |
| [8] |
CLSI M38-A2 Reference Method for Broth Dilution Antifungal Susceptibility Testing of Filamentous Fungi; Approved StandardSecond Edition, M38A2E[S].
|
| [9] |
Siqueira IM, Ribeiro AM, De Medeiros Nobrega YK, et al. DNAhsp65 vaccine as therapeutic strategy to treat experimental chromoblastomycosis caused by fonsecaea pedrosoi[J]. Mycopathologia, 2013, 175(5/6, SI): 463-75. |
| [10] |
Xie Z, Zhang JM, Xi LY, et al. A chronic chromoblastomycosis model by Fonsecaea monophora in Wistar rat[J]. Med Mycol, 2010, 48(1): 201-6. DOI:10.3109/13693780902785320 |
| [11] |
De Hoog GS, Guarro J, Gene J, et al. Atlas of clinical fungi, 4th web-edn[Z], 2015.
|
| [12] |
Najafzadeh MJ, Sun J, Vicente V, et al. Fonsecaea nubica sp. nov, a new agent of human chromoblastomycosis revealed using molecular data[J]. Med Mycol, 2010, 48(6): 800-6. DOI:10.3109/13693780903503081 |
| [13] |
Shi M, Li X, Feng J, et al. High-resolution melting analysis assay for identification of Fonsecaea species[J]. J Clin Lab Anal, 2018, 32(2): jcla.22257. DOI:10.1002/jcla.2018.32.issue-2 |
| [14] |
Ushigami T, Anzawa K, Mochizuki T. Molecular typing using polymorphisms of the polyketide synthase gene (PKS1) of strains in Japan morphologically identified as Fonsecaea pedrosoi[J]. J Dermatol, 2017, 44(1): 36-42. |
| [15] |
Chen Y, Yin S, Li M, et al. A case of chromoblastomycosis by Fonsecaea nubica indicating a possible insect route of transmission[J]. Mycoses, 2016, 59(10): 662-7. DOI:10.1111/myc.12523 |
| [16] |
Yanagihara S, Kobayashi H, Kamo R, et al. Chromoblastomycosis caused by Fonsecaea nubica:First report from Japan[J]. J Dermatol, 2015, 42(8): 833-4. DOI:10.1111/jde.2015.42.issue-8 |
| [17] |
Sophie B, Coralie Z, Mai Ba H, et al. First case of chromoblastomycosis from Bangladesh[J]. Med Mycol Case Rep, 2015, 10: 1-3. DOI:10.1016/j.mmcr.2015.08.001 |
| [18] |
Slesak G, Inthalad S, Strobel M, et al. Chromoblastomycosis after a leech bite complicated by myiasis:a case report[J]. BMC Infect Dis, 2011, 11(1): 14. DOI:10.1186/1471-2334-11-14 |
| [19] |
Najafzadeh MJ, Badali H, Illnait-Zaragozi MT, et al. In vitro activities of eight antifungal drugs against 55 clinical isolates of Fonsecaea spp[J]. Antimicrob Agents Chemother, 2010, 54(4): 1636-8. DOI:10.1128/AAC.01655-09 |
| [20] |
Chowdhary A, Meis JF, Guarro J, et al. ESCMID and ECMM joint clinical guidelines for the diagnosis and management of systemic phaeohyphomycosis:diseases caused by black fungi[J]. Clin Microbiol Infect, 2014, 20(Suppl 3): 47-75. |
| [21] |
Baltazar LM, Ray A, Santos DA, et al. Antimicrobial photodynamic therapy:an effective alternative approach to control fungal infections[J]. Front Microbiol, 2015, 6(2): 202. |
| [22] |
Hu YX, Huang XW, Lu S, et al. Photodynamic therapy combined with terbinafine against chromoblastomycosis and the effect of PDT on fonsecaea monophora in vitro[J]. Mycopathologia, 2015, 179(1/2): 103-9. |
| [23] |
Liu ZH, Xia XJ. Successful sequential treatment with itraconazole and ALA-PDT for chromoblastomycosis because of Alternaria alternata[J]. Dermatol Ther, 2014, 27(6): 357-60. DOI:10.1111/dth.2014.27.issue-6 |
| [24] |
Hira K, Yamada H, Takahashi Y, et al. Successful treatment of chromomycosis using Carbon dioxide laser associated with topical heat applications[J]. J Eur Acad Dermatol Venereol, 2002, 16(3): 273-5. DOI:10.1046/j.1468-3083.2002.00479.x |
| [25] |
Tanzi EL, Alster TS. Long-pulsed 1064-nm Nd:YAG laser-assisted hair removal in all skin types[J]. Dermatol Surg, 2004, 30(1): 13-7. |
| [26] |
孙杰, 黄海峰, 胡君, 等. 聚桂醇硬化剂联合长脉冲1064nm Nd:YAG激光治疗婴幼儿混合型血管瘤疗效观察[J]. 中国美容医学, 2015, 24(2): 40-2. |
| [27] |
Ortiz AE, Anderson RR, Digiorgio C, et al. An expanded study of long-pulsed 1064 nm Nd: YAG laser treatment of basal cell carcinoma [J]. Lasers Surg Med, 2018: doi: 10.1002/lsm.22803.[Epubaheadofprint]. https://onlinelibrary.wiley.com/doi/abs/10.1002/lsm.22803
|
| [28] |
Okan G, Tarikci N, Gokdemir G. The effect of Long-Pulsed Nd:YAG laser for the treatment of onychomycosis[J]. J Am Podiatr Med Assoc, 2017, 107(1): 54-9. DOI:10.7547/15-137 |
| [29] |
Piccolo D, Kostaki D, Del Duca E, et al. Long-Pulsed 1064-nm Nd:YAG laser for the treatment of onychomycosis[J]. Photomed Laser Surg, 2017, 35(4): 213-6. DOI:10.1089/pho.2016.4153 |
| [30] |
杨烨玫, 周思彤, 胡永轩, 等. 长脉宽1064 nm Nd:YAG激光治疗趾甲真菌病的疗效及安全性[J]. 南方医科大学学报, 2016, 36(5): 693-6. |
| [31] |
Dong B, Li D, Li R, et al. A chitin-like component on sclerotic cells of Fonsecaea pedrosoi inhibits Dectin-1-mediated murine Th17 development by masking β-glucans[J]. PLoS One, 2014, 9(12): e114113. DOI:10.1371/journal.pone.0114113 |
| [32] |
Calvo E, Javier Pastor F, Mayayo E, et al. Antifungal therapy in an athymic murine model of chromoblastomycosis by fonsecaea pedrosoi[J]. Antimicrob Agents Chemother, 2011, 55(8): 3709-13. DOI:10.1128/AAC.01662-10 |
 2019, Vol. 39
2019, Vol. 39

