2. 佛山市妇幼保健院病理科,广东 佛山 528000;
3. 南方医科大学南方医院肾内科,广东 广州 510515
2. Department of Pathology, Foshan Maternal and Child Healthcare Hospital, Foshan 528000, China;
3. Department of Nephrology, Nanfang Hospital, Southern Medical
2型糖尿病患者出现各种心血管事件的风险显著高于正常人[1-2]。目前主要用Framingham风险评分来预测患者的心血管事件发生风险,Framingham风险评分是根据Framingham心脏研究提出的一种预评估患者10年内心血管事件发生风险的方法,它主要通过患者的年龄、性别、吸烟、收缩压、总胆固醇、高密度脂蛋白及是否患糖尿病等传统因素来预测患者的心血管事件的发生[3-6]。但是,除传统危险因素以外,已证实晚期氧化蛋白产物(AOPPs)等多种新发现的物质参与了患者心血管病变的发生。AOPPs是体内次氯酸修饰白蛋白后产生的双酪氨酸蛋白交联产物,是体内氧化应激的重要标志物[7],在2型糖尿病患者循环AOPPs显著升高,且与患者的内皮功能呈显著负相关[8],在急性冠脉综合征患者循环AOPPs与冠脉病变程度呈正相关[9],提示循环AOPPs的水平可以反应患者血管病变的程度。但目前尚不清楚AOPPs的升高是否可以预测2型糖尿病患者的心血管事件发生风险升高,故我们通过分析无血管病变的2型糖尿病患者循环AOPPs与Framingham风险评分之间的关系以明确AOPPs与2型糖尿病患者心血管事件发生风险的关系。
1 资料和方法 1.1 研究对象2010年3月~2011年5月在南方医科大学附属的三所医院(南方医院、江都医院、珠江医院)共招募无血管病变的2型糖尿病患者112例,2型糖尿病诊断标准依据美国糖尿病协会的标准[10],所有患者均通过全身视诊、足背动脉触诊以及心肺听诊、心电图、心脏B超、下肢血管B超、踝肱指数等检查排除心梗、脑梗塞、周围大血管病变,通过病史、眼底镜、音叉共振、单尼龙丝触觉、欧米诺足底印迹等查体排除糖尿病视网膜病变、糖尿病周围神经病变,所有患者24 h尿微量白蛋白小于30 mg/24 h,通过全身视诊、肺部听诊、腹部触诊、血常规、hs-CRP等检查排除感染,所有患者近一月内均未使用过维生素C,维生素E等抗氧化药物;同时选择49例健康体检者为对照组。根据世界卫生组织推荐的方法测定身高、体质量、血压,计算体质量指数(BMI)=体质量/身高2(kg/m2);血压测定:安静休息10 min后取坐位,测定侧上肢与心脏齐平,之后测量血压,间隔10 min后测定第2、3次血压,测定3次血压后取平均值,计算平均动脉压=(收缩压+2舒张压)/3(mmHg)。非吸烟者定义为6个月内未有吸烟的人员。
所有入组人员均签订知情同意书。
1.2 方法 1.2.1 一般生化指标所有入组人员血肌酐、尿酸、低密度脂蛋白、高密度脂蛋白、总胆固醇、甘油三酯、24 h尿微量白蛋白均在南方医院中心实验室进行检测。
1.2.2 AOPPs测定按照Witko-Sarsat提出的标准氯胺T法测定[7],并通过低温、高速离心以减少血脂对AOPPs测定的影响[8, 11]。取EDTA抗凝血2 mL,3000 r/min、4 ℃离心5 min,取血清分装并-70 ℃保存。测定时取血浆200 μL,12 000 r/min、4 ℃离心30 min,用1mL细针注射器抽取中间层血浆,避免吸取上层油脂及下层颗粒沉渣。取10 μL血浆与90 μL磷酸缓冲盐溶液(PBS)充分混匀,然后加入10 μL冰醋酸。取90 μL(0~100 μmol/L)氯胺T溶液与10 μL (1.16 mmol/L)碘化钾混匀后再加入10 μL冰醋酸为标准品以制作标准曲线,并以100 μL PBS与10 μL冰醋酸溶液混匀为空白对照。取100 μL混合液体在340 nm分光光度计下测定吸收值,根据标准曲线计算血浆中AOPPs的浓度,以氯胺T单位表示(μmol/L)。1.2.3 Framingham风险评分依照Framingham心脏研究提供的方法,根据患者的年龄、性别、吸烟情况、收缩压、总胆固醇、高密度脂蛋白以及是否患糖尿病的情况计算患者的风险评分[4]。
1.3 统计分析应用SPSS 20.0统计软件分析数据。计量资料采用均数±标准差描述,计数资料采用率或百分比描述。两组间计量资料采用两独立样本t检验,率的比较采用Pearson χ2检验,相关性检测采用spearman相关分析,采用多元线性回归(逐步法)分析对Framingham的独立相关因素,P < 0.05为差异有统计学意义。
2 结果 2.1 正常人群与2型糖尿病患者的基本人口学指标及生化指标比较2型糖尿病患者与正常对照人群相比,两组在年龄、性别、平均动脉压、血肌酐、尿酸水平无显著差异,2型糖尿病患者的吸烟率(P < 0.001)、体质量指数(P=0.02)、低密度脂蛋白(P < 0.001)、甘油三脂(P < 0.001)、总胆固醇(P < 0.016)、血糖(P < 0.001)水平则显著高于正常人,而高密度脂蛋白(P < 0.001)则显著低于正常人群(表 1)。
| 表 1 正常人群与2型糖尿病患者的基本人口学指标及生化指标 Table 1 Characteristics of healthy controls and type 2 diabetic patients |
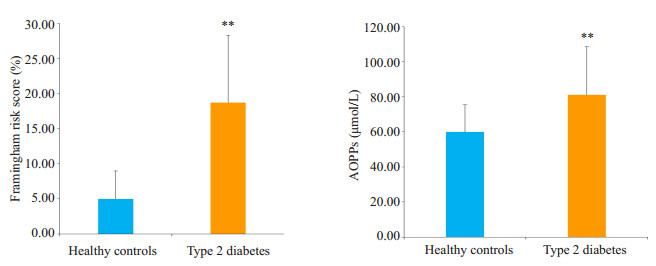
2型糖尿病患者循环AOPPs(P < 0.001)、Framingham风险评分(P < 0.001)显著高于正常人群(图 1)。
|
图 1 2型糖尿病患者及正常人群AOPPs与Framingham风险评分 Figure 1 Plasma levels of AOPPs and Framingham risk scores in type 2 diabetic patients and normal subjects (Mean±SD). **P < 0.001 vs control group |
通过Spearman单因素相关分析发现,在无血管病变的2型糖尿病患者,循环AOPPs与患者的Framingham风险评分呈显著正相关(表 2)。
| 表 2 Framingham风险评分相关因素的Spearman单因素分析结果 Table 2 Spearman univariate analysis of factors associated with Framingham risk score |
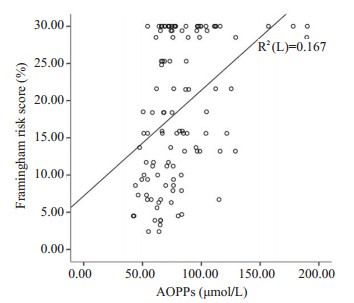
多因素回归分析结果显示在2型糖尿病患者,AOPPs仍与Framingham风险评分的独立正相关(β= 0.305,P < 0.001,图 2,表 3)。
|
图 2 AOPPs与Framingham风险评分相关性分析 Figure 2 Correlation between plasma level of AOPPs and Framingham risk score |
| 表 3 Framingham风险评分的独立相关因素多元回归分析结果 Table 3 Multivariate regression analysis of the factors that independently correlate with the Framingham risk score |
本研究结果显示,与正常人相比,在无显著血管病变的2型糖尿病患者体内,循环AOPPs显著升高,同时Framingham风险评分也显著高于正常人,多元回归分析发现,AOPPs与Framingham风险评分呈独立的正相关关系。
在本研究中发现,2型糖尿病患者Framingham风险评分较正常人显著升高,提示2型糖尿病患者10年内发生心血管疾病的风险率显著高于正常人群。目前已证实,心血管疾病是导致2型糖尿病患者病情进展及死亡的最主要原因,而传统的危险因素已不能完全解释糖尿病患者高心血管疾病的发生率[12-13]。AOPPs是一种含双酪氨酸结构的蛋白氧化产物,多项研究显示其对心血管系统具有显著的损伤作用,不仅可与内皮细胞的AGE受体(RAGE)结合导致内皮细胞凋亡,还可以刺激单核细胞趋化蛋白-1(MCP-1)等细胞因子升高而加速动脉粥样硬化的发生[14-23];前期研究也发现,在无血管病变的2型糖尿病患者循环AOPPs与内皮功能紊乱呈独立的正相关,且这种关系随着尿蛋白的增加而更加明显[8];在急性冠脉综合征患者,循环AOPPs与冠脉病变严重程度呈正相关[9],提示AOPPs不仅对血管内皮细胞有损伤作用,同时通过检测循环AOPPs还可以有效的判断患者的血管功能及血管病变情况。在我们的研究结果中也显示,即使2型糖尿病患者尚未出现任何血管病变,AOPPs已显著升高,而循环AOPPs与患者的Framingham风险评分呈显著独立的正相关关系,提示在2型糖尿病患者未发生任何血管病变之前,监测循环的AOPPs水平可能可以显示2型糖尿病患者心血管疾病发生的风险。同时由于AOPPs在体内主要与血浆白蛋白相结合,具有良好的稳定性,而且临床检测方法简便易行,具有较高的临床推广可能[24-26]。
由于本研究仅为小样本的横断面调查研究,故不能确定因果关系,接下来将进一步扩大样本量并对该组2型糖尿病患者人群进行随访,以明确AOPPs在预测2型糖尿病患者心血管疾病发生中的作用。
综上所述,在无血管病变的2型糖尿病患者AOPPs已显著升高,而且患者10年发生心血管疾病的风险较正常人显著升高,循环AOPPs与Framingham风险评分呈独立的正相关关系,提示循环AOPPs的升高可能预示着2型糖尿病患者心血管疾病发生的风险升高。
| [1] |
苏俊, 田慧, 李春霖, 等. 老年糖尿病住院患者死亡原因分析[J].
第一军医大学学报, 2004, 24(1): 110-2.
|
| [2] |
Al Rawahi AH, Lee P, Al Anqoudi ZAM, et al. Cardiovascular disease incidence and risk factor patterns among omanis with type 2 diabetes: a retrospective cohort study[J].
Oman Med J, 2017, 32(2): 106-14.
DOI: 10.5001/omj.2017.20. |
| [3] |
何斌, 盖鲁粤, 盖兢泾, 等. 冠状动脉CT与冠心病危险因素的相关分析[J].
南方医科大学学报, 2012, 32(10): 1400-6.
DOI: 10.3969/j.issn.1673-4254.2012.10.004. |
| [4] |
D'agostino RB, Vasan RS, Pencina MJ, et al. General cardiovascular risk profile for use in primary care: the framingham heart study[J].
Circulation, 2008, 117(6): 743-53.
DOI: 10.1161/CIRCULATIONAHA.107.699579. |
| [5] |
Sayin MR, Cetiner MA, Karabag T, et al. Framingham risk score and severity of coronary artery disease[J].
Herz, 2014, 39(5): 638-43.
DOI: 10.1007/s00059-013-3881-4. |
| [6] |
Goh LG, Welborn TA, Dhaliwal SS. Independent external validation of cardiovascular disease mortality in women utilising Framingham and SCORE risk models: a mortality follow- up study[J].
BMC Womens Health, 2014, 14(1): 1-11.
DOI: 10.1186/s12905-014-0155-0. |
| [7] |
Witko-Sarsat V, Friedlander M, Capeillére-Blandin C, et al. Advanced oxidation protein products as a novel marker of oxidative stress in uremia[J].
Kidney Int, 1996, 49(5): 1304-13.
DOI: 10.1038/ki.1996.186. |
| [8] |
Liang M, Wang J, Xie C, et al. Increased plasma advanced oxidation protein products is an early marker of endothelial dysfunction in type 2 diabetes patients without albuminuria[J].
J Diabetes, 2014, 6(5): 417-26.
DOI: 10.1111/jdb.2014.6.issue-5. |
| [9] |
Skvarilová M, Bulava A, Stejskal D, et al. Increased level of advanced oxidation products (AOPP) as a marker of oxidative stress in patients with acute coronary syndrome[J].
Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub, 2005, 149(1): 83-7.
DOI: 10.5507/bp.2005.009. |
| [10] |
American Diabetes Association. Diagnosis and classification of diabetes mellitus. Diabetes Care 32 (Suppl 1), S62-S67[J].
Diabetes, 2009, 33(Suppl 1): S62-9.
|
| [11] |
梁敏, 侯凡凡, 陈瑗. 化学修饰蛋白质类尿毒症毒素的检测方法与评价[J].
中华肾脏病杂志, 2003, 19(3): 62-3.
|
| [12] |
Giacco F, Brownlee M. Oxidative stress and diabetic complications[J].
Circ Res, 2010, 107(9): 1058.
DOI: 10.1161/CIRCRESAHA.110.223545. |
| [13] |
Ou H, Huang Z, Mo Z, et al. The characteristics and roles of advanced oxidation protein products in atherosclerosis[J].
Cardiovasc Toxicol, 2017, 17(1): 1-12.
DOI: 10.1007/s12012-016-9377-8. |
| [14] |
郭志坚, 侯凡凡, 刘尚喜, 等. 糖化和氧化产物修饰的蛋白质促进兔主动脉粥样斑块形成[J].
北京大学学报:医学版, 2004, 36(2): 127-30.
|
| [15] |
Marsche G, Semlitsch M, Hammer A, et al. Hypochlorite-modified albumin colocalizes with RAGE in the artery wall and promotes MCP-1 expression via the RAGE-Erk1/2 MAP-kinase pathway[J].
FASEB J, 2007, 21(4): 1145-52.
DOI: 10.1096/fj.06-7439com. |
| [16] |
Zhang Z, Yang L, Lei L, et al. Glucagon- like peptide-1 attenuates advanced oxidation protein product- mediated damage in islet microvascular endothelial cells partly through the RAGE pathway[J].
Int J Mol Med, 2016, 38(4): 1161-9.
DOI: 10.3892/ijmm.2016.2711. |
| [17] |
Guo ZJ, Niu HX, Hou FF, et al. Advanced oxidation protein products activate vascular endothelial cells via a RAGE-mediated signaling pathway[J].
Antioxid Redox Signal, 2008, 10(10): 1699-712.
DOI: 10.1089/ars.2007.1999. |
| [18] |
Peng KF, Wu XF, Zhao HW, et al. Advanced oxidation protein products induce monocyte chemoattractant protein-1 expression via p38 mitogen-activated protein kinase activation in rat vascular smooth muscle cells[J].
Chin Med J, 2006, 119(13): 1088-93.
|
| [19] |
Lin L, Zhao GJ, Qin LL. Association between advanced oxidation protein products (AOPP) and vascular calcification in uremic patients[J].
Eur Rev Med Pharmacol Sci, 2017, 21(18): 4147-52.
|
| [20] |
Marsche G, Frank S, Hrzenjak A, et al. Plasma-advanced oxidation protein products are potent high-density lipoprotein receptor antagonists in vivo[J].
Circ Res, 2009, 104(6): 750-7.
DOI: 10.1161/CIRCRESAHA.108.193169. |
| [21] |
Cao W, Hou FF, Nie J. AOPPs and the progression of kidney disease[J].
Kidney Int Suppl, 2014, 4(1): 102-6.
DOI: 10.1038/kisup.2014.19. |
| [22] |
Chawla D, Bansal S, Banerjee BD, et al. Role of advanced glycation end product (AGE)-induced receptor (RAGE) expression in diabetic vascular complications[J].
Microvasc Res, 2014, 95(1): 1-6.
|
| [23] |
杨小兵, 侯凡凡, 武强, 等. 慢性肾脏病患者晚期氧化蛋白产物血症及其与动脉粥样硬化的关系[J].
中华内科杂志, 2005, 44(5): 342-6.
|
| [24] |
Başkol M, Dolbun Seçkin K, Başkol G. Advanced oxidation protein products, total thiol levels and total oxidant/antioxidant status in patients with nash[J].
Turk J Gastroenterol, 2014, 25(Suppl 1): 32-7.
|
| [25] |
Piwowar A. The advanced oxidation protein products as potential diagnostic and prognostic factor in diseases of the indicated participation of oxidative stress[J].
Postepy Hig Med Dosw(Online), 2014, 68: 446-58.
DOI: 10.5604/17322693.1101545. |
| [26] |
Piwowar A, Knapik-Kordecka M, Warwas M. AOPP and its relations with selected markers of oxidative/antioxidative system in type 2 diabetes mellitus[J].
Diabetes Res Clin Pract, 2007, 77(2): 188-92.
DOI: 10.1016/j.diabres.2006.12.007. |
 2018, Vol. 38
2018, Vol. 38

