子宫内膜异位症是指有活性的内膜组织种植于子宫腔以外而形成的一种女性常见妇科疾病。高达30%~ 50%的EMT患者可合并不孕[1],严重影响妇女的身心健康。腹腔镜保守手术是诊断EMT的金标准,可以提高轻度盆腔EMT的妊娠率[2],术中容易残留微小病灶,术后联用激素类药物,已被证实能有效的减轻疼痛和预防复发,但这些药物无一避免的会抑制排卵,导致围绝经期的状态[3],近年较热门的促性腺激素释放激素激动剂(GnRHa)可高效抑制HPO轴,造成体内低刺激素状态,减灭微小病灶,但其是否有利于提高妊娠率,改善妊娠结局尚具有争议[4-7]。本文通过分析324例EMT合并不孕症患者,对比单纯的腹腔镜手术及术后联用GnRHa对妊娠率及妊娠结局是否有影响。
1 资料和方法 1.1 一般资料2011年1月~ 2016年12月在南方医科大学附属珠江医院妇产科行腹腔镜手术,并经病理检查证实为盆腔EMT合并不孕的患者共364例,在随访过程中失访40例,失访率10.99%(40 /364);根据术后是否联用GnRHa分为GnRHa组和单纯手术组。收集随访资料完整的324例患者的临床资料,年龄20~39岁,平均29.91岁。r-AFS分期:Ⅰ期81例(25.00%),Ⅱ期106例(32.72%),Ⅲ期71(21.91%),Ⅳ期66例(20.37%)。所有患者术前排除生殖道发育异常、免疫因素和男方精液异常等原因。
1.2 研究方法本研究为回顾性病例对照研究,建立统一数据库,详细记录所有患者的年龄、手术方式、美国生殖医学会r-AFS标准术中分期、药物治疗种类及时间、单纯手术组及联合治疗组分别术后及距离最后一次使用GnRHa6月、12月、24月、36月的累计妊娠率。对不同r-AFS分期的不同妊娠的情况进行比较。
1.3 腹腔镜手术方法所有患者均行腹腔镜手术,对有粘连者行盆腔粘连分解术,恢复盆腔解剖结构,并给予Interceed防粘连膜预防再粘连; 对合并有子宫内膜异位囊肿或者黄体囊肿者行囊肿剥除术后根据情况重建卵巢;对于合并子宫腺肌瘤者行腺肌瘤减灶术;重度EMT患者同时行直肠子宫陷凹重建;尽可能恢复其正常解剖形态及暴露双侧宫骶韧带;对输卵管行子宫输卵管通液术,必要时行输卵管修复整形术。对于术前B超提示宫腔占位者,同时行联合宫腔镜检查术,发现息肉、粘膜下肌瘤者则行子宫内膜息肉或粘膜下肌瘤电切术。
1.4 术后联合使用GnRHa的方法术后月经复潮第1~5天内返门诊注射GnRHa针剂第一针,随后每间隔28 d行下一针注射,根据子宫的大小及激素水平的结果及rAFS分期决定总剂量,3~6针不等。
1.5 统计学方法本研究中计量资料以均数±标准差表示,满足正态分布与方差齐性的采用t检验,不满足的采用校正t检验。计数资料方差齐性的采用χ2检验。P < 0.05表示差异有统计学意义。
2 结果 2.1 一般情况364例患者,失访40例,随访率88.70%。随访的324例患者中,年龄19~40岁,平均年龄29.91岁;妊娠者年龄19~40岁,平均年龄28.74岁;原发不孕共162人,继发不孕162人。随访期间妊娠患者共168人,具体妊娠率见表 1~2。
| 表 1 281例患者各期各组的自然妊娠率的对比 Table 1 Postoperative spontaneous pregnancy rates in 281 patients with endometriosis receiving different treatments |
| 表 2 单纯手术组和联合治疗组自然妊娠率和IVF妊娠率的对比 Table 2 Comparison of spontaneous pregnancy rate and pregnancy rate following IVF-ET between operation alone and GnRHa groups |
除去IVF的43人,单纯手术组共82人,联合治疗组199人,对于轻度EMT,两组妊娠率对比差异没有统计学意义(P>0.05);对于中重度EMT,两组妊娠率对比差异有统计学意义(P < 0.05,表 1)。对于单纯手术组,术后IVF妊娠率对比自然妊娠率有显著性差异;对于联合治疗组,药物治疗后的自然妊娠率和IVF妊娠率对比并无显著性差异(表 2)。
2.3 两组子宫内膜异位囊肿的妊娠情况中重度子宫内膜异位囊肿,对于单侧子宫内膜异位囊肿的,联合治疗组较单纯治疗组妊娠率的对比,有显著性提高;而对于双侧子宫内膜异位囊肿的,联合治疗组妊娠率40.91%,单纯治疗组为20.00%,但两者无统计学差异(表 3)。
| 表 3 两组合并子宫内膜异位囊肿的EMT自然妊娠率的对比 Table 3 Comparison of pregnancy rate in patients with endometriosis complicated by endometrioma between the operation group and GnRHa group |
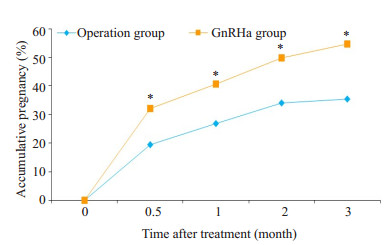
两组3年内累计妊娠率的增长图,可直观的从图中看出两个组对应任意时间点,两组妊娠率相比较,联合治疗组妊娠率都高于单纯手术组,结合卡方检验可知,差异均有统计学意义。3年内对应任意时间点,两组妊娠率相比较,联合治疗组妊娠率都高于单纯手术组,差异均有统计学意义。两组均在治疗结束后的半年内妊娠率增长幅度最大,后增长速度趋于平缓(图 1)。
|
图 1 单纯手术组和联合治疗组术后累计妊娠率的对比 Figure 1 Comparison of accumulative pregnancy rate between the operation group and GnRHa group. *P < 0.054 vs operation group |
EMT在女性中的发病率可高达11%[8],其可通过增加盆腹腔氧化应激物及生殖道胚胎毒性因子[9-11],影响输卵管活动能力及正常子宫收缩[12],而导致不孕。EMT合并不孕目前常用的治疗手段包括手术、药物(GnRHa、COC等)。
本研究单纯手术治疗组中,轻度EMT患者的妊娠率明显改善,为48.08%,重度EMT患者妊娠率稍有改善,为18.18%。该研究结果和Marcoux等[2]及Brown等[4]2014年系统综述多个研究的结果一致,也确证了手术的必要性。轻度EMT主要导致盆腔粘连及输卵管结构改变,对盆腔微环境影响较小,单纯的腹腔镜手术通过分离粘连、去除病灶、修复整形输卵管及冲洗盆腔有助于提高妊娠率。但对于重度EMT者,其单纯手术后妊娠率较低的原因可能与盆腔生理结构及内微环境改变严重,不利于精卵的生存发育及输送有关。另外,重度EMT者卵巢病灶较大且深,行腹腔镜剥除囊肿会不可避免的损伤正常卵巢组织,因此,子宫内膜异位囊肿与不孕症的关系一直备受争议,需权衡是子宫内膜异位囊肿本身及手术处理囊肿影响卵巢储备功能,两者对妊娠的影响更大[13]。EMT患者合并子宫内膜异位囊肿的占20%~40%[14]。本研究中,术中发现双侧子宫内膜异位囊肿的41人,单侧子宫内膜异位囊肿的98人,共139人,发病率为42.90%。其中,轻度内异症的合并子宫内膜异位占总体的5.25%;重度内异症合并巧囊的占总体的37.65%。该类患者行子宫内膜异位囊肿剥除术后71人妊娠,自然妊娠率为46.40%,IVF妊娠率高达92.86%,提示子宫内膜异位囊肿剥除术可能更有利于妊娠。但Hamdan等[15]Meta分析发现手术治疗子宫内膜异位囊肿并不能改善IVF/ICSI的妊娠结局。最新的研究显示,子宫内膜异位囊肿囊液中存在蛋白水解酶、炎症因子等介导细胞损伤的介质,且较普通囊肿囊液高出成百上千倍,对卵巢功能极为不利[16]。结合Benaglia和Harada的研究[17-18]可以推测去除卵巢上的内异症病灶,虽然不可避免会造成部分正常卵巢组织的流失,但卵巢经修复后可不影响其卵子质量,最终,虽术后取卵数下降,但卵子质量高仍可保障IVF的成功率。综上,建议有生育要求的不孕女性,需个体化评估,若卵巢储备功能尚可,由经验丰富的医生剥除卵巢子宫内膜异位囊肿,可尽早终止异位内膜对卵巢的免疫性炎症破坏,有利于保护卵巢储备功能,对提高自然妊娠率有一定的帮助。
除了腹腔镜手术,近年来研究热门的还有GnRHa,但对于术后应用GnRHa治疗是否可以提高妊娠率一直存在争议。既往有研究认为术后联用GnRHa可以提高轻度EMT患者的妊娠率[19],但对于提高重度EMT者妊娠率影响不大[20];甚至有研究[3]提出术后联用药物并不能提高生育力。本研究发现对轻度EMT患者术后应用GnRHa治疗对妊娠率并无明显的帮助,但对中重度EMT者术后应用GnRHa治疗,自然妊娠率(49.44%)明显升高,且稍高于轻度EMT者术后的自然妊娠率(48.08%)。和黄意娟等[21]的研究结果一致。对于合并卵巢子宫内膜异位囊肿的中重度EMT者,本研究结果显示,联合治疗可显著提高妊娠率,也佐证了GnRHa对提高中重度EMT患者妊娠率的重要作用。既往较一致的观点认为,中重度EMT术后应用GnRHa治疗可通过假绝经疗法,抑制盆腔炎症反应、新生血管生成,促进细胞凋亡等促使残余的子宫内膜异位病灶萎缩而改善盆腔环境[5, 22]。而近年来的新观点认为,EMT的发生可能与干细胞有关[23],且EMT患者腹腔内由于氧化应激形成了广泛的炎症反应,进而卵子质量下降导致不孕[6-7, 9, 24]。而GnRHa除了可以通过激素抑制方面有利于妊娠,同时还可以通过抑制EMT病灶中干细胞的种植而较长期的抑制病灶的复发及改善腹腔的炎性环境而提高妊娠率[25-26]。
术后因各种原因,如年龄>35岁,试孕1年失败者后选择行IVF者,单纯手术组的IVF妊娠率(87.50%)率较自然妊娠率(37.80%)显著提高,证明IVF能明显增加妊娠率;而联合治疗组,IVF妊娠率(74.07%)率较自然妊娠率(56.28%)有提高,但无统计学意义。这就指导我们在腹腔镜保守治疗术后,若积极试孕仍不成功,需及早行IVF。这同Vercellini等[27]研究结果一致,虽输卵管机械性通畅,仍可因微小的内异病灶而存在功能上的损上,而IVF可使EMT患者避免输卵管因素及可以挑选优质的受精卵而显著提高妊娠率,尤其是中重度患者。
本研究还发现术后或距离最后一次GnRHa注射的半年内,两组妊娠率增长速度明显,2年内累计妊娠率占了术后自然妊娠率的绝大部分。这可能与术后以及用药半年内盆腔环境得到最大的改善,有利于妊娠,而随着时间得推移,病灶复发而再次影响盆腔环境。本研究中,合并卵巢子宫内膜异位囊肿的患者,在随访时间内未妊娠的68人中,囊肿复发的8人,复发率为11.76%,皆为中重度EMT,其中最短时间距离为6个月,最长时间为4年,其中4人已再次行保守治疗术。而Wheeler等在1983年发表的第一个对照性研究[28]发现子宫内膜异位症单纯手术后,3年的复发率为13.6%,5年的复发率为40.3%;对于重度内异症患者尤甚,术后5年,Ⅰ~Ⅱ累计复发率为22%,而Ⅲ~Ⅳ期患者为33~50%。这就提醒患者术后或GnRHa治疗后半年内积极备孕,若两年内尚未能自然妊娠,考虑到自然妊娠的几率低,且随着年龄的增长,卵巢功能下降,子宫内膜异位囊肿复发率高,就得权衡利弊,若年纪较大者需密切评估卵巢功能,若提示功能较差,则应更早地转向ART。
本研究存在的不足为样本量不足够大,可能存在选择偏倚;另为回顾性分析,回访数据可能因患者的不配合存在及记忆失真或不完整存在信息偏倚;未来可通过多中心、大样本的前瞻性研究得出更为可靠的结论。
| [1] |
Sensky TE, Liu DT. Endometriosis: associations with menorrhagia, infertility and oral contraceptives[J].
Int J Gynaecol Obstet, 1980, 17(6): 573-6.
DOI: 10.1002/j.1879-3479.1980.tb00210.x. |
| [2] |
Marcoux S, Maheux R, Bérubé S. Laparoscopic surgery in infertile women with minimal or mild endometriosis[J].
N Engl J Med, 1997, 337(4): 217-22.
DOI: 10.1056/NEJM199707243370401. |
| [3] |
Streuli I, De Ziegler D, Santulli P, et al. An update on the pharmacological management of endometriosis[J].
Expert Opin Pharmacother, 2013, 14(3): 291-305.
DOI: 10.1517/14656566.2013.767334. |
| [4] |
Brown J, Farquhar C. Endometriosis: an overview of Cochrane Reviews[J].
Cochrane Database of Systematic Reviews, 2014, 10(3): D9590.
|
| [5] |
Khan KN, Kitajima M, Hiraki K, et al. Cell proliferation effect of GnRH agonist on pathological lesions of women with endometriosis, adenomyosis and uterine myoma[J].
Hum Reprod, 2010, 25(11): 2878-90.
DOI: 10.1093/humrep/deq240. |
| [6] |
Christodoulakos G, Augoulea A, Lambrinoudaki I, et al. Pathogenesis of endometriosis: the role of defective 'immunosurveillance'[J].
Eur J Contracept Reprod Health Care, 2007, 12(3): 194-202.
DOI: 10.1080/13625180701387266. |
| [7] |
Augoulea A, Mastorakos G, Lambrinoudaki I, et al. The role of the oxidative-stress in the endometriosis-related infertility[J].
Gynecol Endocrinol, 2009, 25(2): 75-81.
DOI: 10.1080/09513590802485012. |
| [8] |
Buck Louis GM, Hediger ML, Peterson CM, et al. Incidence of endometriosis by study population and diagnostic method: the ENDO study[J].
Fertil Steril, 2011, 96(2): 360-5.
DOI: 10.1016/j.fertnstert.2011.05.087. |
| [9] |
Scutiero G, Iannone P, Bernardi G, et al. Oxidative stress and endometriosis: a systematic review of the literature[J].
Oxid Med Cell Longev, 2017, 2017: 7265238.
|
| [10] |
Malvezzi H, Da Broi MG, Meola J, et al. Peritoneal fluid of women with endometriosis reduces SOD1 in bovine oocytes in vitro maturation[J].
Cell Tissue Res, 2018.
|
| [11] |
Robertson SA, Chin PY, Femia JG, et al. Embryotoxic cytokinesPotential roles in embryo loss and fetal programming[J].
J Reprod Immunol, 2018, 125: 80-8.
DOI: 10.1016/j.jri.2017.12.003. |
| [12] |
Pinto V, Matteo M, Tinelli R, et al. Altered uterine contractility in women with chronic endometritis[J].
Fertil Steril, 2015, 103(4): 1049-52.
DOI: 10.1016/j.fertnstert.2015.01.007. |
| [13] |
Leone Roberti Maggiore U, Gupta J K, Ferrero S. Treatment of endometrioma for improving fertility[J].
Eur J Obstet Gynecol Reprod Biol, 2017, 209: 81-5.
DOI: 10.1016/j.ejogrb.2016.02.035. |
| [14] |
Vercellini P, Chapron C, De Giorgi O, et al. Coagulation or excision of ovarian endometriomas?[J].
Am J Obstet Gynecol, 2003, 188(3): 606-10.
DOI: 10.1067/mob.2003.7. |
| [15] |
Hamdan M, Dunselman G, Li TC, et al. The impact of endometrioma on IVF/ICSI outcomes: a systematic review and meta-analysis[J].
Hum Reprod Update, 2015, 21(6): 809-25.
DOI: 10.1093/humupd/dmv035. |
| [16] |
anchez AM, Vigano P, Somigliana E, et al. The distinguishing cellular and molecular features of the endometriotic ovarian cyst: from pathophysiology to the potential endometrioma-mediated damage to the ovary[J].
Hum Reprod Update, 2014, 20(2): 217-30.
DOI: 10.1093/humupd/dmt053. |
| [17] |
Benaglia L, Bermejo A, Somigliana E, et al. In vitro fertilization outcome in women with unoperated bilateral endometriomas[J].
Fertil Steril, 2013, 99(6): 1714-9.
DOI: 10.1016/j.fertnstert.2013.01.110. |
| [18] |
Harada M, Takahashi N, Hirata T, et al. Laparoscopic excision of ovarian endometrioma does not exert a qualitative effect on ovarian function:insights from in vitro fertilization and single embryo transfer cycles[J].
JAssist Reprod Genet, 2015, 32(5): 685-9.
DOI: 10.1007/s10815-015-0457-7. |
| [19] |
皮洁, 洛若愚, 贾胜楠, 等. 不同药物治疗腹腔镜术后子宫内膜异位合并不孕的效果观察[J].
中国妇幼保健, 2016, 31(3): 639-41.
|
| [20] |
胡晓军, 刘玉玲, 党群. 重度子宫内膜异位症腹腔镜术后应用GnRHa及反向添加疗法的临床效果[J].
实用医学杂志, 2014, 30(4): 557-60.
|
| [21] |
黄意娟, 张月红, 叶赛芳. 腹腔镜术后联合GnRHa治疗卵巢巧克力囊肿的临床疗效及其对卵巢功能的影响[J].
中国妇幼保健, 2012, 27(18): 2871-3.
|
| [22] |
Khan KN, Kitajima M, Hiraki K, et al. Changes in tissue inflammation, angiogenesis and apoptosis in endometriosis, adenomyosis and uterine myoma after GnRH agonist therapy[J].
Hum Reprod, 2010, 25(3): 642-53.
DOI: 10.1093/humrep/dep437. |
| [23] |
Gargett CE, Schwab KE, Deane JA. Endometrial stem/progenitor cells: the first 10 years[J].
Hum Reprod Update, 2016, 22(2): 137-63.
|
| [24] |
Miller JE, Ahn SH, Monsanto SP, et al. Implications of immune dysfunction on endometriosis associated infertility[J].
Oncotarget, 2017, 8(4): 7138-47.
|
| [25] |
Ersoy GS, Zolbin MM, Cosar E, et al. Medical therapies for endometriosis differentially inhibit stem cell recruitment[J].
Reprod Sci, 2017, 24(6): 818-23.
DOI: 10.1177/1933719116682879. |
| [26] |
Imamura T, Khan KN, Fujishita A, et al. Effect of GnRH agonist therapy on the expression of human heat shock protein 70 in eutopic and ectopic endometria of women with endometriosis[J].
Eur J Obstet Gynecol Reprod Biol, 2014, 180: 16-23.
DOI: 10.1016/j.ejogrb.2014.06.002. |
| [27] |
Vercellini P, Vigano P, Somigliana E, et al. Endometriosis: pathogenesis and treatment[J].
Nat Rev Endocrinol, 2014, 10(5): 261-75.
DOI: 10.1038/nrendo.2013.255. |
| [28] |
Wheeler JM, Malinak LR. Recurrent endometriosis: incidence, management, and prognosis[J].
Am J Obstet Gynecol, 1983, 146(3): 247-53.
DOI: 10.1016/0002-9378(83)90744-5. |
 2018, Vol. 38
2018, Vol. 38

