2. 西安交通大学医学院附属西安市中心医院 放射科,陕西 西安 710003;
3. 延安大学医学院,陕西 延安 716000
2. Department of Radiology, Xi'an Central Hospital Affiliated to Xi'an Jiaotong University College of Medicine, Xi'an 710003, China;
3. Medical College of Yan'an University, Yan'an 716000, China
帕金森病(PD)是神经系统第2大退行性疾病,随着年龄的增长发病率随之增加[1]。目前,PD主要通过临床医生依据患者的起病年龄、缓慢进展性病程、特征性临床症状和左旋多巴治疗敏感性等作出临床诊断,缺少有效的辅助检查方法。PD的病程进展呈多样化其发展趋势也很难预测。学者们认为迫切需要探索PD的敏感生物学标记[2]。影像学生物标记物在帕金森病的诊断及病程监测当中所起的作用越来越重要[3]。目前可用正电子发射断层摄影术和单光子发射计算机断层扫描对PD患者进行诊断及病情评估。但常因其昂贵的检查费用、需要有创性注射放射性核素作为示踪剂、肾功能衰竭者禁忌等而在一定程度上限制了临床应用。动脉自旋标记技术(ASL)是由Detre等[4]首先提出的脑灌注的影像技术,可定量获得全脑平均脑血流量(mCBF),广泛应用在临床及科研中[5]。但在发现局部脑血流量(rCBF)方面存在不足。随着后处理软件的不断开发,发现基于体素分析(VBA)可以准确识别rCBF改变特征。目前,应用VBA的ASL技术在痴呆等疾病的诊断中发挥着重要作用[6],但其在PD中的研究较少。Albachari等[7]应用VBA发现右侧顶上回接近角回区域血流灌注减低。但其未对PD患者进行分组研究。Lin等[8-9]的研究则主要关注左旋多巴药物对血流灌注的影响。而本研究采用VBA的ASL技术探究不同分期PD患者rCBF特征,试图寻找PD早期诊断和病情评估的影像学生物标记。
1 资料和方法 1.1 研究对象收集2014年7月~2017年5月西安交通大学医学院附属西安市中心医院神经内科门诊或住院部符合入选条件并自愿参加该项研究的受试者为本课题的研究对象。纳入标准:(1)入组的PD患者经2位高年资临床医生诊断,诊断均符合1992年英国帕金森病协会脑库临床诊断标准以及2016年制定的中国帕金森病的诊断标准[10],并行简易精神状态检查(MMSE)[11],总分>28分者判断为无认知功能障碍和痴呆者;(2)患者既往无其它神经系统疾病和精神病,如脑血管疾病史(短暂性脑缺血发作、脑卒中、脑出血者)、痴呆、癫痫、抑郁、精神分裂症等;(3)无MRI检查禁忌,同意行头颅MRI及ASL检查者,并签署知情同意书;(4)常规头颅MRI检查无异常发现。最终收集23例PD患者和13例正常对照,其中23例PD患者根据临床症状的严重程度,按照H-Y分级分为早期和中晚期。早期PD组13例,男7例,女6例,年龄61.92±9.21岁;中晚期PD组10例,男5例,女5例,年龄66.20±10.22岁;健康对照组13例,男7例,女6例,年龄62.31±8.10岁。
1.2 方法 1.2.1 仪器设备所有受试者采用GE 1.5T双梯度超导型MRI设备,使用标准8通道相控阵头线圈进行图像采集,头部用软垫固定检查者头部以减少头动影响,要求在检查时放松睁眼并保持清醒和静止。PD患者在正常服药的状态下,在“开期”进行检查以减少头动的影响。
1.2.2 扫描序列所有的受检者均接受常规MRI扫描,包括3DT1、T2WI序列及弥散加权成像序列,以排除其他器质性病变。3D T1加权像通过矢状位3DT1快速扰相梯度回波序列获得,有以下参数:视野=240 mm×240 mm,矩阵=256×256,重复时间=9.0 s,回波时间=2.9 ms,翻转角=20°,层厚=1.2 mm,层间距=0 mm,总共获取覆盖全脑128层矢状位图像。3D CASL(CASL)的参数如下:视野=24 cm,带宽=62.5 kHz/pixel,翻转角=90°,重复时间=4.5 s,回波时间=9.8 ms,层厚=4 mm,层间距= 0 mm,标记时间=1.6 s,延迟标记时间=1525 ms,每一检查者获得72幅标签/对照图像。
1.2.3 图像后处理和数据分析采用Matlab R2010b(Mathwors,MA,USA)及统计学参数图分析软件8软件包进行数据处理,具体步骤[12]:对获得的3DT1和3D CASL图像进行离线后处理,离线后的图像应用MRIcro(http://www.cabiatl.com/mricro)进行图像格式的转换,所用的MRI扫描获得的DICOM图像均转换为NIFTI格式;之后进行图像预处理,包括头动矫正、结构像和功能像的配准以及平滑处理以减少噪声的影响;预处理之后的图像应用动脉自旋标记灌注磁共振成像信号处理工具包ASLtbx(http://www.cfn.upenn.edu)进行平均脑血流量的计算,以获得每位受检者的全脑平均CBF值并获得原始灌注图像;再采用SPM将3D TI图像按照蒙特利尔神经研究所(MNI)提出的加拿大蒙特利尔神经研究所标准脑空间进行分割,分割后3D T1图像与原始灌注图像进行配准,使其配准到MNI标准脑空间,标准化的图像进行平滑采样,使用8 mm半高全宽的平滑核进行高斯平滑。然后应用SPM8软件包对上述步骤得到的灌注图像进行组水平分析,采用基于体素分析的方差分析,统计参数图的结果采用未校正的P < 0.001为显著性差异,像素数目阈值设为5,得到试验设计的组效果图;最后应用xjview8.4(http://www.alivelearn.net/xjview8/)提取脑灌注改变区的解剖部位及MNI空间坐标值、体素数、t值及未校正P值。
1.3 统计学分析应用SPSS 19.0统计分析软件对数据进行统计学分析,检验水准取双侧P=0.05。对病例的一般情况采用统计描述,确定各参数的均数及标准差,以均数±标准差表示。对3组间的年龄和MMSE评分进行方差分析,P < 0.05为差异有统计学意义。性别采用组间χ2检验,P < 0.05为差异有统计学意义。对早期PD和中晚期PD的H-Y分级、UPDRS Ⅲ进行双样本t检验,P < 0.05为差异有统计学意义。
2 结果 2.1 临床资料对比早期、中晚期PD与正常对照组的一般临床资料比较,3组在性别、年龄、受教育年限和MMSE差异均无统计学意义(P>0.05,表 1)。早期PD和中晚期PD组的病程、H-Y分级和UPDR-Ⅲ差异具有统计学意义(P < 0.05,表 1)。
| 表 1 早期、中晚期PD组与正常对照组的一般临床资料比较 Table 1 Comparison of general clinical data among patients with early-stage and advanced PD and normal control subjects |
| 表 2 早期PD组较正常对照组rCBF减低区 Table 2 Decreased rCBF in early-stage PD patients in comparison with normal control group |
正常对照组、早期和中晚期PD组的mCBF分别是53.74±2.17、54.99±2.13、53.48±3.96 mL/100(g·min)。方差分析结果显示F=1.27,P=0.30,故3者之间的mCBF差异无统计学意义。
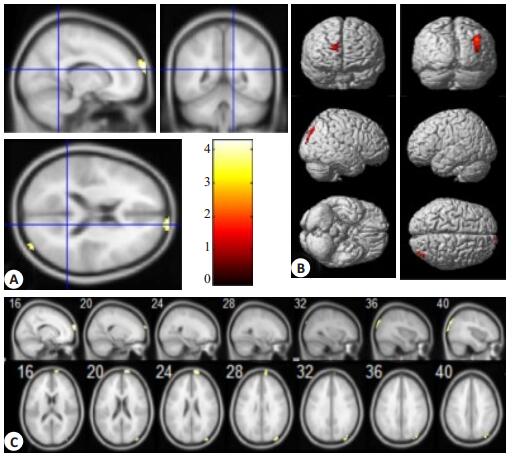
2.3 早期PD组rCBF改变特征与正常对照相比,早期PD组的rCBF减低区主要分布于右侧枕上回和右侧额上回(图 1)。
|
图 1 rCBF减低在三视图、三维投射图和T1模板图 Figure 1 Statistical parametric map showing decreased rCBF in the right superior occipital gyrus and the right superior frontal gyrus on triple-view (A), 3D projection (B) and T1 template map (C). |
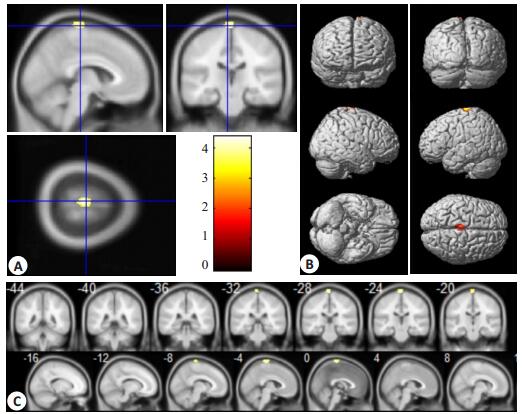
与正常对照相比,中晚期PD组的rCBF减低区主要分布于左侧中央前回、左侧中央后回(表 3,图 2)。
| 表 3 中晚期PD组较正常对照组rCBF减低区 Table 3 Decreased rCBF in advanced PD group in comparison with normal control group |
|
图 2 rCBF减低在三视图、三维投射图和T1模板图 Figure 2 Statistical parametric map showing decreased rCBF in the left precentral gyrus and the left postcentral gyrus on triple-view (A), 3D projection (B) and T1 template map (C). |
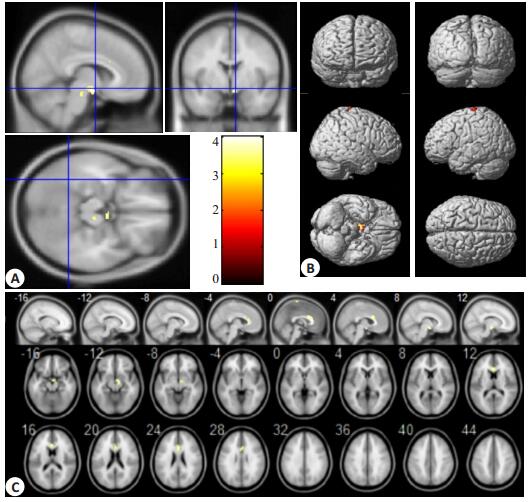
与早期PD组相比,中晚期PD组不仅表现为左侧中央前回、中央后回rCBF减低,且出现双侧胼胝体和右侧中脑黑质rCBF减低(表 4,图 3)。
| 表 4 中晚期PD组较早期PD组rCBF减低区 Table 4 Decreased rCBF in advanced PD group in comparison with early-stage PD group |
|
图 3 rCBF减低在三视图、三维投射图和T1模板图 Figure 3 Statistical parametric map showing the decreased rCBF in the left precentral gyrus, left postcentral gyrus, bilateral corpus callosum and right midbrain substantia nigra on triple-view (A), 3D projection (B) and T1 template map (C). |
本研究应用VBA方法对ASL所获数据进行处理后发现早期PD组rCBF减低区主要分布于右侧额上回和右侧枕上回;中晚期PD组的rCBF减低区主要分布于左侧中央前回、左侧中央后回。提示PD早期rCBF已发生了改变,且随着疾病的进展,rCBF也在不断发生变化。
本研究应用ASL技术发现,不同病程的PD患者和正常对照之间全脑mCBF差异无统计学意义,这与多数研究基本一致。有学者应用ASL技术对正常对照组、PD组和PD痴呆组的全脑mCBF进行评估,发现3组之间无明显差异,且多巴胺能药物不影响3组的全脑mCBF [8]。另有研究同样发现PD患者和正常对照组全脑mCBF未见明显异常[13]。
PD早期就存在不同神经系统对应的皮层下结构变性,涉及多巴胺能、胆碱能、去甲肾上腺素能和色氨酸能神经网络,因此可以观察到广泛的皮层下低灌注[8]。有研究同样证实了PD皮层低灌注区域涉及范围之广[9]。PD患者表现为广泛皮层低灌注,甚至是在疾病的早期阶段。本研究发现,静息状态下与正常对照相比,早期PD组的脑血流灌注减低区主要分布于右侧枕上回和右侧额上回(Brodmann分区9区)[14]。这与Melzer等[15]的研究发现灌注减低的区域主要在顶部的枕叶皮层、楔叶、和额中回(Brodmann分区8、9区)基本一致。且这些区域被证实与认知下降有关[16-19]。Wei等[20]联合DTI和ASL测得的双侧黑质FA值、双侧前额皮层脑血流量和双侧顶叶白质FA值这些神经影像变量可能是早期诊断PD相对的精确诊断模式。本研究提示在PD早期就可能存在认知功能减退,应进一步行与认知相关的精神心理量表及其他相关检查。二者结合起来将有助于PD的早期诊断。
本研究同时发现,静息状态下与正常对照相比,中晚期PD组的脑血流灌注减低区主要分布于左侧中央前回、左侧中央后回。与Madhyastha等[21]的研究发现左侧中央前回灌注减低一致,但Madhyastha等未发现中央后回灌注减低,这可能由于患者起病的主要症状以及病程的不同导致。
根据Braak病理模式,α-突触核蛋白沉积在特定脑区和神经类型内,产生特定的病理改变,其时间模式是从低位脑干至中脑的易感区域再至前脑和大脑皮质[22]。本研究显示早期PD患者枕上回和额上回的低灌注,这与Braak病理分期Ⅴ期出现高级感觉相关皮层病理改变部位相同;同时,发现中晚期PD患者其低灌注区域在中央前回、中央后回,这与Braak病理分期第Ⅵ期出现初级感觉和运动皮层病理改变的部位相同[23]。因此,本研究发现的早期和中晚期PD低灌注区域遵循Braak病理模式,提示ASL可能为识别PD灌注异常区域较为可靠生物学标记。
本研究中,静息态下与早期PD组相比,中晚期PD组不仅表现为左侧中央前回、中央后回大脑皮层的灌注减低,且右侧中脑黑质、皮层下胼胝体也表现为低灌注。这可能为中晚期患者运动症状进一步加重,并且出现非运动症状的影像学标记。黑质多巴胺神经递质缺乏引起PD运动症状[25],随着PD运动症状的逐渐加重,黑质多巴胺能神经元的丢失越来越严重[26]。因此黑质低灌注可能为中晚期PD患者运动症状加重的影像学生物标记。而胼胝体主要功能是整合和传递双侧大脑半球的信息,处理感觉、运动和高级认知信号[24],也有研究证实胼胝体或胼胝体的皮层连接与PD非运动症状认知损害有关[27],主要出现在Braak病理分期5、6期[28]。另外,2016年中国PD指南也提出5年内仍不出现任何一种常见的非运动症状,作为诊断PD的警示征象[10],因此胼胝体低灌注可能为中晚期PD患者非运动症状的影像学生物标记。表明应用VBA的ASL技术有可能为监测PD进展提供一种新的影像学指标。
综上所述,应用VBA的ASL技术发现PD患者与正常对照相比rCBF发生变化,并且中晚期与早期患者相比rCBF也有不同,提示此技术是监测PD患者CBF动态变化的有效方法,能够为找寻PD早期诊断和病程追踪的影像学生物标记提供帮助, 但仍需要大样本研究进一步证实。
| [1] | Postuma RB, Berg D, Stern M, et al. MDS clinical diagnostic criteria for Parkinson's disease[J]. Mov Disord, 2015, 30(12): 1591-601. DOI: 10.1002/mds.26424. |
| [2] | Jones R. Biomarkers: casting the net wide[J]. Nature, 2010, 466(7310): 11-2. |
| [3] | Pyatigorskaya N, Gallea C, Garcia-Lorenzo DA, et al. A review of the use of magnetic resonance imaging in Parkinson's disease[J]. Ther Adv Neurol Disord, 2014, 7(4): 12-26. |
| [4] | Detre JA, Leigh JS, Williams DS, et al. Perfusion imaging[J]. Magn Reson Med, 1992, 23(1): 37-45. DOI: 10.1002/(ISSN)1522-2594. |
| [5] | 中华医学会放射学分会质量管理与安全管理学组中华医学会放射学分会磁共振学组. 动脉自旋标记脑灌注MRI技术规范化应用专家共识[J]. 中华放射学杂志, 2016, 50(11): 817-24. DOI: 10.3760/cma.j.issn.1005-1201.2016.11.003. |
| [6] | Sierra-Marcos A. Regional cerebral blood flow in mild cognitive impairment and alzheimer's disease measured with arterial spin labeling magnetic resonance imaging[J]. Int J Alzheimers Dis, 2017, 7(3): 5479597. |
| [7] | Albachari S, Parkes LM, Vidyasagar R, et al. Arterial spin labelling reveals prolonged arterial arrival time in idiopathic Parkinson's disease[J]. Neuroimage Clin, 2014, 6(3): 1-8. |
| [8] | Lin WC, Chen PC, Huang YC, et al. Dopaminergic therapy modulates cortical perfusion in parkinson disease with and without dementia according to arterial spin labeled perfusion magnetic resonance imaging[J]. Medicine, 2016, 95(5): e2206. DOI: 10.1097/MD.0000000000002206. |
| [9] | Lin WC, Chen PC, Huang CC, et al. Autonomic function impairment and brain perfusion deficit in parkinson's disease[J]. Front Neurol, 2017, 8(8): 246. |
| [10] | 中华医学会神经病学分会帕金森病及运动障碍学组. 中国帕金森病的诊断标准[J]. 中华神经科杂志, 2016, 49(4): 268-71. |
| [11] | Folstein MF, Folstein SE, McHugh PR. A practical method for grading the cognitive state of patients for the clinician[J]. J Psychiatr Res, 1975, 12(3): 189-98. DOI: 10.1016/0022-3956(75)90026-6. |
| [12] | Wang Z, Aguirre GK, Rao H, et al. Empirical optimization of ASL data analysis using an ASL data processing toolbox: ASLtbx[J]. Magn Reson Imaging, 2008, 26(2): 261-9. DOI: 10.1016/j.mri.2007.07.003. |
| [13] | Al-Bachari S, Vidyasagar R, Emsley HC. Structural and physiological neurovascular changes in idiopathic Parkinson's disease and its clinical phenotypes[J]. J Cereb Blood Flow Metab, 2017, 37(10): 3409-21. DOI: 10.1177/0271678X16688919. |
| [14] | Borghammer P, Chakravarty M, Jonsdottir KY, et al. Cortical hypometabolism and hypoperfusion in Parkinson's disease is extensive: probably even at early disease stages[J]. Brain Struct Funct, 2010, 214(4): 303-17. DOI: 10.1007/s00429-010-0246-0. |
| [15] | Melzer TR, Watts R, Macaskill MR, et al. Arterial spin labelling reveals an abnormal cerebral perfusion pattern in Parkinson's disease[J]. Brain, 2011, 134(3): 845-55. DOI: 10.1093/brain/awq377. |
| [16] | Kasama S, Tachibana H, Kawabata K, et al. Cerebral blood flow in Parkinson's disease, dementia with Lewy bodies, and Alzheimer's disease according to three-dimensional stereotactic surface projection imaging[J]. Dement Geriatr Cogn Disord, 2005, 19(5/6): 266-75. |
| [17] | Nobili F, Abbruzzese G, Morbelli S, et al. Amnestic mild cognitive impairment in Parkinson's disease: a brain perfusion SPECT study[J]. Mov Disord, 2009, 24(3): 414-21. DOI: 10.1002/mds.22381. |
| [18] | Syrimi ZJ, Vojtisek L, Eliasova I, et al. Arterial spin labelling detects posterior cortical hypoperfusion in non-demented patients with Parkinson's disease[J]. J Neural Transm, 2017, 124(5): 1-7. |
| [19] | Verclytte S, Lopes R, Lenfant P, et al. Cerebral hypoperfusion and hypometabolism detected by arterial spin labeling MRI and FDGPET in early-onset alzheimer's disease[J]. J Neuroimaging, 2016, 26(2): 207-12. DOI: 10.1111/jon.2016.26.issue-2. |
| [20] | Wei X, Yan R, Chen Z, et al. Combined diffusion tensor imaging and arterial spin labeling as markers of early parkinson's disease[J]. Sci Rep, 2016, 20(6): 33762. |
| [21] | Madhyastha TM, Askren MK, Boord P, et al. Cerebral perfusion and cortical thickness indicate cortical involvement in mild parkinson's disease[J]. Mov Disord, 2015, 30(14): 1893-900. DOI: 10.1002/mds.26128. |
| [22] | Braak H, Del Tredici K, Rüb U, et al. Staging of brain pathology related to sporadic Parkinson's disease[J]. Neurobiol Aging, 2002, 24(2): 197-211. |
| [23] | Braak H, Ghebremedhin E, Rub U, et al. Stages in the development of Parkinson's disease-related pathology[J]. Cell Tissue Res, 2004, 318(1): 121-34. DOI: 10.1007/s00441-004-0956-9. |
| [24] | Andrea. Neuroanatomy, corpus callosum[M]. Treasure Island (FL): StatPearls Publishing, 2017. |
| [25] | Kalia LV. Biomarkers for cognitive dysfunction in Parkinson's disease[J]. Parkinsonism Relat Disord, 2018, 46(Suppl 1): S19-S23. |
| [26] | Lin JG, Chen CJ, Yang HB, et al. Electroacupuncture promotes recovery of motor function and reduces dopaminergic neuron degeneration in rodent models of parkinson's disease[J]. Int J Mol Sci, 2017, 18(9): E1846. DOI: 10.3390/ijms18091846. |
| [27] | Wiltshire K, Concha L, Gee M, et al. Corpus callosum and cingulum tractography in Parkinson's disease[J]. Can J Neurol Sci, 2010, 37(5): 595-600. DOI: 10.1017/S0317167100010751. |
| [28] | O'callaghan C, Lewis JG. Cognition in parkinson's disease[J]. Int Rev Neurobiol, 2017, 133(4): 557-83. |
 2018, Vol. 38
2018, Vol. 38

