眼眶脂肪体积增大是导致甲状腺相关性眼病(TAO)患者眼球突出、眼睑闭合不全等最主要的原因[1]。眼眶内软组织包括眼外肌、脂肪、泪腺等,其中眼眶脂肪体积占比重最大。临床方面,Nishida等[2]发现在TAO患者中,眼眶脂肪组织容积的增加明显高于眼外肌容积的增加,并且眼眶脂肪组织容积与突眼度的相关系数(r=0.70,P=0.0006)也高于眼外肌容积与突眼度的相关系数(r=0.58,P=0.008)。TAO后期的眼眶减压术,也是基于眼眶后脂肪剔除[3]。基础研究方面,目前已公认共同抗原学说,相关研究也表明疾病炎症活动期主要为淋巴细胞浸润成纤维细胞,可能由于甲状腺及眼眶软组织受TRAb攻击所致,而成纤维细胞在某些因素影响下会发生发展为成脂肪细胞[4-5]。因此,眼眶脂肪体积的定量测量日益受到重视。
测量眼眶脂肪体积的金标准无疑是眼眶脂肪活检,但临床难以实现,因此目前测量眼眶脂肪体积的方法主要建立于影像学基础,包括B超[6]、CT [7-11]、MRI [12-15]。获取图像后,既往研究许多都是利用三维重建技术来进行测量眼眶脂肪体积[9],这就要求影像学图像层厚薄,造成扫描时间延长、价格昂贵、重建耗时久,故临床难以推广。此外,CT扫描本身具有放射性,患者依从性差[16];其次,CT对眼眶后软组织分辨率远不及MRI [17]。MRI图像,尤其是T1WI成像,能够对眶内眼外肌、脂肪、视神经等精细显像,并且可以测量突眼度、观察视神经轴变化,为临床提供客观有效的数据[18-19]。因此,我们建立了一种新的基于MRI图像对眼眶脂肪体积进行测量的方法,半自动化的处理图像模式,使得其具有简单、快速的特点,非常便于临床推广使用。
这种新方法主要通过Adobe® Photoshop CC 2015软件[20]对MRI单层图像进行分析处理,从而测出MRI单层图像眼眶脂肪部分的面积,随后通过近柱体模型对单层面积进行叠加计算,最后计算出眼眶脂肪体积。
1 材料和方法 1.1 人体眼眶MRI图像数据的获取采用荷兰飞利浦公司医用磁共振成像设备ACHIEVA 1.5T,对10名按照Bartley[21]标准诊断的TAO患者进行扫描,TAO患者取仰卧位,采用标准头颅八通道相控阵线圈,头部置于线圈内,尽可能左右对称,调整颅脑的正中矢状位使其与线圈的纵轴一致。进行患者眼眶的横断、冠状及平行视神经的斜矢状位扫描,横断位扫描定位线平行于听眦线,其中以显示内、外直肌、视神经能在同一层面最佳。
扫描序列:自旋回波(SE)T1WI横断位成像:TR:550 ms,TE:15 ms,视野(field of view,FOV):180 mm× 161 mm,扫描层数:12层,层厚3.5 mm,层间距0.35 mm,翻转角:90°,采集矩阵:224×178。采集次数(AC):1。采集时间(TA):148 s。
采集完图像后,将数据传输至南方医科大学第三附属医院PACS系统,包括图像、患者基本信息、序列、层厚等。随后将图像导出,导出格式为Dicom,再利用本文提出的基于MRI图像对眼眶脂肪体积进行测量的方法(详见1.4),对MRI图像数据进行脂肪体积测量,整个眼眶脂肪体积测量过程从导入图像到Photoshop后开始进行计时,测量由2名专业领域且专业水平不同的操作人员连续10 d进行,测量结果将进行重复性、一致性及信度检验。
1.2 标准化脂肪模型的建立我们采用3D打印的形式,建立1个内径为30 mm× 30 mm×30 mm的立方体模具,随后校验模具内径,确认模具内径为30 mm×30 mm×30 mm,即此模具标准容积为27 mL。随后我们将市售黄油加热融化(商品名:总统淡味黄油棒,商品号:3228022000311)并进行离心(3500 g,3 min,37 ℃),取离心管最上层液体灌注入标准化模具中,此过程保持平稳,待黄油液面灌注超出模具顶面时,停止灌注。随后室温下等待30 min~1 h,待黄油凝固后以平整工具刮去超出模具顶面的多余部分黄油,使黄油与顶面成平整状态。
1.3 标准化脂肪模型的MRI图像获取对模型进行MRI扫描,扫描标准、导出方式及格式与1.1节叙述一致。紧接着利用MRI图像数据进行脂肪体积测量,测量从导入图像至Photoshop开始计时,测量由2名专业领域且专业水平不同的操作人员进行,测量结果与模型标准体积(27 cm3)进行对比以计算测量误差(详见1.5节)。
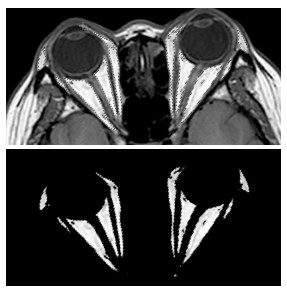
1.4 脂肪体积的测量计算对导出的Dicom图像采用Adobe® Photoshop CC 2015进行处理。首先将Dicom图像导入至Photoshop并将图像修改为实际大小,然后依次调整图像曝光度(0.3~0.9)、位移(0~0.45)以及灰度系数(0.3~1),紧接着对图像通道进行色阶处理(阴影输入色阶40~150,高光输入色阶90~200),即可抽出初步眼眶脂肪选区。以上过程均为自动化操作,可以用批处理命令以自动完成。接下来,人工对初步选区进行分割并获得最终选区(图 1)。最后将汇总的面积以近柱体体积公式进行体积计算。整个体积测量过程,包括人体MRI图像数据、模具MRI数据,均由2名各专业领域且专业水平不同的操作人员进行。近柱体体积公式如下:
|
图 1 最终选区的形成 Figure 1 Formation of the final selection. |
V=(S1+S2+……+Sp)×2.54×2.54×层厚(S1、S2……Sp为单层图像脂肪面积)
1.5 眼眶脂肪体积测量的精确度、信度、可重复性、一致性分析本文通过平均差百分比(MD%)、变异系数(CV)进行精确度、信度分析。通过组内相关系数(ICC)[22]进行信度分析,描绘Bland-Altman [23]图进行组内一致性分析。
本文数据均采用SPSS 20.0统计软件分析,定量资料以均数±标准差表示,进行信度、一致性、可重复性等分析。
2 结果 2.1 利用CT、MRI图像进行体积测量的精确度对比同一名操作员同时对体积为27 cm3的标准模具的CT及MRI图像进行体积测量,利用CT图像测得的体积为36.48±1.55 cm3,平均差百分比为34.50%;利用MRI图像测得的体积为26.85±0.44 cm3,平均差百分比为-0.77%。
2.2 两种测量方法所需时间的对比结果2名操作员分别利用本研究方法及既往研究的Mimics三维重建体积测量方法,对同一只眼眶进行眼眶脂肪体积测量,计算从扫描到测量测眼眶脂肪体积时间,操作员1:利用本研究方法用时466.13±22.03 s,利用Mimics三维重建用时2155.22±33.59 s;操作员2:利用本研究方法用时422.55±42.19 s,利用Mimics三维重建用时2007.22±25.68 s。
2.3 模具测量及精确度检验结果已知标准脂肪模具的体积为27 cm3(表 1),操作员1运用上述方法学测量标准脂肪模具体积为26.86± 0.02 cm3(平均差百分比:-0.61%),操作员2测量值为26.80±0.03 cm3(平均差百分比:-0.73%),两者较实际模具体积平均差百分比绝对值均小于1%。
| 表 1 模具测量结果 Table 1 Measurements of the model |
2名操作人员连续10 d对同一只眼眶进行脂肪体积测量(表 2),操作人员1测量所需时间为277.44± 41.53 s,体积为17.93±0.09 cm3;操作人员2测量所需时间为237.73±35.61 s,体积为17.93±0.07 cm3。两名操作人员测量耗时较短,此方法测量数据快速。两组数据变异系数(CV)分别为:0.50%、0.39%,分析两者可重复性,两者变异系数均小于1%。
| 表 2 单眼眼眶脂肪体积测量结果 Table 2 Measurements of one orbital fat |
两名操作人员同时测量10名甲状腺相关性眼病患者眼眶脂肪体积,组内相关系数(ICC)为0.996,95%置信区间为(0.985,0.999),ICC为0表示不可信,为1表示完全可信,大于0.75表示信度良好,本研究ICC介于0.75~1之间。
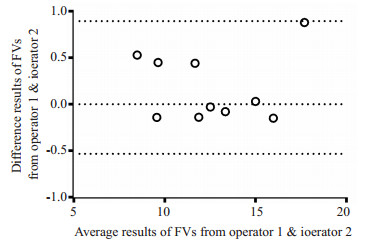
图 2显示的是Bland-Altman差值法分析结果。两名操作人员测量的两组数据的差值偏倚为0.18,偏倚标准差为0.37,则95%一致性界限为(-0.54,0.90),其一致性界限较窄,且只有一个数据点落到95%一致性界限上。
|
图 2 操作员1 & 2测量的眼眶脂肪体积的Bland-Altman图 Figure 2 The Bland-Altman plot of FVs measured by operator 1 & 2. |
依据本文结果,通过目前临床常规采集的眼眶MRI序列图像即可对眼眶脂肪体积进行测量,并且具有测量速度快,重复性好,精确度高等优势。
就测量速度而言,对比已有的基于影像学检查的测量脂肪体积的方法[7-9, 12],我们新方法用时远远低于前者,这是其一大优势。这里的用时短是双方面的。一方面,患者进行的是SE序列T1WI成像扫描,在临床常见且采集时间短,相对比起前人[13-15]行影像学检查所耗的时间,此成像扫描所耗时间大大减少;另一方面,对比起其它类型的图像处理软件,Photoshop已诞生多年,中间历经多次改版优化,图像处理速度较其它同类型软件具有优势,同时因为已进入市场多年、适用领域广泛、支持文件批处理等原因,其操作十分简便,易于上手,因而在单层图像的面积获取方面,其用时也低于其它同类软件,学习成本较同类软件也更低,对操作人员软件知识掌握要求不高。
在本研究中我们也对此新测量方法进行了重复性、信度检测,从变异系数、组内相关系数均可以看出新的测量眼眶脂肪体积的方法可重复性高、信度优;通过Bland-Altman [23]差值法分析的结果也提示不同测量者间一致性高。以上优势都是由于本研究测量方法的自动化的程度较以前方法高。在我们建立的新方法中,人工操作的部分仅存在于初始选区获取之后,最终选区获得之前,也就是说我们已经实现了整个测量过程中自动化处理过程大部分化,因而带来的人工误差也相对较小。相比起以前手动勾画眼眶及眼眶脂肪选取的手动或半自动方法[7-8, 12, 24],我们的新方法所耗人力大幅度降低。
而对本研究新测量方法精度的检验上,我们选择建立一个标准的脂肪模具以完成对新方法测量精度的校验。就结果而言,这种新方法测量精度较高,但这其中尚有一些误差未能排除。一方面,我们使用的标准脂肪模具为正方体,也就是柱体,而眼眶脂肪是不规则体,而我们使用的体积公式是近柱体的累积计算公式,公式对于不规则体的测量其本身存在一定的系统误差,但鉴于眼眶脂肪的不规则性,我们尚在寻找一种合适的方法对其进行校正。另一方面,我们的新方法主要建立在层厚较大的T1WI成像基础上,图像采集虽然耗时较短,但较大的层厚也必然会导致相当一部分结构信息的丢失,这也是误差的另一个来源。
现有的IDEAL、传统Dixon等方法是通过脂像图片信号计算得出脂肪分数,是半定量的脂肪量化方法;并且IDEAL、Dixon等方法对磁共振技术要求较高,需要特定设备与序列,临床推广性不强。相比现有的三维重建方法,本文所建立的新方法显然在节省人力和时间成本上具有巨大优势,故此新方法具有良好的临床推广性,能够让临床医生更好地了解患者眼眶后软组织情况,有助于TAO的诊断、治疗、预后随访。同时测量眼眶脂肪体积所利用的T1WI成像的1.5TMRI图像普通磁共振仪器均可采集,这比起既往研究所利用的3.0T磁共振[13-15]设备及CT仪器[1, 8, 11, 25],更常见且适用度广、危害性小,在我国二三级城市也常见。总而言之,我们的新方法可以行之有效地对眼眶MRI图像进行眼眶脂肪体积测量,它快速简便,具有耗时短、精确度高、重复性好、一致性高、可信度优、学习成本低等优势,极具临床推广价值。
| [1] | Regensburg NI, Wiersinga WM, Berendschot TT, et al. Do subtypes of graves' orbitopathy exist?[J]. Ophthalmology, 2011, 118(1): 191-6. DOI: 10.1016/j.ophtha.2010.04.004. |
| [2] | Nishida Y, Tian S, Isberg B, et al. Significance of orbital fatty tissue for exophthalmos in thyroid-associated ophthalmopathy[J]. Graefes Arch Clin Exp Ophthalmol, 2002, 240(7): 515-20. DOI: 10.1007/s00417-002-0498-3. |
| [3] | 蔡季平. 甲状腺相关眼病手术治疗[J]. 中国实用内科杂志, 2015, 35(07): 577-80. |
| [4] | Smith TJ, Hegedus L. Graves' disease[J]. N Engl J Med, 2016, 375(16): 1552-65. DOI: 10.1056/NEJMra1510030. |
| [5] | Smith TJ. TSH-receptor-expressing fibrocytes and thyroid-associated ophthalmopathy[J]. Nat Rev Endocrinol, 2015, 11(3): 171-81. DOI: 10.1038/nrendo.2014.226. |
| [6] | Yamamoto K, Itoh K, Yoshida S, et al. A quantitative analysis of orbital soft tissue in Graves' disease based on B-mode ultrasonography[J]. Endocrinol Jpn, 1979, 26(2): 255-61. DOI: 10.1507/endocrj1954.26.255. |
| [7] | Regensburg NI, Kok PH, Zonneveld FW, et al. A new and validated CT-based method for the calculation of orbital soft tissue volumes[J]. Invest Ophthalmol Vis Sci, 2008, 49(5): 1758-62. DOI: 10.1167/iovs.07-1030. |
| [8] | Kim HC, Yoon SW, Lew H. Usefulness of the ratio of orbital fat to total orbit area in mild-to-moderate thyroid-associated ophthalmopathy[J]. Br J Radiol, 2015, 88(153): 20150164. |
| [9] | Ji Y, Qian Z, Dong Y, et al. Quantitative morphometry of the orbit in Chinese adults based on a three-dimensional Reconstruction method[J]. J Anat, 2010, 217(5): 501-6. DOI: 10.1111/joa.2010.217.issue-5. |
| [10] | Potgieser PW, Wiersinga WM, Regensburg NI, et al. Some studies on the natural history of Graves' orbitopathy: increase in orbital fat is a rather late phenomenon[J]. Eur J Endocrinol, 2015, 173(2): 149-53. DOI: 10.1530/EJE-14-1140. |
| [11] | Byun JS, Moon NJ, Lee JK. Quantitative analysis of orbital soft tissues on computed tomography to assess the activity of thyroidassociated orbitopathy[J]. Graefes Arch Clin Exp ophthalmol, 2017, 255(2): 413-20. DOI: 10.1007/s00417-016-3538-0. |
| [12] | Comerci M, Elefante A, Strianese D, et al. Semiautomatic regional segmentation to measure orbital fat volumes in thyroid-associated ophthalmopathy[J]. Neuroradiol J, 2013, 26(4): 373-9. DOI: 10.1177/197140091302600402. |
| [13] | Higashiyama T, Nishida Y, Ohji M. Changes of orbital tissue volumes and proptosis in patients with thyroid extraocular muscle swelling after methylprednisolone pulse therapy[J]. Jpn J Ophthalmol, 2015, 59(6): 430-5. DOI: 10.1007/s10384-015-0410-4. |
| [14] | Kaichi Y, Tanitame K, Itakura H, et al. Orbital fat volumetry and water fraction measurements using T2-Weighted FSE-IDEAL imaging in patients with Thyroid-Associated orbitopathy[J]. AJNR Am J Neuroradiol, 2016, 37(11): 2123-8. DOI: 10.3174/ajnr.A4859. |
| [15] | Hu H, Xu XQ, Wu FY, et al. Diagnosis and stage of Graves' ophthalmopathy: Efficacy of quantitative measurements of the lacrimal gland based on 3-T magnetic resonance imaging[J]. Exp Ther Med, 2016, 12(2): 725-9. DOI: 10.3892/etm.2016.3389. |
| [16] | 刘洲君, 刘超. 甲状腺相关性眼病影像学诊断的研究进展[J]. 江苏医药, 2015, 41(6): 691-3. |
| [17] | 洪庆山, 沈洁, 薛耀明, 等. MRI在甲状腺相关眼病分级和分期的应用[J]. 中华内分泌代谢杂志, 2010, 26(3): 215-6. |
| [18] | 范艳飞, 沈洁, 李际敏, 等. MRI定量指标用于评定甲状腺相关眼病活动分期的可行性探讨——附84例报告[J]. 新医学, 2010, 41(3): 160-3. |
| [19] | Prummel MF, Gerding MN, Zonneveld FW, et al. The usefulness of quantitative orbital magnetic resonance imaging in Graves' ophthalmopathy[J]. Clin Endocrinol (Oxf), 2001, 54(2): 205-9. DOI: 10.1046/j.1365-2265.2001.01220.x. |
| [20] | 王研, 张志常. Photoshop软件在临床影像诊断及医学形态学方面的应用[J]. 电脑与信息技术, 2012, 20(3): 27-8, 51. |
| [21] | Bartley GB, Gorman CA. Diagnostic criteria for Graves' ophthalmopathy[J]. Am J Ophthalmol, 1995, 119(6): 792-5. DOI: 10.1016/S0002-9394(14)72787-4. |
| [22] | Bartko JJ. The intraclass correlation coefficient as a measure of reliability[J]. Psychol Rep, 1966, 19(1): 3-11. DOI: 10.2466/pr0.1966.19.1.3. |
| [23] | Bland JM, Altman DG. Statistical methods for assessing agreement between two methods of clinical measurement[J]. Lancet, 1986, 1(8476): 307-10. |
| [24] | 蒋丽琼, 何小寒, 刘桂琴, 等. 利用ImageJ软件测量眼眶脂肪体积[J]. 中国CT和MRI杂志, 2016, 14(3): 11-3, 17. |
| [25] | Forbes G, Gehring DG, Gorman CA, et al. Volume measurements of normal orbital structures by computed tomographic analysis[J]. AJR Am J Roentgenol, 1985, 145(1): 149-54. DOI: 10.2214/ajr.145.1.149. |
 2017, Vol. 9
2017, Vol. 9

