2. 南方医科大学南方医院 肝胆外科,广东 广州 510515;
3. 南方医科大学南方医院 心理科,广东 广州 510515;
4. 南方医科大学南方医院 南方医科大学 中西医结合医院外 二科,广东 广州 510315
2. Department of Hepatobiliary Surgery, Nanfang Hospital, Southern Medical University, Guangzhou 510515, China;
3. Department of Psychology, Nanfang Hospital, Southern Medical University, Guangzhou 510515, China;
4. Second Department of Surgery, Traditional Chinese Medicine-Integrated Hospital Affiliated to Southern Medical University, Guangzhou 510315, China
长效干扰素(PegIFN)作为一线抗病毒药物之一被广泛应用于慢性乙型肝炎(CHB)患者的抗病毒治疗。其优势在于抑制/降解病毒的同时还可增强机体的细胞免疫功能,产生免疫控制,形成双重机制的抗病毒作用。但PegIFN在使用过程中存在较多不良反应,包括流感样症候群、不同程度的白细胞减少、不同程度的精神心理异常等[1-2]。其中,常见的精神心理症状有抑郁、焦虑、烦躁、易激惹、睡眠障碍、注意力下降、意志力下降、性功能障碍等[1]。这些精神心理异常引起的主诉常常困扰基层医院感染病科的医患双方:既影响患者的生活质量,又降低患者对PegIFN治疗的依从性,迫使其主动或被动地进行药物减量或过早停药[3-4],从而导致PegIFN治疗失败。既往PegIFN所致的精神心理异常的评估涉及复杂的量表评估、精神心理科转诊,患者接受程度低;干预治疗涉及到精神类药物的应用,感染病科医师常不熟悉。虽然国外有PegIFN治疗前给予精神药物预防性干预的报道[5-8],但国内对CHB患者PegIFN治疗中出现的抑郁、焦虑进行测评、干预和随访的研究尚未见报道。我们近年来与精神心理科合作,在临床实践中采用简洁的PHQ-9量表和GAD-7量表进行精神心理异常测评,用艾司西酞普兰或阿普唑仑处理PegIFN治疗过程中出现的抑郁和焦虑症状,同时比较分析两种干预药物的疗效,取得了满意的结果。现报道如下。
1 资料和方法 1.1 病例选择病例均为南方医科大学南方医院感染内科2014年1月~2016年6月收治的CHB患者。所有CHB患者的诊断均符合中华医学会肝病学分会与感染病学分会联合制订的《慢性乙型肝炎防治指南》(2010版)标准[9]。纳入标准:诊断为CHB患者;年龄在18~65岁之间;接受PegIFN治疗,治疗前经评估无抑郁或焦虑等精神心理异常,自愿参加本研究,并签署知情同意书;具备基本的阅读和认知能力,能够接受精神心理异常的问卷调查。排除标准:其他肝炎病毒重叠感染;合并自身免疫性肝病或遗传代谢性肝病等;既往有精神疾病史;未能控制的自身免疫性疾病;妊娠;失代偿期肝硬化;其他不适合本研究的情况。本研究共纳入165名患者,其中男性107例(64.8%),女性58例(35.2%)。年龄为21~56岁,年龄(32.7±7.0)岁。
1.2 治疗方法CHB患者均接受PegIFN(PegIFN α-2a)治疗,疗程48周,随访24周。药物剂量和用法:Peg-IFNα-2a(派罗欣,罗氏公司)180 μg或者135μg(体质量≥60 kg时180 μg,<60 kg时135 μg),皮下注射,每周1次。
1.3 量表和评估标准本研究使用的PHQ-9量表和GAD-7量表是由美国精神医学会(APA)出版的《精神疾病诊断与统计手册》第5版(DSM-5)推荐的量化评估标准,2013年5月发布,随后由中华医学会精神科分会向全国推广。这两个量表内容简洁,可操作性强,经国内外研究验证具有良好的信度和效度[10-12]。PHQ-9抑郁量表为4级评分,其中0~4分:没有抑郁;5~9分:轻度抑郁;10~14分:中度抑郁;15~27分:重度抑郁。GAD-7焦虑量表为4级评分,其中0~4分:没有焦虑;5~9分:轻微焦虑;10~14分:中度焦虑;15~21分:重度焦虑。
1.4 研究方法在使用PegIFN治疗12周时对165例CHB患者按时(±1周)进行PHQ-9量表和GAD-7量表问卷调查。调查者经过系统培训,采用统一指导语。两个量表均由受试对象在自愿及不受影响的环境下自行填写。在开始评定前,先由调查人员把总的评分方法和要求向受试对象交代清楚,然后让其做出独立的自我评定。评定的时间范围是“最近两个星期”的实际感觉。评定结束时,由患者本人和临床医生逐一核对,凡有漏评或者重复评定的,均提醒患者再考虑评定,以免影响分析的准确性。从165例患者中筛选出有中重度抑郁或中重度焦虑症状的患者,均经过精神科医生确认,之后进入干预研究队列。单纯中重度抑郁患者使用艾司西酞普兰进行干预,单纯中重度焦虑患者使用阿普唑仑干预,合并中重度抑郁和中重度焦虑的患者根据其患者意愿选择艾司西酞普兰或者阿普唑仑进行干预。
1.5 艾司西酞普兰和阿普唑仑干预治疗方法及疗效评估对于需要使用艾司西酞普兰和阿普唑仑控制抑郁和焦虑症状的患者,记录其开始用药的时间,艾司西酞普兰用法为10 mg/d,连续用药8周,随访期间若评分正常则巩固治疗2周后停药,停药4周后再次测评;阿普唑仑初始剂量为0.4 mg/d,然后根据患者的病情调整剂量至0.8~2.4 mg/d,疗程和随访测评与艾司西酞普兰相同。疗效测评使用PHQ-9量表和GAD-7量表进行测评,比较艾司西酞普兰和阿普唑仑治疗2周,4周,8周以及停药4周后PHQ-9量表和GAD-7量表评分的变化情况。
1.6 统计学分析统计学分析采用SPSS21.0统计软件包对所有数据进行处理分析,计量资料以均数±标准差表示,组内不同时间点测得的评分差异采用重复测量方差分析,组间相同时间点测得的评分差异采用配对t检验,P<0.05为差异有统计学意义。
2 结果 2.1 患者基线特征患者的一般资料,包括人口统计学特征和生化、病毒学及其他临床资料见表 1。纳入本研究的165例CHB病人中,51例出现了中重度抑郁或焦虑症状,需要药物干预,为干预组(精神药物干预组),其余病例为对照组。比较干预组和对照组的基线特征,发现男性是PegIFN治疗过程中发生中重度抑郁或焦虑的影响因素(P<0.05),而年龄、肝硬化、ALT、AST、ALB、TBIL、Log HBV DNA的基线水平在两组中无统计学差异(P<0.05)。
| 表 1 接受PegIFN治疗的CHB患者基线情况 Table 1 Baseline characteristics of the patients receiving PegIFN treatment |
在PegIFN治疗第12周时对165名患者同时使用PHQ-9量表和GAD-7量表进行精神心理异常测评。37例患者由精神科医师判断为中重度抑郁,发生率为22.4%;31例为中重度焦虑,发生率为18.8%;其中,合并中重度抑郁和中重度焦虑的患者有17例,发生率为10.3%。
2.3 艾司西酞普兰对抑郁以及阿普唑仑对焦虑的干预效果单纯中重度抑郁的患者(n=20)在使用艾司西酞普兰治疗后,PHQ-9量表评分在第2、4、8周时都在逐渐下降,即症状得到改善,说明从第2周开始即起药效,治疗前后的评分差异有统计学意义。单纯中重度焦虑的患者(n=14)在使用阿普唑仑治疗后,GAD-7量表评分也从第2周开始逐渐下降,与治疗前相比有统计学意义。干预治疗8周后,我们根据量表得分趋于正常而给患者停药,并于停药4周后再次测评,发现得分没有上升(PHQ-9评分:5.5±1.8;GAD-7评分:5.2±1.4),提示患者经过干预治疗恢复正常后,停药后其抑郁和焦虑症状也没有复发。表 2显示艾司西酞普兰对抑郁以及阿普唑仑对焦虑均有效。
| 表 2 接受PegIFN治疗的CHB患者基线及药物干预后第2、4、8周PHQ-9及GAD-7评分 Table 2 PHQ-9 and GAD-7 scores in PegIFN-treated patients before and after intervention (Mean±SD) |
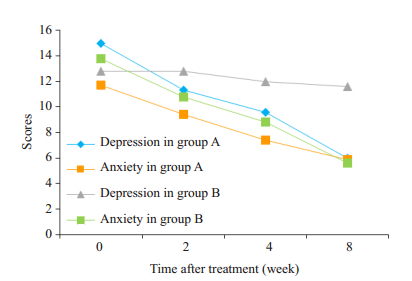
合并中重度抑郁和中重度焦虑的17例患者中,根据患者个人意愿选择艾司西酞普兰或者阿普唑仑进行干预,最终进入艾司西酞普兰组(A组)有10人,进入阿普唑仑组(B组)有7人。使用药物干预后两组的抑郁和焦虑症状改善情况如图 1所示。
|
图 1 艾司西酞普兰和阿普唑仑对抑郁和焦虑症状的疗效比较 Figure 1 Efficacy of escitalopram and alprazolam in relieving depression and anxiety. |
使用艾司西酞普兰治疗后,A组患者的PHQ-9评分和GAD-7评分均从第2周开始有明显下降,治疗前后有统计学意义(PHQ-9:F=11.133,P=0.000;GAD-7:F= 11.281,P=0.000)。使用阿普唑仑治疗后,B组患者GAD-7评分较治疗前有显著下降(F=9.352,P=0.001),但PHQ-9评分下降不明显,与治疗前比较无统计学差异(F=0.186,P=0.904)。说明艾司西酞普兰对抑郁和焦虑均有较好疗效,阿普唑仑对焦虑效果显著,但对抑郁效果不明显。比较A、B两组在焦虑方面的改善情况,通过分析两组治疗前和治疗后8周评分的下降幅度,发现B组患者评分下降幅度更大一些,差异有统计学意义(t=-3.198,P=0.010),即焦虑症状改善更明显。
3 讨论由于具有抗病毒和免疫控制双重机制的治疗作用,长效干扰素在治疗CHB患者中,若适应证选择得当,常可获得HBeAg/HBeAb转化率高,临床治愈率(HBsAg消失或血清学转化)高的明显优势[13-14]。随着近年来国内外慢性乙型肝炎防治指南将HBsAg的消失或血清学转化列为理想的治疗目标[15],长效干扰素治疗人数逐渐增多。既往长效干扰素较复杂的不良反应,特别是抑郁和焦虑等精神心理异常的特点、测评、认定和处理,常使感染病科医师觉得棘手[16]。既影响患者的生活质量、增加了医疗风险,也降低了患者对长效干扰素治疗的依从性[17-18]。针对这一特殊问题,我们建立了接受长效干扰素治疗CHB患者的随访队列,与精神心理科密切合作,在国内率先同时使用简洁的PHQ-9量表和GAD-7量表对接受PegIFN治疗的CHB患者进行精神心理评估,解决了患者精神心理异常及早发现、准确评估、及时治疗的难题。通过对165例接受PegIFN治疗的CHB患者进行精神心理评估,发现中重度抑郁的患者有37例,发生率为22.4%;中重度焦虑的患者有31例,发生率为18.8%;其中,合并中重度抑郁和中重度焦虑的有17例。这与国外Pavlovic等[19]的研究报道结果基本相似。
艾司西酞普兰是西酞普兰的左旋对映体,体内对5-HT再摄取的抑制作用较后者高5~7倍,是抗抑郁治疗的主力药物之一;阿普唑仑属短效地西泮类,抗焦虑作用比地西泮高10倍,是精神心理科用于抗焦虑的常用药物。两种药物均具有用量小,副作用轻微,不影响日常工作,易于为非精神心理科的医师掌握使用、易于被患者接受等特点[20-22]。我们在与精神心理科医师多次讨论后,将两个药物用于控制PegIFN治疗CHB患者引发的精神心理异常的干预,结果证实艾司西酞普兰或阿普唑仑对干扰素引起的抑郁或焦虑症状疗效好,安全性高。这些结果为临床上常规评估使用PegIFN的患者的精神心理异常及其程度,并对安全、有效地使用艾司西酞普兰或阿普唑仑控制这些异常提供了临床数据和依据。国内尚未见类似报道。为评估艾司西酞普兰对抑郁以及阿普唑仑对焦虑的干预效果,我们对出现单纯中重度抑郁的患者使用艾司西酞普兰干预后,发现PHQ-9评分逐渐下降,即病人的抑郁症状得到改善。单纯中重度焦虑的患者在使用阿普唑仑治疗后,GAD-7评分亦逐渐下降。干预治疗8周后,量表得分恢复正常的患者,巩固治疗2周后,可根据其意愿停药,并积极调节情绪。于停药4周后再次测评,发现得分没有上升,提示患者经过干预治疗恢复正常,停药后抑郁和焦虑症状没有复发,说明艾司西酞普兰对抑郁以及阿普唑仑对焦虑均有较好疗效。在队列随访中证实疗效良好,停药后辅以心理、行为指导,未见复发。对轻度抑郁和焦虑,我们主要提供心理、行为指导,鼓励每天参加半小时以上的文体活动,均在4~12周内得到明显缓解;这些结果提示:与精神科诊断的抑郁症或焦虑症患者有所不同, PegIFN治疗引起的精神心理异常是属于一过性的。适时使用艾司西酞普兰干预抑郁症状或者阿普唑仑干预焦虑症状都能在短期内取得良好的临床效果,从而明显提高患者对PegIFN治疗的依从性。
我们通过分析合并中重度抑郁和焦虑症状患者的测评结果来比较艾司西酞普兰和阿普唑仑对抑郁和焦虑的疗效,发现A组患者的抑郁和焦虑的评分都有明显下降,说明艾司西酞普兰对抑郁和焦虑均有较好疗效。Jiang等[23]的研究表明,艾司西酞普兰对伴有焦虑症状的重度抑郁障碍患者具有明显疗效和良好的耐受性,这与我们的结论一致。同样,齐明华等[24]研究认为,艾司西酞普兰对长效干扰素治疗引发的抑郁症状、焦虑症状和敌对症状等均有明显的治疗效果。此外,我们发现B组患者焦虑的评分下降也比较明显,但抑郁评分前后差异没有统计学意义,说明阿普唑仑对焦虑症状疗效显著,但对抑郁症状疗效不明显。我们针对艾司西酞普兰和阿普唑仑在焦虑症状的改善情况进行对比,发现阿普唑仑比艾司西酞普兰疗效要好。李涛等[25]研究显示,艾司西酞普兰和阿普唑仑治疗广泛性焦虑障碍都具有良好的效果,但其只对两组间的有效率进行了比较,而我们的研究中通过计算患者在干预前以及干预第8周评分下降的幅度来比较两个药物的疗效,发现阿普唑仑治疗焦虑评分下降的幅度更大一些(t=-3.198,P=0.010),即阿普唑仑治疗焦虑症状的疗效比艾司西酞普兰要好。
综上所述,对CHB患者由PegIFN诱发的精神心理症状调查显示,中重度抑郁和中重度焦虑的发生率较高(分别为22.4%和18.8%);对中重度抑郁和中重度焦虑的药物干预研究表明,艾司西酞普兰对抑郁和焦虑均有较好疗效,阿普唑仑对焦虑效果显著,但对抑郁效果尚不明显;在焦虑改善方面,阿普唑仑比艾司西酞普兰疗效要好。因此,在长效干扰素治疗过程中应定期对患者的精神状况进行监测,采用简洁的PHQ-9抑郁量表和GAD-7焦虑量表可以及时发现接受长效干扰素治疗的CHB患者的精神心理异常,适当的药物干预有良好疗效,值得多中心大样本深入研究后临床推广应用。
| [1] | Yang JF, Kao YH, Dai CY, et al. Comparison of adverse effects related to pegylated interferon-based therapy for patients with chronic hepatitis B and chronic hepatitis C in Taiwan[J]. Hepatol Int, 2010, 4(4): 732-40. DOI: 10.1007/s12072-010-9208-0. |
| [2] | 李明慧, 谢尧. 慢性病毒性肝炎患者干扰素α治疗不良反应临床处理专家共识[J]. 临床肝胆病杂志, 2014, 30(11): 1106-11. DOI: 10.3969/j.issn.1001-5256.2014.11.003. |
| [3] | Park SH. Completion of chronic hepatitis C virus treatment in interferon-induced major depressive disorder with psychotic features[J]. Psychiatry Investig, 2011, 8(4): 381-3. DOI: 10.4306/pi.2011.8.4.381. |
| [4] | Mm B, A Y, U Y, et al. Major depressive disorder and generalized anxiety disorder and response to treatment in hepatitis C patients in Egypt[J]. Int J Psychiatry Med, 2015, 50(2): 147-62. DOI: 10.1177/0091217415605029. |
| [5] | Hotho DM, Bezemer G, Hansen BE, et al. Effects of escitalopram prophylaxis during antiviral treatment for chronic hepatitis C in patients with a history of intravenous drug use and depression[J]. J Clin Psychiatry, 2014, 75(10): 1069-77. |
| [6] | Schaefer M, Berg T, Sarkar S, et al. Escitalopram for the prevention of peginterferon-alpha2a-associated depression[J]. Ann Intern Med, 2013, 158(2): 140. |
| [7] | De Knegt RJ, Bezemer G, Van Gool AR, et al. Randomised clinical trial: escitalopram for the prevention of psychiatric adverse events during treatment with peginterferon-alfa-2a and ribavirin for chronic hepatitis C[J]. Aliment Pharmacol Ther, 2011, 34(11/12): 1306-17. |
| [8] | Schaefer M, Sarkar R, Knop V, et al. Escitalopram for the prevention of peginterferon-alpha 2a-Associated depression in hepatitis C Virus-Infected patients without previous psychiatric disease a randomized trial[J]. Ann Intern Med, 2012, 157(2): 94-103. DOI: 10.7326/0003-4819-157-2-201207170-00006. |
| [9] | 中华医学会肝病学分会. 中华医学会感染病学分会.慢性乙型肝炎防治指南(2010年版)[J]. 中华肝脏病杂志, 2011, 19(1): 13-24. |
| [10] | 孙晓艳, 李怡雪, 余灿清, 等. 中文版抑郁量表信效度研究的系统综述[J]. 中华流行病学杂志, 2017, 38(1): 110-6. |
| [11] | 何筱衍, 李春波, 钱洁, 等. 广泛性焦虑量表在综合性医院的信度和效度研究[J]. 上海精神医学, 2010, 22(4): 200-3. |
| [12] | Belk RA, Pilling M, Rogers KD, et al. The theoretical and practical determination of clinical cut-offs for the British Sign Language versions of PHQ-9 and GAD-7[J]. BMC Psychiatry, 2016, 16(1): 372. DOI: 10.1186/s12888-016-1078-0. |
| [13] | Krishnamoorthy TL, Mutimer D. Hepatitis B: encouraging the use of interferon[J]. Curr Opin Infect Dis, 2015, 28(6): 557-62. DOI: 10.1097/QCO.0000000000000209. |
| [14] | Konerman MA, Lok AS. Interferon treatment for hepatitis B[J]. Clin Liver Dis, 2016, 20(4): 645-65. DOI: 10.1016/j.cld.2016.06.002. |
| [15] | European Association for the Study of the Liver. EASL 2017 Clinical Practice Guidelines on the management of hepatitis B virus infection[J]. J Hepatol, 2017, 67(2): 370-98. DOI: 10.1016/j.jhep.2017.03.021. |
| [16] | Coman HG, Herta DC, Nemes B. Psychiatric adverse effects of interferon therapy[J]. Clujul Med, 2013, 86(4): 318-20. |
| [17] | Hepgul N, Pariante CM, Baraldi S, et al. Depression and anxiety in patients receiving interferon-alpha: The role of illness perceptions[J]. J Health Psychol, 2016, 2016: 1-10. |
| [18] | Marcellin P, Lau GK, Zeuzem S, et al. Comparing the safety, tolerability and quality of Life in patients with chronic hepatitis B vs chronic hepatitis C treated with peginterferon alpha-2a[J]. Liver Int, 2008, 28(4): 477-85. DOI: 10.1111/j.1478-3231.2008.01696.x. |
| [19] | Pavlović Z, Delić D, Marić NP, et al. Depressive symptoms in patients with hepatitis C treated with pegylated interferon alpha therapy: a 24-week prospective study[J]. Psychiatr Danub, 2011, 23(4): 370-7. |
| [20] | 陈新谦, 金有豫, 汤光. 新编药物学[M]. 第17版. 人民卫生出版社, 2011. |
| [21] | Si TM, Wang G, Yang FD, et al. Efficacy and safety of escitalopram in treatment of severe depression in Chinese population[J]. Metab Brain Dis, 2017, 32(3): 891-901. DOI: 10.1007/s11011-017-9992-5. |
| [22] | Ait-Daoud N, Hamby AS, Sharma S, et al. A Review of Alprazolam Use, Misuse, and Withdrawal[J]. J Addict Med, 2017, [Epub ahead of time]. http://www.ncbi.nlm.nih.gov/pubmed/28777203 |
| [23] | Jiang K, Li L, Wang X, et al. Efficacy and tolerability of escitalopram in treatment of major depressive disorder with anxiety symptoms: a 24-week, open-label, prospective study in Chinese population[J]. Neuropsychiatr Dis Treat, 2017, 13: 515-26. DOI: 10.2147/NDT. |
| [24] | 齐明华, 周斌, 苏梅蕾, 等. 艾司西酞普兰干预干扰素治疗慢性丙型病毒性肝炎引发的精神症状[J]. 南方医科大学学报, 2013, 33(7): 1012-6. |
| [25] | 李涛, 陈思宇. 艾司西酞普兰与阿普唑仑治疗广泛性焦虑症对照研究[J]. 现代医药卫生, 2011, 27(18): 2787-8. |
 2017, Vol. 37
2017, Vol. 37

