2. 通大学医学部生理学与病理生理学系,陕西 西安 710061
2. Department of Physiology and Pathophysiology, Xi'an Jiaotong University College of Medicine, Xi'an 710061, China
许多病人在经历过心绞痛后会引发胸痛后遗症而发展成顽固性心绞痛,如续发的纤维肌痛,并伴有肌肉紧张性的增加,这种长期发作的疼痛给患者带来剧烈的身体痛苦和严重的精神负担[1]。然而,目前人们对于心脏痛觉的中枢调控机制了解甚少,心脏痛觉模型复制困难是其重要的原因之一。动物虽无心绞痛的主观体验,可是存在与其类似的心脏伤害性感受反应。本课题组通过心包内注射致痛剂诱发大鼠心脏伤害性感受模型,对心源性疼痛的传入通路及中枢调节机制已取得初步进展[2-3]。
内源性痛觉调制系统由下行抑制系统和下行易化系统组成。研究表明[4]:脑干网状结构在痛觉调节过程中既有易化作用,又有抑制作用。延髓外侧网状核(LRN)位于延髓尾端,下橄榄核下半部的背外侧,是构成脑干网状结构的重要核团之一,是下行性镇痛系统的一个重要结构,同时参与心血管活动的调节[5-6]。电刺激或化学刺激LRN区域,对脊髓背角伤害性信息传递产生显著的抑制作用[7]。相反,电损毁LRN,脊髓背角伤害性神经元对伤害性刺激产生易化作用[8]。然而这些关于LRN的下行抑制调控作用主要集中在躯体痛觉,对于内脏痛觉,尤其是心脏痛觉的研究甚少。我们前期研究表明,电刺激LRN能够抑制心脏-躯体运动反射,那么,化学性激活LRN能否抑制心脏伤害性感受?脊髓水平5-羟色胺受体是否参与其中还不清楚。
谷氨酸是已知神经系统内最重要的兴奋性神经递质,可以选择性激活神经元的胞体,对过路纤维无影响。本研究拟通过谷氨酸微注射激活LRN,观察心包内注射缓激肽诱发心脏-躯体运动反射及脊髓背角c-Fos表达的变化,探讨化学性激活LRN对心脏伤害性感受的下行性抑制调控作用及其脊髓参与的受体机制。
1 材料和方法 1.1 实验药品与实验仪器戊巴比妥钠、缓激肽、谷氨酸及麦角新碱(均购于美国Sigma公司),麦角新碱溶于30%二甲基亚砜(麦角新碱微溶于生理盐水中,易溶于二甲基亚砜中,故二甲基亚砜作为麦角新碱的溶媒)中,配置成3 μg/mL和5 μg/mL;其余药物均溶解于生理盐水中,配制成所需浓度。戊巴比妥钠:20 mg/mL和5 mg/mL;缓激肽:0.001 mg/mL;谷氨酸:3.38 mg/mL(4 nmol/0.2 μL)、8.45 mg/ml(10 nmol/0.2 μL)、16.9 mg/mL(20 nmol/ 0.2 μL)、33.8 mg/mL(40 nmol/0.2 μL)。
BL-420A生物信号采集与分析系统及压力换能器(成都泰盟生物科技有限公司);蠕动泵(BT100-2J,保定兰格恒流泵有限责任公司);小动物呼吸机(DW3000-B型,淮北正华生物仪器设备有限公司)。
1.2 实验动物分组及模型建立 1.2.1 实验动物分组实验选用36只雄性SD大鼠,体质量280~300 g,由西安交通大学医学院实验动物中心提供,大鼠在标准清洁级环境中饲养。动物随机分为5组:缓激肽组(n=6)、缓激肽+谷氨酸组(n=6)、缓激肽+麦角新碱组(n=6)、缓激肽+谷氨酸+麦角新碱组(n= 12)、缓激肽+谷氨酸+溶媒组(n=6)。
1.2.2 实验动物模型建立实验动物给予2%戊巴比妥钠(45~55 mg/kg)腹腔麻醉。行气管插管后对动物实施人工呼吸(呼吸频率:60~70/min,潮气量:5.0~6.0 mL),左侧颈静脉插管用于补液及维持麻醉[0.05%戊巴比妥钠,15 mg(/kg·h)],右侧颈总动脉插管用于监测动脉血压,维持平均动脉压处于90~100 mmHg,从而保证一个稳定而合适的麻醉状态。暴露左侧背斜方肌,记录EMG。直肠温度计监测大鼠体温,通过温控仪维持大鼠体温在(37.0±0.5)℃。
心包插管术与给药方法:将大鼠左侧第1到第3肋软骨切断,暴露胸腺。沿胸腺中线分离胸腺2片小叶,暴露心包膜。用玻璃探针的尖端在心包膜上开一小孔,将一内径0.051 cm、外径0.094 cm、长12~14 cm远端有数个小洞的硅胶管顺胸腺中线经此孔插入心包约2 cm,依次缝合各层胸壁组织,以固定心包插管。通过心包插管心包内注射缓激肽0.2 mL,记录EMG活动60 s后回抽,0.2 mL无菌生理盐水连续冲洗心包5次,同一只大鼠,心包注射缓激肽每次间隔40 min。最后一次注射缓激肽不回抽,2 h后对大鼠经升主动脉行4%多聚甲醛灌注。
背斜方肌EMG的记录:同芯电极以30°的角度插入背斜方肌约1.5~1.7 mm,通过BL-420A生物信号采集与分析系统记录其EMG活动,每次缓激肽诱发EMG活动总放电单位数(TMUD)通过BL-420A分析软件直接统计得出。由于不同大鼠缓激肽诱发的TMUD有所不同,为了消除个体之间的差异,每只大鼠首次心包内注射缓激肽所诱发的TMUD被标化为100%,作为基础对照;其后续EMG的TMUD均以首次TMUD为分母进行标化,得出百分数,即EMG的变化率。
1.3 LRN内微量注射将动物头部固定于大鼠脑立体定位仪上,行枕骨开颅术,在闩部水平去除硬脑膜和软脑膜,暴露尾端延髓。以写翮(第四脑室尾侧最后点,相当于前囟后14.3 mm)为零坐标,依据Paxinos-Watson大鼠脑定位图谱[9]确定LRN三维坐标位置为:吻侧0.3~0.5 mm,旁开1.6~2.2 mm,脑表面下2.8~3.2 mm。为了消除谷氨酸微量注射对相邻核团神经元的影响,微量注射使用0.5 μL微量注射器(Hamilton, Reno, Nevada, USA),其尖端与玻璃微电极相连,微电极尖端直径约为50~ 100 μm,注射速度为0.2 μL/min,不同浓度谷氨酸注射量均为0.2 μL。实验结束后,LRN内同一注射位点行2%膀胺天蓝微量注射(0.2 μL)以标记谷氨酸在脑干的注射位点,只统计注射位点在LRN内的数据。
1.4 脊髓蛛网膜下腔置管术与药物注射按照Yaksh介绍的方法行脊髓蛛网膜下腔置管。动物取俯卧位,于两耳尖剪开皮肤,纵向分离肌肉,充分暴露枕骨大孔。用精细眼科手术剪小心剪开硬脊膜,可见清亮透明的脑脊液迅速涌出。使大鼠的头部向下倾斜,沿脊髓尾侧的方向将一段充满生理盐水长约10 cm PE-10管缓慢从枕骨大孔开口处插入到脊髓T3~T5蛛网膜下腔内,插入长度为3.5~4.0 cm。药物注射采用改良过的50 μL微量注射器,注射的体积均为10 μL,注射的时间约1 min。每次实验结束后,经PE-10管注入10 μL 2%膀胺天蓝以标记药物的扩散范围,统计注射位置在脊髓T3~T5的实验数据。
1.5 尼氏染色与ABC免疫组织染色以上各组处理后,暴露大鼠心脏,经左心室升主动脉插管灌注固定。先用150 mL 0.01 mol/L PBS(pH7.4)快速灌流,继之以约200 ml含30%饱和苦味酸和4%多聚甲醛的0.1 mol/L PB(PH7.4)固定溶液快速灌注固定,然后再以同样的固定液250 mL缓慢滴注,持续l.5~2 h。灌注完毕后取脑与T3~T5脊髓,置于上述新鲜固定液中后固定4 h(4 ℃)。继之将上述组织转入含30%蔗糖的0.1 mol/L PB溶液中(4 ℃)沉底后,冰冻切片,片厚30 μm。脑片行尼氏染色,在显微镜下进一步确定注射位点。T3~T5脊髓按照切片顺序隔3取1,分3组收集于含0.01 mol/L的PBS的洗片盒中备用。免疫组织化学ABC法兔抗鼠c-Fos抗体的工作浓度为1: 1000。对照实验用PBS代替一抗,其余步骤相同。用Olympus光学显微镜(BX51)照相,用软件SPOT对切片进行图像采集,用Imag-Pro-Plus软件计数。
1.6 统计学分析应用SPSS13.0统计软件进行统计学分析。各处理因素干预大鼠心包内注射缓激肽诱发EMG的变化率以均数±标准误表示,组间比较采用One-way ANOVA并LSD检验进行分析,两组间比较采用t检验,P < 0.05为有统计学意义。
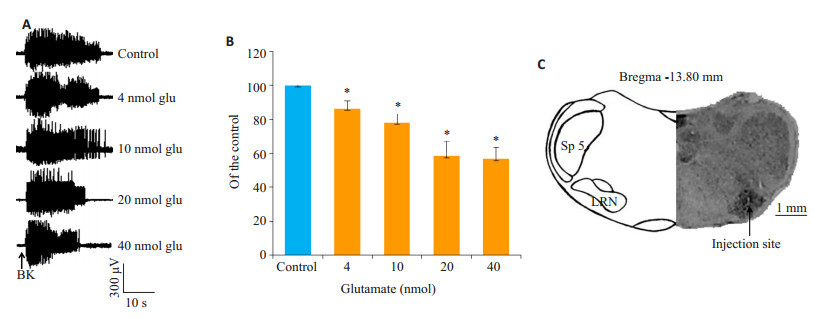
2 结果 2.1 谷氨酸微注射于LRN后心包内缓激肽诱发EMG活动的变化LRN内谷氨酸微量注射(4/10/20 nmol/0.2 μL)剂量依赖性地抑制心包内注射缓激肽诱发的心脏-躯体运动反射,EMG活动分别下降到缓激肽对照值的(86.39± 1.54)%、(77.01±0.26)%和(58.32±3.67)%。然而,当谷氨酸的剂量增加至40 nmol/0.2 μL,EMG活动不再进一步降低(图 1A、B)。
|
图 1 LRN内谷氨酸微注射前后EMG的变化 Figure 1 Changes of EMG responses after glutamate microinjection in the LRN (A), quantitative analysis (B), and a representative brain section of the microinjection site (C); *P < 0.05 vs control. Glu: Glutamate; LRN: Lateral reticular nucleus; Py: Pyramidal tract; Sp5: Spinal trigeminal nucleus. |
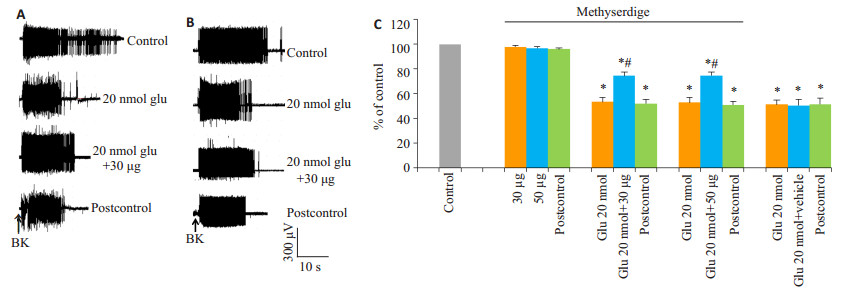
鞘内微注射非选择性5-HT受体拮抗剂麦角新碱30/50 μg对心包内注射缓激肽诱发的心脏-躯体运动反射无影响;而鞘内注射麦角新碱30/50 μg减弱了20 nmol/0.2 μL谷氨酸激活LRN所致心脏-躯体运动的抑制作用,EMG活动分别由鞘内注射前的(53.46± 1.43).%和(52.78 ± 1.77)%增加到(74.39 ± 1.22)%和(74.62 ± 1.09)%(t=11.16,P < 0.001或者t=10.53,P < 0.001)。鞘内注射等剂量溶媒EMG变化无统计学意义(图 2)。
|
图 2 谷氨酸微注射LRN联合鞘内注射麦角新碱或溶媒前后EMG的变化 Figure 2 Changes of EMG responses after glutamate microinjection in the LRN and intrathecal injection of methysergide at 30 μg (A) and 50 μg (B) and quantitative analysis of the results (C). i.t.: Intrathecal. *P < 0.05 vs control; #P < 0.05 vs glutamate. |
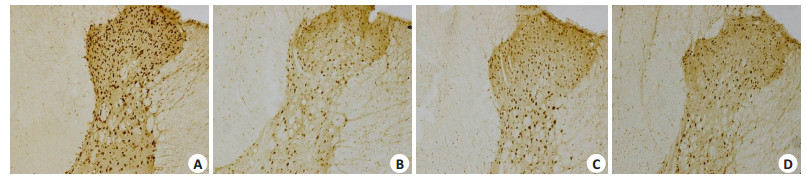
免疫组织化学结果显示,缓激肽组大鼠脊髓背角c-Fos的表达显著增多(图 3A);缓激肽+谷氨酸组大鼠脊髓背角内c-Fos表达明显减少(图 3B),与缓激肽组相比较,具有显著性差异(P < 0.05);缓激肽+谷氨酸+麦角新碱组脊髓背角c-Fos的表达有所减少(图 3C),与缓激肽组、缓激肽组+谷氨酸相比较,均具有显著性差异(P < 0.05);缓激肽+谷氨酸+溶媒组大鼠脊髓背角内c-Fos的表达明显减少(图 3D),与缓激肽组相比较,具有显著性差异(P < 0.05),但与缓激肽+谷氨酸组相比无显著性差异(P > 0.05)。
|
图 3 各组大鼠脊髓背角c-Fos的表达 Figure 3 Expressions of c-Fos in the spinal dorsal horn of rats receiving intrapericardial bradykinin injection (A), LRN glutamate microinjection (B), intra-LRN glutamate microinjection with intrathecal injection of methysergide (C), and LRN glutamate microinjection with intrathecal injection of vehicle (D) (Original magnification: ×100). |
LRN是一个重要的调节伤害性感受的脑干下行性中继站,同时也参与脊髓伤害性信息传递的调节。电或化学刺激激活LRN显著抑制躯体伤害性反射(如甩尾反射、热板反射等)和脊髓背角神经元的伤害性反应[4-5, 10-11]。动物实验和临床研究均证明心脏功能异常能够引起继发性肌肉收缩和/或肌张力增加[12-13]。2001年,Jou等建立一种心绞痛样疼痛的动物模型,通过向心包内注射致痛物质诱发动物上背部脊柱旁肌肉收缩,即诱发心脏-躯体运动反射,监测背斜方肌EMG活动可作为该反射的指标[14]。众所周知,谷氨酸是一种兴奋性氨基酸,能够选择性直接激活神经元的胞体对过路纤维无影响[15]。在本研究中,将谷氨酸微量注射于LRN剂量依赖性地抑制背斜方肌EMG活动。证明激活LRN能够抑制心脏伤害性感受,这与躯体痛的研究结果相一致[4-5, 10-11]。
Gebhart和Ossipov研究表明脊髓内5-HT受体参与了调节LRN对甩尾反射的抑制作用[10, 16]。本实验鞘内注射非选择性5-HT受体拮抗剂麦角新碱显著地降低了化学激活LRN对心脏-躯体运动反射的抑制作用。表明脊髓内5-HT受体不仅参与了LRN对躯体伤害性感受的抑制性调控,而且也参与了LRN对心脏伤害性感受的调控。然而,5-HT对脊髓伤害性反应的调节是复杂的,可能产生抑制作用,也有可能产生易化作用。这可能因为激活的受体亚型不同、注射的剂量不同或者伤害性刺激类型不同所致。有研究显示脊髓内的5-HT1、5-HT2和5-HT3受体与镇痛效应有关[2, 17-20]。麦角新碱作为5-HT1和5-HT2受体的拮抗剂被广泛使用。本研究鞘内注射麦角新碱部分翻转了化学激活LRN对心脏伤害性感受的抑制作用,提示5-HT和它的受体可能参与电刺激LRN对心脏伤害性感受的下行抑制作用。虽然LRN内或者邻近部位存在5-HT能神经元,但下行投射到脊髓的5-HT能神经元主要起源于中缝大核。已有研究表明LRN有向中缝大核投射的神经元[21]。因此,本实验观察到麦角新碱部分翻转化学激活LRN对心脏伤害性感受的下行抑制作用可能归因于激活了向中缝大核内投射的LRN神经元。
c-Fos是原癌基因中的即刻早期基因产物,1987年,Hunt等[22]首先将原癌基因用于痛觉研究中。自此,在神经科学研究中,探索伤害性感受神经通路最常用的方法之一,就是观察c-Fos在中枢神经系统的空间表达状况[23-24]。在本实验中,我们同样采取了这种方法寻找LRN对心脏伤害性感受抑制效应发生的证据及其脊髓参与的受体机制。起源于心脏的交感传入纤维进入上胸部脊髓后,与脊髓上行通路的神经元形成突触,继而这些神经元发出初级传入纤维进入脊髓T1~T6的Ⅰ~ Ⅴ、Ⅶ和Ⅹ层,及其他上行通路[25]。因此以上区域c-Fos表达的增加代表着心血管紧急事件的发生。我们的实验结果显示缓激肽激活了心脏交感传入纤维而导致T3~T5脊髓背角c-Fos表达增加,而化学性激活LRN显著抑制了c-Fos表达,鞘内注射麦角新碱部分翻转了化学激活LRN对c-Fos表达的抑制作用,支持了LRN对心脏伤害性感受的抑制调控作用,且脊髓水平的5-HT受体参与这一抑制作用。这与激活LRN对EMG影响的电生理结果相一致。
本研究结果表明化学性激活LRN对心脏伤害性感受发挥下行性抑制调控作用,且脊髓水平的5-HT受体参与这一抑制作用,至于究竟是5-HT受体何种亚型参与,有待下一步研究。
| [1] | Levine PR, Mascette AM. Musculoskeletal chest pain in patients with " angina" : a prospective study[J]. South Med J, 1989, 82(5): 580-5, 591. DOI: 10.1097/00007611-198905000-00010. |
| [2] | Jou CJ, Farber JP, Qin C, et al. Intrapericardial algogenic chemicals evoke cardiac-somatic motor reflexes in rats[J]. Auton Neurosci, 2001, 94(1-2): 52-61. DOI: 10.1016/S1566-0702(01)00345-9. |
| [3] | Han M, Liu X, Du J. Modulatory effect of neurokinin-1 and non-N-methyl-D-aspartate receptors on cardiosomatic reflex in rat spinal cord[J]. Nan Fang Yi Ke Da Xue Xue Bao, 2014, 34(12): 1728-32. |
| [4] | Mitsi V. Zachariou V modulation of pain, nociception, and analgesia by the brain reward center[J]. Neuroscience, 2016, 338: 81-92. DOI: 10.1016/j.neuroscience.2016.05.017. |
| [5] | Neuroscience HJ. (Chinese).3rd Eds.beking university medical press [M]. [S.l.]:Beijing, 2013: pp 657-9. |
| [6] | Millan MJ. Descending control of pain[J]. Prog Neurobiol, 2002, 66(6): 355-474. DOI: 10.1016/S0301-0082(02)00009-6. |
| [7] | Morton CR, Johnson SM, Duggan AW. Lateral reticular regions and the descending control of dorsal Horn neurones of the cat: selective inhibition by electrical stimulation[J]. Brain Res, 1983, 275(1): 13-21. DOI: 10.1016/0006-8993(83)90413-4. |
| [8] | Hall JG, Duggan AW, Morton CR, et al. The location of brainstem neurones tonically inhibiting dorsal Horn neurones of the cat[J]. Brain Res, 1982, 244(2): 215-22. DOI: 10.1016/0006-8993(82)90080-4. |
| [9] | Paxinos G, Watson C. The rat brain in stereotaxic coordinates (4nd edition), San Diego[M]. CA: Academic Press, 1998. |
| [10] | Gebhart GF, Ossipov MH. Characterization of inhibition of the spinal nociceptive tail-flick reflex in the rat from the medullary lateral reticular nucleus[J]. J Neurosci, 1986, 6: 701-13. |
| [11] | Morton CR, Siegel J, Xiao HM, et al. Modulation of cutaneous nociceptor activity by electrical stimulation in the brain stem does not inhibit the nociceptive excitation of dorsal Horn neurons[J]. Pain, 1997, 71(1): 65-70. DOI: 10.1016/S0304-3959(97)03340-X. |
| [12] | Schoen RE, Finn WE. A model for studying a viscerosomatic reflex induced by myocardial infarction in the cat[J]. J Am Osteopath Assoc, 1978, 78: 122-3. |
| [13] | Beal MC. Viscerosomatic reflexes:a review[J]. J Am Osteopath Assoc, 1985, 85: 786-801. |
| [14] | Jou CJ, Farber JP, Qin C, et al. Intrapericardial algogenic chemicals evoke cardiac-somatic motor reflexes in rats[J]. Auton Neurosci, 2001, 94(1/2): 52-61. |
| [15] | Marquez J, Campos-Sandoval JA, Penalver AA, et al. Glutamate and brain glutaminases in drug addiction[J]. Neurochem Res, 2017, 42(3, SI): 846-57. DOI: 10.1007/s11064-016-2137-0. |
| [16] | Janss AJ, Gebhart GF. Spinal monoaminergic receptors mediate the antinociception produced by glutamate in the medullary lateral reticular nucleus[J]. J Neurosci, 1987, 7(9): 2862-73. |
| [17] | Zhuo M, Gebhart GF. Characterization of descending facilitation and inhibition of spinal nociceptive transmission from the nuclei reticularis gigantocellularis and gigantocellularis pars alpha in the rat[J]. J Neurophysiol, 1992, 67: 1599-614. |
| [18] | Jeong CY, Choi J, Yoon MH. Roles of serotonin receptor subtypes for the antinociception of 5-HT in the spinal cord of rats[J]. Eur J Phar, 2004, 502: 205-11. DOI: 10.1016/j.ejphar.2004.08.048. |
| [19] | Mallet C, Daulhac L, Bonnefon J, et al. Endocannabinoid and serotonergic systems are needed for acetaminophen-induced analgesia[J]. Pain, 2008, 13: 190-200. |
| [20] | Kilinc E, Guerrero-Toro C, Zakharov A, et al. Serotonergic mechanisms of trigeminal meningeal nociception: Implications for migraine pain[J]. Neuropharmacology, 2017, 116: 160-73. DOI: 10.1016/j.neuropharm.2016.12.024. |
| [21] | Marchand JE, Hagino N. Afferents to the periaqueductal gray in the rat. A horseradish peroxidase study[J]. Neuroscience, 1983, 9: 95-106. DOI: 10.1016/0306-4522(83)90049-0. |
| [22] | Hunt SP, Pini A, Evan G. Induction of c-fos-like protein in spinal cord neurons following sensory stimulation[J]. Nature, 1987, 328(6131): 632-4. DOI: 10.1038/328632a0. |
| [23] | Harris JA. Using c-fos as a neural marker of pain[J]. Brain Res Bull, 1998, 45(1): 1-8. DOI: 10.1016/S0361-9230(97)00277-3. |
| [24] | 刘晓华, 韩曼, 杜剑青. 大鼠心包腔内注射辣椒素诱发c-Fos在孤束核内的表达及迷走神经切断对其表达的影响[J]. 西安交通大学学报, 2014, 35(4): 451-4. |
| [25] | Kuo DC, Oravitz JJ, Degroat WE. Tracing of afferent and efferent pathways in the left inferior cardiac nerve of the cat using retrograde and transport of horseradish peroxidase[J]. Brain Res, 1984, 321: 111-8. DOI: 10.1016/0006-8993(84)90686-3. |
 2017, Vol. 37
2017, Vol. 37

