椎体成形术(PVP)是治疗骨质疏松压缩骨折的有效方法。随着PVP的广泛应用,术后邻近节段再骨折倍受关注。据报道,432例PVP手术患者,术后86例(19.9%)发生了186个节段的新鲜骨折。其中77例(41.4%)发生在邻近节段[1]。大量的研究探讨邻椎骨折的危险因素,包括年龄、骨密度、骨折椎体的位置、骨水泥渗和术后椎体高度恢复率等[2-4]。骨水泥的位置可能与PVP术后新发骨折有关,术后骨水泥未同时接触上下终板者发生手术椎体再骨折的几率较骨水泥同时接触上下终板的患者更高,即骨水泥分布越均匀,术椎本身再骨折的风险越小[5]。椎体后凸成形术(PKP)后,骨水泥的体积分数对邻近节段骨折的发生率有显著影响[6]。骨水泥的分布包括量和位置两个要素。由于椎体大小的个体差异性,骨水泥的相对量比绝对量能够更加准确反映其分布。另外,骨水泥的弥散情况也可能对椎体的应力及负荷产生影响。既往的研究主要评价了骨水泥的绝对量及体积分数[6-8],并未考虑其分布特点对邻椎骨折的影响。本研究旨在探讨衡量骨水泥分布情况的指标-分布指数,用来描述并区分术后骨水泥的量、弥散情况及位置特点,并探讨分布指数与PVP术后邻椎骨折的关系。
1 资料和方法 1.1 一般资料选择2011年4月~2014年4月在我院诊断为骨质疏松压缩骨折并接受椎体成形术治疗的患者,共143例。术后进行1年的随访。其中男30例,女113例,年龄54~ 91岁,平均70.2岁。骨质疏松压缩骨折的诊断标准参考骨质疏松性骨折诊疗指南[9]。纳入标准:(1)胸椎或者腰椎骨质疏松压缩骨折诊断明确,并接受椎体成形手术治疗者;(2)术后按医嘱抗骨质疏松治疗;(3)获得至少1年随访。排除标准:(1)术后未进行X线复查,资料不完整的患者;(2)伴有精神疾病或者恶性肿瘤病史者;(3)合并脊柱感染、脊柱肿瘤或者代谢性骨病者[10-11]。随访期间,如发生邻近节段骨折为再骨折组,如随访结束时未发生邻近节段骨折为对照组。
1.2 手术方法患者取俯卧位,C臂定位伤椎及穿刺点后,2%利多卡因局部麻醉,C臂正位透视下经椎弓根穿刺,穿刺针到达椎弓根内侧缘后,侧位透视要求穿刺针到达椎弓根和椎体连接处,确保穿刺针经过椎弓根、到达椎体前1/3处,拔出穿刺针,向椎体内注入骨水泥。不同患者根据骨折部位及面积,调整穿刺的角度,使骨水泥灌注至骨折处。待骨水泥硬化后拔出穿刺针,酒精消毒伤口,无菌敷料包扎。术后第2天复查X线,如无异常,要求患者起床活动。出院后规范抗骨质疏松治疗。方案为:口服碳酸钙(维D钙咀嚼片,美国安士制药)600 mg/d,维生素D(骨化三醇胶丸,R.P. Scherer GmbH&Co.KG),0.25 μg/d,阿伦磷酸盐(阿仑膦酸钠,Merck Sharp & Dohme(Australia)Pty.Limited),每周70 mg。
1.3 观察指标记录患者的性别、年龄、骨密度、手术节段、骨水泥的量以及是否存在骨水泥渗漏。术后随访1年,如患者再次出现腰痛、背痛等症状,予胸腰椎MR检查,根据邻椎是否出现急性压缩骨折,分为再骨折组和对照组。
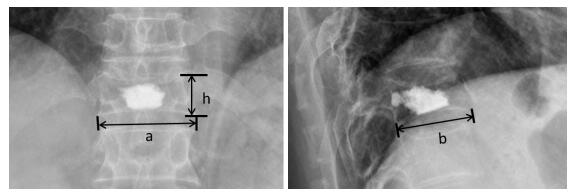
通过计算椎体的体积和骨水泥的量,获得反映骨水泥相对量的“量体指数”。具体方法如下(图 1):术后复查脊柱X线片,正位片下测量强化椎体的高度(h)、下终板长度(a),侧位片下测量下终板的长度(b)。将椎体近似看做底面为椭圆形的圆柱体,计算椎体体积V= π×a×b/2×h。量体指数为(DV)=骨水泥的量/椎体体积。
|
图 1 骨水泥量体指数的计算方法:根据术后正侧位片测量术椎下终板的长度和高度,计算椎体近似体积 Figure 1 Calculation of the volume-cubage index based on measurements on X-ray films. The lengths of the vertebral body were measured on both anterioposterior and lateral X-ray films, and the height of the vertebral body was determined on lateral X-ray to calculate the approximate vertebral cubage. |
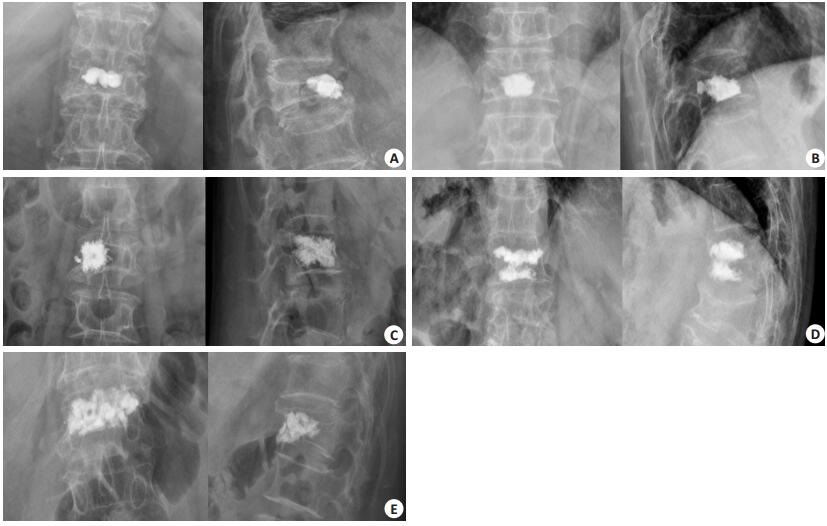
为衡量骨水泥的位置和弥散程度,通过观察术后正位和侧位X线片,将骨水泥的分布情况分为5种类型,即分布指数(DI)(表 1,图 2)。
| 表 1 骨水泥分布指数 Table 1 Classification of the patterns of cement distribution in the vertebrae (distribution index) |
|
图 2 骨水泥分布指数 Figure 2 Typical cases illustrating the distribution index of cement in the vertebrae. A, B, C, D and E: Type Ⅰ, Ⅱ, Ⅲ, Ⅳ and Ⅴ of cement distribution, respectively. |
应用SPSS13.0软件包完成统计分析。比较再骨折组和对照组性别、年龄、骨密度、手术节段、骨水泥量、是否渗漏、骨水泥分布指数(DI)、量体指数(DV)的差异,计量资料以均数±标准差表示,采用两独立样本t检验,计数资料采用Person χ2或者Fisher确切概率法分析两组的差异。有统计学意义的变量纳入Logistic回归模型进行多因素分析。P < 0.05认为差异有统计学意义。
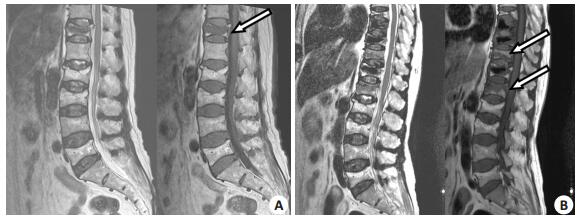
2 结果143例患者中,9例由于术后无法联系到而失访,134例患者获得至少1年随访。其中,胸椎压缩骨折17例,胸腰段压缩骨折96例,腰椎压缩骨折21例,分别占12.7%、71.6%、15.7%,主要发生在胸腰段。随访结束时,116例(86.6%)未发生邻近节段骨折(对照组),18例(13.4%)出现邻近节段骨折(再骨折组)。其中,再骨折患者中12例接受手术治疗,即再次行椎体成形术,术后症状改善。6例接受保守治疗。典型病例如图 3。
|
图 3 1例PVP术后邻近节段骨折的典型病例 Figure 3 A typical case of adjacent segment fracture after percutaneous vertebroplasty. A: T12 osteoporotic compression fracture treated with percutaneous vertebroplasty; B: New fractures in T11 and L1 3 months after treatment. Arrow in A indicates operated segment, and arrows in B indicate adjacent fractured segments. |
比较再骨折组和对照组的年龄、骨水泥量、量体指数,两组差异无统计学意义(P > 0.05)。但是,再骨折组的骨密度显著低于对照组(P < 0.05)。分析两组骨水泥的分布情况,对照组骨水泥的分布指数更高,差异具有统计意义(P < 0.05,表 2)。
| 表 2 再骨折组与对照组临床定量数据的比较 Table 2 Comparison of the quantitative variables between re-fracture and control groups (Mean±SD) |
再骨折组男2例,女16例,对照组男24例,女92例,两组性别比例差异无统计学意义(P > 0.05)。两组均有病例出现骨水泥渗漏,再骨折组8例(44.4%),对照组21例(18.1%),差异具有统计学意义(P=0.026)。比较两组骨水泥的分布情况,两组分布指数的构成比例差异有统计学意义(P < 0.05,表 3)。根据上述单因素分析,筛选出有统计学意义的变量,即骨密度、骨水泥渗漏以及骨水泥分布指数,纳入Logistic回归模型进行多因素分析。结果表明,3种因素均为邻近节段再骨折的危险因素(P < 0.05)。骨水泥渗漏使邻椎骨折的风险增加4倍,骨水泥分布指数越高,邻椎骨折发生的概率越低。骨密度下降1个标准差,邻椎骨折发生的风险增加1倍。
| 表 3 再骨折组与对照组分布指数的比较 Table 3 Comparison of distribution index between re-fracture and control groups |
多年的临床实践表明,PVP是治疗骨质疏松压缩骨折的有效方法。术后患者能够迅速缓解疼痛,早期起床活动,恢复生活自理。但是,术后再发骨折,尤其是邻椎骨折逐渐引起临床医生的重视。初次压缩骨折本身即邻椎骨折的危险因素,一旦发生压缩骨折,其邻椎再骨折的风险将增加2~12.6倍[12-13]。为了进一步研究邻椎骨折的危险因素,我们随访的时间为1年。根据前人的研究,术后1年内邻椎骨折的发生率为19.2% [14],随访一年能够获得适当的阳性事件数量。另一方面,结合临床实际,1年之内患者对随访的依从性较好,能够尽量降低失访率。
本研究中,邻椎骨折的发生率为13.4%,与前人的报道有所差异。Lindsa等[14]随访PVP手术的患者1年后,发现新发骨折的发生率为19.2%。除此之外,其他研究报道的该发生率不尽相同,如7.9%~21.7% [12, 15-17]等。Kim等[3]通过12个月的病例随访,发现51.9%的患者出现邻椎骨折,其中一半的骨折发生在6个月内。但是,这种骨折的发生率并非随着随访时间延长而增加。一项历时2年的随访研究表明术后邻椎骨折的发生率不足20% [18]。这种现象可能源自研究基线的差异,即不同研究之间患者的骨密度、年龄以及压缩骨折的程度不同。另外,本研究评估的是症状性邻近节段骨折,发生影像学改变但是没有疼痛、活动受限等症状的再发骨折不在此列。
骨密度反应骨骼质量,是影响邻椎骨折的重要因素。无论单因素分析,还是Logistic回归,均表明骨密度是邻椎骨折的保护因素。即骨密度越高,邻椎骨折的发生率越低,骨密度每增加一个单位,邻椎骨折的发生率大约降低一半(OR=0.621)。这一点与前人的研究结果类似[19-22]。既往研究也发现,应用促进骨形成药物能够显著改善骨密度,降低新发骨折的发生率[23]。骨骼质量受多因素影响,除了不同的生活水平及营养状况,还包括骨峰值、体重指数以及患者平时的锻炼情况。而且,不同患者存在的医源性因素有所差异,如手术治疗和保守治疗、手术的并发症等。因此,尽管患者的年龄无显著差异,但平均骨密度存在差异,邻近节段骨折的发生率并不相同。这种再骨折的发生可能同时受到医疗干预和骨质疏松自然病程的影响,骨水泥渗漏和分布情况是反映手术干预的因素,骨密度则是自然病程的重要指示变量。无论是否接受手术治疗,更加疏松的椎体结构所耐受的负荷较小,更容易发生骨折。因此,术后积极、规范的抗骨质疏松能够降低再骨折的风险[24]。
骨水泥渗漏是PVP手术常见的并发症,通常发生于椎体中比较薄弱的部位,也可能沿着骨折线渗漏至椎间隙。本研究中,再骨折组骨水泥渗漏的发生率显著高于对照组,表明椎间隙渗漏可能是邻椎骨折发生的危险因素。Joon等[25]的研究也支持这一结论。椎间隙渗漏引起邻椎骨折的机制尚不完全清楚。有人认为椎间盘中的骨水泥类似旋转中心,削弱邻椎终板的强度,限制小关节的活动,进而增加了邻椎骨折发生的风险[2, 16]。根据脊柱功能单位的概念,骨水泥的量和分布模式影响椎体的刚度[26]。从生物力学角度来看,椎间盘内注射骨水泥能够增加邻椎终板的压力,改变相应终板的结构,进而增加邻椎骨折发生的风险。PVP手术改变邻椎的生物力学负荷,增加了整个功能脊柱单位甚至某个区域(如胸腰段或者腰段)的刚度,但是椎间隙渗漏并不增加新发骨折的风险[27-28]。两种不同结论的存在,可能跟骨水泥渗漏的量和位置有关。如果渗漏局限于椎间隙可能对邻椎骨折无明显影响。如果渗漏的骨水泥触及邻位终板,则可能导致其生物力学的改变,进而影响邻椎骨折的发生率。骨水泥渗漏和邻椎骨折的关系有待进一步研究。
骨水泥的分布包括骨水泥的量、形状和相对位置两个方面。由于椎体的大小有所差别,骨水泥的绝对量无法反应其分布情况,我们采用量-体指数反应骨水泥的相对量。但是无论是骨水泥的绝对量还是量-体指数,对邻椎骨折均无显著影响。真实的椎体是不规则的几何形状,为了方便计算量-体指数,我们将椎体近似为椭圆形的圆柱体,可能与事实有所差异,这是本研究的不足之处。为了同时反映骨水泥分布的形状和相对位置,我们将采用骨水泥分布指数量化骨水泥分布的均匀程度。本研究中,我们分别从定性和定量的角度探讨分布指数的影响。定性分析表明再骨折组和对照组之间骨水泥指数具有差异性。定量分析后,发现骨水泥分布越均匀,邻椎再骨折的风险越小。根据Logistic回归分析评价,骨水泥分布指数每升高一级,邻椎骨折发生的风险降低80%,可能是评估再骨折的重要参考指标。
| [1] | Trout AT, Kallmes DF, Kaufmann TJ. New fractures after vertebroplasty: adjacent fractures occur significantly sooner[J]. AJNR Am J Neuroradiol, 2006, 27(1): 217-23. |
| [2] | Kim SH, Kang HS, Choi JA, et al. Risk factors of new compression fractures in adjacent vertebrae after percutaneous vertebroplasty[J]. Asian Spine J, 2004, 45(4): 440-5. |
| [3] | Wang H, Sribastav SS, Ye F, et al. Comparison of percutaneous vertebroplasty and balloon kyphoplasty for the treatment of single level vertebral compression fractures: a meta-analysis of the literature[J]. Pain Physician, 2015, 18(3): 209-22. |
| [4] | Takahara K, Kamimura M, Moriya H, et al. Risk factors of adjacent vertebral collapse after percutaneous vertebroplasty for osteoporotic vertebral fracture in postmenopausal women[J]. BMC Musculoskelet Disord, 2016, 17(12): 12. |
| [5] | 田伟, 韩骁, 刘波, 等. 经皮椎体后凸成形术后骨水泥分布与手术椎体再骨折的关系[J]. 中华创伤骨科杂志, 2012, 14(3): 211-5. |
| [6] | Lin D, Hao J, Li L, et al. Effect of bone cement volume fraction on adjacent vertebral fractures after unilateral percutaneous kyphoplasty[J]. Clin Spine Surg, 2016, 30(3): E270-5. |
| [7] | Zhang H, Xu CY, Zhang TX, et al. Does percutaneous vertebroplasty or balloon kyphoplasty for osteoporotic vertebral compression fractures increase the incidence of new vertebral fractures? a Meta-Analysis[J]. Pain Physician, 2017, 20(1): E13-28. |
| [8] | Yang S, Liu Y, Yang H, et al. Risk factors and correlation of secondary adjacent vertebral compression fracture in percutaneous kyphoplasty[J]. Int J Surg, 2016, 36(Pt A): 138-42. |
| [9] | 中华医学会骨科学分会骨质疏松学组. 骨质疏松性骨折诊疗指南[J]. 中华骨科杂志, 2017, 37(1): 1-10. |
| [10] | Lee KA, Hong SJ, Lee S, et al. Analysis of adjacent fracture after percutaneous vertebroplasty: does intradiscal cement leakage really increase the risk of adjacent vertebral fracture?[J]. Skeletal Radiol, 2011, 40(12): 1537-42. DOI: 10.1007/s00256-011-1139-x. |
| [11] | Zhong BY, Wu CG, He SC, et al. ANVCFV score system: assessment for probability of new vertebral compression fractures after percutaneous vertebroplasty in patients with vertebral compression fractures[J]. Pain Physician, 2015, 18(6): E1047-57. |
| [12] | Syed MI, Patel NA, Jan S, et al. New symptomatic vertebral compression fractures within a year following vertebroplasty in osteoporotic women[J]. AJNR Am J Neuroradiol, 2005, 26(6): 1601-4. |
| [13] | Voormolen MH, Lohle PN, Juttmann JR, et al. The risk of new osteoporotic vertebral compression fractures in the year after percutaneous vertebroplasty[J]. J Vasc Interv Radiol, 2006, 17(1): 71-6. DOI: 10.1097/01.RVI.0000190910.43602.3C. |
| [14] | Lindsay R, Silverman SL, Cooper C, et al. Risk of new vertebral fracture in the year following a fracture[J]. JAMA, 2001, 285(3): 320-3. DOI: 10.1001/jama.285.3.320. |
| [15] | Lin WC, Cheng TT, Lee YC, et al. New vertebral osteoporotic compression fractures after percutaneous vertebroplasty: retrospective analysis of risk factors[J]. J Vasc Interv Radiol, 2008, 19(2 Pt 1): 225-31. |
| [16] | Kim SH, Kang HS, Choi JA, et al. Risk factors of new compression fractures in adjacent vertebrae after percutaneous vertebroplasty[J]. Acta radiol, 2004, 45(4): 440-5. DOI: 10.1080/02841850410005615. |
| [17] | Moon ES, Kim HS, Park JO, et al. The incidence of new vertebral compression fractures in women after kyphoplasty and factors involved[J]. Yonsei Med J, 2007, 48(4): 645-52. DOI: 10.3349/ymj.2007.48.4.645. |
| [18] | Chen WJ, Kao YH, Yang SC, et al. Impact of cement leakage into disks on the development of adjacent vertebral compression fractures[J]. J Spinal Disord Tech, 2010, 23(1): 35-9. DOI: 10.1097/BSD.0b013e3181981843. |
| [19] | Uppin AA, Hirsch JA, Centenera LV, et al. Occurrence of new vertebral body fracture after percutaneous vertebroplasty in patients with osteoporosis[J]. Radiology, 2003, 226(1): 119-24. DOI: 10.1148/radiol.2261011911. |
| [20] | Lee DG, Park CK, Park CJ, et al. Analysis of risk factors causing new symptomatic vertebral compression fractures after percutaneous vertebroplasty for painful osteoporotic vertebral compression fractures: a 4-year follow-up[J]. J Spinal Disord Tech, 2015, 28(10): E578-83. DOI: 10.1097/BSD.0000000000000043. |
| [21] | Seo DH, Oh SH, Yoon KW, et al. Risk factors of new adjacent compression fracture after percutaneous vertebroplasty: effectiveness of bisphosphonate in osteoporotic or osteopenic elderly patients[J]. Korean J Neurotrauma, 2014, 10(2): 86-91. DOI: 10.13004/kjnt.2014.10.2.86. |
| [22] | Yoshii T, Ueki H, Kato T, et al. Severe kyphotic deformity resulting from collapses of cemented and adjacent vertebrae following percutaneous vertebroplasty using Calcium phosphate cement. A case report[J]. Skeletal Radiol, 2014, 43(10): 1477-80. DOI: 10.1007/s00256-014-1912-8. |
| [23] | 杨德鸿, 胡少宇, 孟越, 等. 特立帕肽保守治疗骨质疏松性脊柱骨折: 12例报告[J]. 南方医科大学学报, 2016, 36(3): 414-8. |
| [24] | Chen YC, Lin WC. Can anti-osteoporotic therapy reduce adjacent fracture in magnetic resonance imaging-proven acute osteoporotic vertebral fractures?[J]. BMC Musculoskelet Disor, 2016, 17(151): 151. |
| [25] | Rho YJ, Choe WJ, Chun YI. Risk factors predicting the new symptomatic vertebral compression fractures after percutaneous vertebroplasty or kyphoplasty[J]. Eur Spine J, 2012, 21(5): 905-11. DOI: 10.1007/s00586-011-2099-5. |
| [26] | Yan L, Chang Z, Xu Z, et al. Biomechanical effects of bone cement volume on the endplates of augmented vertebral body: a three-dimensional finite element analysis[J]. Chin Med J (Engl), 2014, 127(1): 79-84. |
| [27] | Lee WS, Sung KH, Jeong HT, et al. Risk factors of developing new symptomatic vertebral compression fractures after percutaneous vertebroplasty in osteoporotic patients[J]. Eur Spine J, 2006, 15(12): 1777-83. DOI: 10.1007/s00586-006-0151-7. |
| [28] | Muto M, Guarnieri G, Giurazza F, et al. What's new in vertebral cementoplasty?[J]. Br J Radiol, 2016, 89(159): 20150337. |
 2017, Vol. 37
2017, Vol. 37
