甲状腺相关性眼病是成年人常见的眼眶疾病之一,通常认为它是一种与甲状腺疾病相关的器官特异性的自身免疫性疾病[1]。目前认为眼眶成纤维细胞可能是主要的效应细胞,可参与脂肪合成、透明质酸形成、趋化因子产生等一系列病理改变[2]。眼球突出是甲状腺相关性眼病(TAO)最主要症状,通常伴随眼睑挛缩、眼睑肿胀、结膜发红等,不仅影响美观,而且威胁视力,严重影响患者的生活质量。
眼球突出由眼眶内容物增多引起,这不仅仅是球后软组织炎症水肿所致,已有多位学者从基础实验及临床影像学指标证实球后脂肪组织体积增加是造成眼球突出最主要的原因[3-6]。国际指南对于中重度活动期TAO患者推荐一线使用糖皮质激素治疗[7],它具有强大的抗炎和免疫调节的作用[8],对于眼部炎症症状疗效明显,但对以脂肪体积增多所致突眼患者疗效欠佳[9],对此类患者而言,尚无有效的内科治疗方法,只能待疾病稳定后选择外科减压术。可见积极探索球后脂肪增长规律及精准测量球后脂肪体积对评估患者治疗时机及预后有重要价值。早期有学者通过测量球后脂肪组织的最大横截面积或眶内侧脂肪厚度等指标评估脂肪组织含量[10-11],但这些指标仅从二维空间测量局部的组织的病变。考虑到体积指标能更全面反应其病理改变,部分学者通过各种软件半自动手工法得到脂肪体积[5, 12],然而,这些测量方法操作复杂,工作量巨大,难以在临床中普及,且上述研究并未阐明球后脂肪体积与临床治疗时机的联系。本研究应用Photoshop软件测量计算球后脂肪体积,该方法可批量处理眼眶磁共振数据,仅需数分钟便可得出结果,且精准度高。为进一步指导临床治疗,本研究利用球后脂肪体积结合现已公认的活动期指标——SIR值[13]及一般临床指标,综合探索TAO的最佳治疗时机,以期改善预后。
1 资料和方法 1.1 一般临床资料连续收集2016年1月~2016年12月在南方医科大学第三附属医院内分泌科门诊及住院部确诊的资料完整的35例(70个眼眶)TAO患者的临床资料。其中男13例,女22例。年龄16~67岁,中位年龄31岁。均为双眼发病者。TAO病程2~140月,中位病程9个月。所有TAO患者均未接受静脉激素治疗。同时募集了12名(24个眼眶)正常志愿者为对照组,其中男性5例,女性7例,年龄24~50岁,中位年龄27岁。所有健康志愿者生命体征及生长发育无异常,无眼部症状及体征。所有受检对象均签署知情同意书。
1.2 观察分析项目 1.2.1 临床症状与体征包括球结膜水肿或发红,眼睑水肿或发红,眼球运动,睑裂宽度,复视情况,视力、视野及眼底情况的检查,眼压,突眼度,视觉诱发电位,眼外观登记照相等。
1.2.2 实验室检查项目甲状腺功能状况,包括FT3(游离三碘甲腺原氨酸)、FT4(游离甲状腺素)、TSH(促甲状腺素)、TRAb(促甲状腺素受体抗体)。
1.2.3 磁共振(MRI)扫描患者及正常志愿者眼眶MRI扫描均采用荷兰飞利浦公司ACHIEVA 1.5T磁共振扫描仪。磁共振扫描软件版本:R 3.2.3。主机操作系统为Windows XP。采用标准头部线圈。患者取仰卧位, 头部置于线圈内,尽可能左右对称,调整颅脑的正中矢状位使其与线圈的纵轴一致,进行眼眶的横断扫描。横断位扫描定位线平行于视神经。扫描序列为:(1)自旋回波(SE)T1WI横断位成像:TR:550 ms,TE:15 ms,视野(field of view, FOV):180 mm×161 mm,扫描层数:12层,层厚3.5 mm,层间距0.35 mm,翻转角:90°,采集矩阵:224×178。采集次数(AC):1。采集时间(TA):2 min28 s;(2)STIR(short-Tau inversion recovery)序列:TR: 2650 ms,TE: 90 ms,层厚3.5 mm。由2名以上影像医师分别阅读MRI图像,对上述测量结果取得一致意见。
1.2.4 球后脂肪测量方法本研究利用商业化软件Adobe Photoshop CC半自动化测量,具体步骤如下:导入Dicom格式T1WI轴位眼眶MRI数据,选择合适画布大小,然后依次调整图像曝光度(0.3~0.9)、位移(0~0.45)以及灰度系数(0.3~1),进一步调整色阶(阴影输入色阶40~150,高光输入色阶90~200),并结合手动勾选半自动化获到脂肪组织,最后由软件计算出每层球后脂肪组织面积,逐层相加乘以层厚即得体积。本团队前期通过采集TAO患者眼眶和已知体积脂肪模具MRI图像使用该方法进行测量验证,测量时间约5~10 min,所测的体积与其已知真实体积相对误差在1%以内,处于可接受范围内,因此该方法操作相对简便,耗时较短,精准度高。
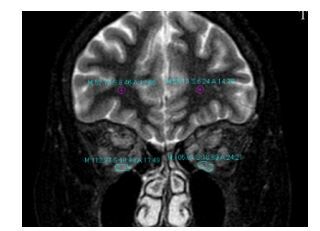
1.2.5 SIR值测量方法在STIR序列冠状位分别测量眼外肌T2值,多条眼外肌病变者,以信号最强者为代表。同时在冠状位选取距离眼眶后极约2 cm处测量同侧脑白质信号值(图 1),眼外肌最高信号值与脑白质比值即为SIR值。
|
图 1 眼外肌T2信号值及脑白质信号值 Figure 1 T2 values of the extraocular muscles and white matter. |
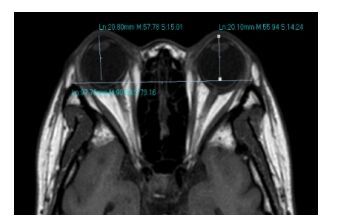
在T1WI序列视神经轴层面,以双侧角膜前缘与双侧颧弓连线的垂直距离即为眼球突出值(图 2)。
|
图 2 在T1WI序列测量眼球突出度 Figure 2 Degree of exophthalmus measured in T1WI sequence. |
本组病例TAO诊断标准参照2016年EUGOGO指南推荐[9]根据典型临床特征、甲状腺功能确诊,排除颅内及其他眼眶疾病。
1.3.2TAO活动性评估采用2016年EUGOGO指南推荐通过CAS评分来测量,CAS≥3分时,是TAO活动的标志。
1.4 本研究采用IBMSPSS 20统计软件进行分析其中计量资料采用均数±标准差表示。计数资料用阳性例数或率表示。符合正态分布且方差齐的计量资料,采用两独立样本t检验,不符合正态分布的比较采用非参数Mann-Whitney U检验。TAO临床指标与眼眶MRI指标相关分析,采用Spearman秩相关。对于正态分布及方差齐的多组资料间比较采用One-Way ANOVA检验,组间多重比较采用LSD法。采用线性回归分析变量线性数量关系。以P<0.05为差异有统计学意义。
2 结果 2.1 一般结果35例(70个眼眶)TAO患者中18例(36个眼眶)患者CAS≥3分(活动组),17例(34个眼眶)患者CAS<3分(非活动组),两组患者的性别比例无明显差异,平均年龄的差异不具有统计学意义(P=0.925)。活动组CAS评分显著高于非活动组(P=0.000)。活动组SIR值显著高于非活动组(P=0.000)。活动组突眼度高于非活动组(P=0.046)。两组脂肪体积无明显差异。实验室检查项目中除TRAb活动组显著高于非活动组外(P=0.012),其余各项检验值无统计学差异(表 1)。
| 表 1 TAO患者一般资料 Table 1 Characteristics of 35 consecutive TAO patients |
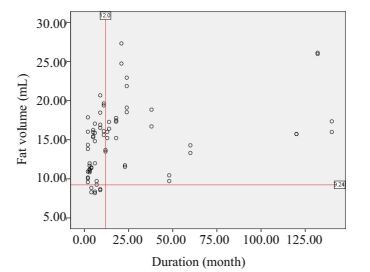
本研究中采用临床易获取的两项影像学指标——脂肪体积及SIR值分析其与临床各项指标的相关性,结果表明脂肪体积与病程有相关性(r=0.480,P<0.01),脂肪体积与突眼度存相关性(r=0.622,P<0.01),脂肪体积与其余各项临床指标均无相关性。SIR值与CAS评分存在相关性(r=0.536,P<0.01),该指标与其余各项临床指标均无相关性(表 2)。除此之外,CAS评分与TRAb存在正相关(r=0.416,P<0.01,图 3~6)。
| 表 2 影像学相关指标与TAO临床指标相关性 Table 2 Correlation between the imaging indexes and clinical parameters of the patients with TAO |
|
图 3 病程与脂肪体积相关性散点图 Figure 3 Scatter plot showing the correlation between disease course (cutoff point of 1 year)and orbital fat volume. |
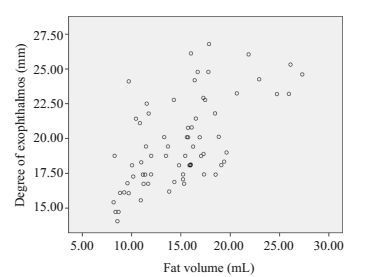
|
图 4 突眼度与脂肪体积相关性散点图 Figure 4 Scatter plot showing the correlation between orbital fat volumes and the degree of exophthalmos. |
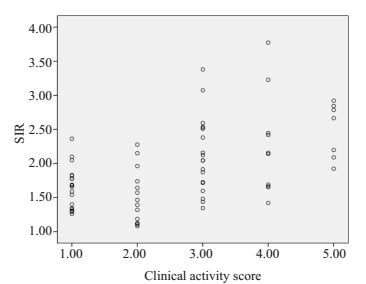
|
图 5 SIR值与CAS相关性散点图 Figure 5 Scatter plot showing the correlation between the CAS and the SIR(r=0.536, P < 0.01) |
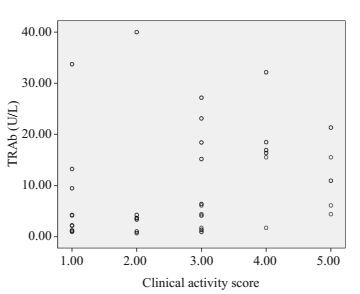
|
图 6 TRAb值与CAS相关性散点图 Figure 6 Scatter plot showing the correlation between the CAS and the TRAb. |
通过线性回归统计可得y=0.88x-2.344,(y代表球后脂肪体积,x代表突眼度)。即突眼度每增加1 mm,球后脂肪体积将增加0.88 mL(图 7)。
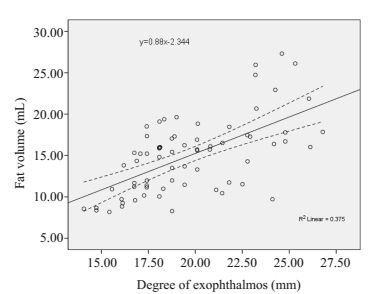
|
图 7 TAO患者脂肪体积与突眼度线性回归散点图 Figure 7 Scatter plot with a linear regression line between exophthalmos and FV in TAO. The dashed lines represent the 95% confidence interval. |
以病程作为分组条件将患者分为3组,6个月以内组患者球后脂肪体积为12.49±2.90 mL;6~12个月组球后脂肪体积14.76±4.28 mL;大于12个月组球后脂肪组织体积17.52±4.63 mL。通过方差分析可得3组球后脂肪体积存在显著差异(P<0.01)。3组组间脂肪体积比较显示病程6个月以内组与6~12个月组相比,差异不具有统计学意义(P=0.084)。其余各组差异显著。正常组球后脂肪体积为9.24±2.04 mL,TAO组明显高于正常组(P<0.01,图 8)
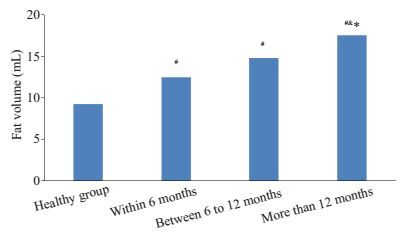
|
图 8 不同病程TAO组与正常组球后脂肪体积的比较 Figure 8 Comparison of orbital fat volumes between TAO patients with different disease courses and healthy subjects.#P < 0.01 vs healthy group; & P < 0.01 vs within 6 months groups; *P < 0.05 vs 6 to 12 months groups. |
TAO是一种多因素且发病机制复杂的疾病。多年来大量研究者们均致力于从各方面寻找其发病机制,但至今仍未得到统一的认识。早期的研究将眼眶成纤维细胞及炎症细胞、细胞因子导致的眶内自身免疫性炎症反应作为研究重点,对它们在发病过程中的作用已有一定的探究[2, 14]。但近年来有研究认为,患者主要临床表现之—眼球突出,主要是由于球后脂肪组织体积增大所致,因而脂肪细胞成了近期研究的热点。目前,从分子基因及细胞层面均有研究证实了在TAO患者中脂肪从头合成是显著增加[15-16]。同时,多位学者利用眼眶MRI及计算机断层扫描(CT)技术定量测量球后软组织的形态改变[10-11, 17-18],同样提示TAO患者球后脂肪含量的增加。既往研究是通过逐层勾画眼眶及眼球、视神经及眼外肌轮廓得出每层面积,再乘以层厚和层数得出体积,最后利用眼眶体积减去眼球等体积得到球后脂肪体积,这些测量方法操作复杂、繁琐,误差较大,难以在临床中推广。
本研究采用Photoshop软件测量球后脂肪体积,该方法智能化程度高,操作简便,通过比较35名(70个眼眶)TAO患者与12名(24个眼眶)健康人的球后脂肪体积,证实TAO组显著高于健康对照组(P<0.01)。Peyster等[19]学者计算正常人单侧球后脂肪体积约为8.16 mL,TAO患者单侧球后脂肪体积约为9.60~12.53 mL。蒋丽琼等[17]测量正常人球后脂肪组织手工方法所得为8.8 mL,半自动方法所得为8.7 mL;TAO患者球后脂肪组织手工方法所得为12.6 mL,半自动方法所得为13.1 mL。本研究结果与已有研究基本相符。
此外,本研究发现球后脂肪体积与病程成正相关(r=0.480)。我们考虑有以下两个原因:第一,目前研究证据显示眼眶成纤维细胞是甲状腺相关眼病的主要效应细胞。眼眶成纤维细胞可分为成肌纤维细胞和成脂纤维细胞,根据其表面是否表达糖蛋白Thy-1,可将其分为表达Thy-1(Thy-1 +)型,和不表达Thy-1(Thy-1-)型。分化为眼外肌的成肌纤维细胞仅表达Thy-1(Thy-1+),分化为脂肪组织的成脂纤维细胞表现为Thy-1+和Thy-1-的双峰表达。然而只有Thy-1-的成纤维细胞有能力分化为成熟脂肪细胞。但Thy-1+成纤维细胞产生炎症因子的能力高于Thy-1-[20]。所以,脂肪生成过程主要出现在脂肪组织,而眼外肌组织通常表现为炎症反应。根据经典的朗德尔曲线可知疾病早期为炎症活动阶段,因此眼外肌体积的增大将提早于球后脂肪组织体积的改变。第二,疾病早期主要以Th1淋巴细胞占主导,主要介导细胞免疫;疾病后期以Th2淋巴细胞为主,主要介导体液免疫[21]。对于TAO而言,体液免疫主要针对TSH受体生成抗体,而伴随脂肪生成的过程中TSH受体表达增加[22],且根据相关研究显示在球后脂肪组织以Th2淋巴细胞占主导[23],所以可以推断脂肪生成出现在疾病的后期。
我们进一步以病程作为分组的标准将TAO患者分为病程6月以内、病程6~12月、病程大于12月3组,根据组间多重比较的结果显示,3组患者的球后脂肪体积呈阶梯状上升。病程6月以内组和病程6~12月组球后脂肪体积差异不显著,但病程6~12月组和病程大于12月组球后脂肪体积差异明显(P<0.05)。且病程6月以内组和病程大于12月组球后脂肪体积差异显著(P<0.01)。这提示病程1年左右是球后脂肪体积增高的高峰阶段,而该阶段静脉糖皮质激素治疗疗效欠佳。所以,我们应当重视发病1年这个时间切点,在发病1年以内积极激素治疗,抑制成纤维细胞活性,减轻球后脂肪增生,避免突眼加重。
在本研究中TAO患者球后脂肪体积与突眼度相关性强。通过回归方程我们进一步得出突眼度每增加1 mm,球后脂肪体积将增加0.88 mL。该结果进一步证实脂肪体积的增加是造成突眼度的增长的重要因素。
本研究观察到SIR值与CAS具有相关性(r=0.536),早在1989年Hosten等[24]通过测量Graves眼病患者眼外肌T2弛豫时间发现眼外肌的炎症水肿,并且发现CAS与T2值之间存在正性相关性。本研究采用STIR序列可以更好地反映眼外肌水肿和炎症状态等病理信息,且SIR值(眼外肌T2值与同侧脑白质T2值之比)与T2绝对值相比更加客观,克服了患者年龄及性别的差异。目前国内外大多数研究均以同侧颞肌作为参照组织[18],但在STIR序列上颞肌显影不佳,难以识别,而利用脑白质作为参照组织则解决上述难题。Micha等[13]对比了颞肌及脑白质作为参照组织的优劣,认为脑白质组织均一性高,且在MRI上可视范围广,易于选取,是利于临床应用的参照组织。此外TRAb与CAS之间存在中等相关(r=0.416)。TRAb是一种多克隆抗体,可特异性结合促甲状腺素受体,它是Graves病和TAO的共同抗原,众多研究也证实TRAb与CAS之间具有相关性[25]。但在本研究中尚未证实TRAb与SIR值的相关性,仍需进一步增加样本量探索两者的关系。以上结果提示SIR值及血清TRAb可作为活动期激素治疗时机的可靠指标。
然而,本研究还存在不足之处,首先,测量球后脂肪组织体积应用的MRI数据层厚相对较厚,为3.5 mm,所得球后脂肪体积存在一定偏差,本研究团队正进行相关研究探索精准体积修正系数,以得到更加精准的真实体积。其次,本研究样本量较少,仍需进一步完善患者随访资料。最后,本研究仅初步观察到TAO患者和正常人群球后脂肪体积差异的趋势,仍需进一步研究,找到确切激素治疗时机的切点。
综上所述,球后脂肪体积可以更加全面反应脂肪组织的病变,脂肪体积增多与突眼度及病程成正相关,病程1年以上是球后脂肪生成的高峰阶段,常提示预后欠佳,应把握1年以内的最佳治疗时机。SIR值及TRAb含量与CAS相关,可作为活动期积极激素治疗的指标。结合球后脂肪体积及SIR值综合选择治疗时机有望作为一个重要依据来指导临床医师对于TAO患者的诊疗并预测其预后。
| [1] | Khong JJ, Mcnab AA, Ebeling PR, et al. Pathogenesis of thyroid eye disease: review and update on molecular mechanisms[J]. Br J Ophthalmol, 2016, 100(1): 142-50. DOI: 10.1136/bjophthalmol-2015-307399. |
| [2] | Dik WA, Virakul S, Van Steensel L. Current perspectives on the role of orbital fibroblasts in the pathogenesis of Graves' ophthalmopathy[J]. Exp Eye Res, 2016, 142: 83-91. DOI: 10.1016/j.exer.2015.02.007. |
| [3] | Potgieser PW, Wiersinga WM, Regensburg NI, et al. Some studies on the natural history of Graves' orbitopathy: increase in orbital fat is a rather late phenomenon[J]. Eur J Endocrinol, 2015, 173(2): 149-53. DOI: 10.1530/EJE-14-1140. |
| [4] | Wiersinga WM, Regensburg NI, Mourits MP. Differential involvement of orbital fat and extraocular muscles in graves' ophthalmopathy[J]. Eur Thyroid J, 2013, 2(1): 14-21. DOI: 10.1159/000348246. |
| [5] | Nishida Y, Tian S, Isberg B, et al. Significance of orbital fatty tissue for exophthalmos in thyroid-associated ophthalmopathy[J]. Graefes Arch Clin Exp Ophthalmol, 2002, 240(7): 515-20. DOI: 10.1007/s00417-002-0498-3. |
| [6] | Khong JJ, Wang LY, Smyth GK, et al. Differential gene expression profiling of orbital adipose tissue in thyroid orbitopathy[J]. Invest Ophthalmol Vis Sci, 2015, 56(11): 6438-47. DOI: 10.1167/iovs.15-17185. |
| [7] | Bartalena L, Baldeschi L, Boboridis K, et al. The 2016 European thyroid association/European group on graves' orbitopathy guidelines for the management of graves' orbitopathy[J]. Eur Thyroid J, 2016, 5(1): 9-26. DOI: 10.1159/000443828. |
| [8] | 李静, 马建民. 糖皮质激素在眼眶病中的应用及研究进展[J]. 临床眼科杂志, 2014, 22(04): 372-8. DOI: 10.3969/j.issn.1006-8422.2014.04.028. |
| [9] | Higashiyama T, Nishida Y, Ohji M. Changes of orbital tissue volumes and proptosis in patients with thyroid extraocular muscle swelling after methylprednisolone pulse therapy[J]. Jpn J Ophthalmol, 2015, 59(6): 430-5. DOI: 10.1007/s10384-015-0410-4. |
| [10] | Kim HC, Yoon SW, Lew H. Usefulness of the ratio of orbital fat to total orbit area in mild-to-moderate thyroid-associated ophthalmopathy[J]. Br J Radiol, 2015, 88(153): 20150164. |
| [11] | 陈燕萍, 林志春, 沈洁, 等. MRI眶内结构定量分析在Graves眼病的应用研究[J]. 临床放射学杂志, 2007, 26(4): 336-40. |
| [12] | Rha EY, Kim JM, Yoo G. Volume measurement of various tissues using the image J software[J]. J Craniofac Surg, 2015, 26(6): e505-6. DOI: 10.1097/SCS.0000000000002022. |
| [13] | Pająk M, Loba P, Wieczorek-Pastusiak J, et al. Signal intensity and T2 time of extraocular muscles in assessment of their physiological status in Mr imaging in healthy subjects[J]. Pol J Radiol, 2012, 77(4): 7-12. DOI: 10.12659/PJR.883622. |
| [14] | Shen J, Li Z, Li W, et al. Th1, Th2, and Th17 cytokine involvement in thyroid associated ophthalmopathy[J]. Dis Markers, 2015(2015): 609593. |
| [15] | Kumar S, Coenen MJ, Scherer PE, et al. Evidence for enhanced adipogenesis in the orbits of patients with Graves' ophthalmopathy[J]. J Clin Endocrinol Metab, 2004, 89(2): 930-5. DOI: 10.1210/jc.2003-031427. |
| [16] | Kumar S, Leontovich A, Coenen MJ, et al. Gene expression profiling of orbital adipose tissue from patients with Graves' ophthalmopathy: a potential role for secreted frizzled-related protein-1 in orbital adipogenesis[J]. J Clin Endocrinol Metab, 2005, 90(8): 4730-5. DOI: 10.1210/jc.2004-2239. |
| [17] | 蒋丽琼, 何小寒, 刘桂琴, 等. 利用ImageJ软件测量眼眶脂肪体积[J]. 中国CT和MRI杂志, 2016, 14(03): 11-3. DOI: 10.3969/j.issn.1672-5131.2016.03.004. |
| [18] | Szucs-Farkas Z, Toth J, Kollar J, et al. Volume changes in intra-and extraorbital compartments in patients with Graves' ophthalmopathy: effect of smoking[J]. Thyroid, 2005, 15(2): 146-51. DOI: 10.1089/thy.2005.15.146. |
| [19] | Peyster RG, Ginsberg F, Silber JH, et al. Exophthalmos caused by excessive fat: CT volumetric analysis and differential diagnosis[J]. AJR Am J Roentgenol, 1986, 146(3): 459-64. DOI: 10.2214/ajr.146.3.459. |
| [20] | Smith TJ, Koumas L, Gagnon A, et al. Orbital fibroblast heterogeneity May determine the clinical presentation of thyroid-associated ophthalmopathy[J]. J Clin Endocrinol Metab, 2002, 87(1): 385-92. DOI: 10.1210/jcem.87.1.8164. |
| [21] | Aniszewski JP, Valyasevi RW, Bahn RS. Relationship between disease duration and predominant orbital T cell subset in Graves' ophthalmopathy[J]. J Clin Endocrinol Metab, 2000, 85(2): 776-80. |
| [22] | Starkey KJ, Janezic A, Jones G, et al. Adipose thyrotrophin receptor expression is elevated in Graves' and thyroid eye diseases ex vivo and indicates adipogenesis in progress in vivo[J]. J Mol Endocrinol, 2003, 30(3): 369-80. DOI: 10.1677/jme.0.0300369. |
| [23] | Hiromatsu Y, Yang D, Bednarczuk T, et al. Cytokine profiles in eye muscle tissue and orbital fat tissue from patients with thyroid-associated ophthalmopathy[J]. J Clin Endocrinol Metab, 2000, 85(3): 1194-9. |
| [24] | Hosten N, Sander B, Cordes M, et al. Graves ophthalmopathy: Mr imaging of the orbits[J]. Radiology, 1989, 172(3): 759-62. DOI: 10.1148/radiology.172.3.2772184. |
| [25] | 吴娜, 孙丰源, 李佳, 等. 甲状腺相关眼病患者血清TRAb, TPOAb, TGAb水平变化及意义[J]. 山东医药, 2015, 55(30): 59-60. DOI: 10.3969/j.issn.1002-266X.2015.30.025. |
 2017, Vol. 37
2017, Vol. 37

