2. 福建医科大学药学院, 福建 福州 350122
2. School of Pharmacy, Fujian Medical University, Fuzhou 350108, China
肿瘤是一类严重危害人类生命健康的疾病,其发生、侵袭生长和转移是一种复杂的病理生理过程,其中肿瘤组织中新生血管的生成是肿瘤发生、浸润与转移的重要因素之一[1-2]。血管内皮生长因子(VEGF)是血管内皮细胞特异性的肝素结合生长因子,可在体内诱导血管新生,并可作用于血管内皮细胞促进血管内皮细胞增殖,增加血管通透性,与肿瘤的生长和血行转移有着密切的联系[3]。因此,检测人体内的VEGF水平对肿瘤的监测、治疗、预后等具有重要的意义。然而,目前主要应用于VEGF等蛋白肿瘤标志物的检测方法[4-8]仍存在一些不足,需要继续寻找开发具备简单、经济、灵敏的检测新技术。
近年来,核酸适体的发现使得抗体—抗原反应研究有了历史性突破,为传统免疫检测技术的发展开辟了一条新的道路。核酸适体[9](Aptamer)是通过指数富集配体系统进化技术(SELEX)经体外筛选得到的寡聚核苷酸,它是一种寡聚单链DNA或RNA,具有类似抗体的功能,能识别特异性的靶分子。核酸适体因其具有亲合力高,化学性质稳定,制备周期短,成本低等优点,已被用作抗体的替代识别元件,广泛的应用于检测技术和诊断试剂中[10-11]。其中,就有研究者利用核酸适体独特的性质,开发了用于检测肿瘤标志物VEGF的检测技术[12-16]。虽然这些方法能够得到较好的灵敏度和选择性。然而它们都还存在一定的缺陷,比如有些需要经过复杂的操作步骤,有些结果需要大型的仪器分析以及存在假阳性和假阴性的现象等。为克服这些问题,本研究根据前人研究报道,选择合适的VEGF核酸适体2G19[17],以磁珠为载体,并利用脲酶水解尿素可使溶液pH值发生变化从而使酚红的颜色发生不同程度变化的原理,构建了一种新颖的比色检测技术,可实现VEGF的灵敏检测。本研究不仅可以实现肉眼检测,还可以应用pH计来进行测定,这不仅扩展了pH计的应用范围,也为以后研制便携式的检测器提供参考价值。此外,本研究也为临床肿瘤的监测、治疗、预后等提供依据。
1 材料和方法 1.1 仪器紫外分光光度仪(UV-2450型,日本岛津(苏)制);微型离心机(Mini-6K型,常州迈科诺仪器有限公司);超声波清洗器(KQ116型,昆山市超声仪器公司);电子天平(Sartorius BS124S 型,北京赛多利斯仪器有限公司);pH 计(UB-7 型,美国丹佛仪器公司);涡旋仪(L-866,海门市其林贝尔仪器有限公司)。
1.2 试剂酚红购自国药集团化学试剂有限公司;链霉亲和素修饰的磁珠(MBs)购自Dynal Biotech ASA.(Oslo,Norway);VEGF165 购自R&D Systems 中国公司。5'-CTGGCCAGgTACCAAAAGaTGATCTTGGGCCCGTCCGAATGGTGGGTGTTCTGGCCAG-biotin-3',5'-NH2-ATCTTTTGGTAGCTGGCCAG-3',脲酶均购自大连宝生物技术有限公司。溶液:TE缓冲液(10 mmol/LTris-HCl,100 mmol/LNaCl,0.05 mmol/L EDTA,pH 7.0),底物液(2 mol/L NaCl,60 mmol/L MgCl2,50 mmol/L尿素,1 mmol/L HCl,pH 5.5),配制上述溶液的试剂Tris、NaCl、MgCl2、EDTA、HCl、尿素均购自国药集团化学试剂有限公司。血样标本来自福州市第一医院。实验用水均为Millipore Milli-Q系统纯化的超纯水(18.2 MΩ/cm);其它试剂均为分析纯。
1.3 方法 1.3.1 脲酶标记单链的制备将3.2 μL 6.4 mmol/L的马来酰亚胺基苯甲酸N-羟基琥珀酰亚胺酯(MBS)与10 μL100 μmol/L的单链DNA混合并稀释至100 μL,室温下反应1 h。将混合物通过截流相对分子质量为3 000 000的柱膜过滤,以除去未结合的MBS。用50 μL的TE缓冲液洗涤3次,并分散在100 μL的TE缓冲液中,继续加入1 mL 3.3 μmol/L的脲酶溶液,室温下反应1 h。将反应液通过300 000的截流离心柱过滤,50 μL的TE缓冲液洗涤3次,最后分散在100 μL的TE缓冲液中,4 ℃储存备用。
1.3.2 检测体系的建立量取100 μL 1 mg/mL的链霉亲和素修饰的磁珠置于2 mL的离心管中,用100 μL TE缓冲液洗涤3次,分散在含100 pmol生物素修饰适体和150 pmol/L 脲酶标记单链的100 μL的TE缓冲液中。37 ℃条件下,孵化2 h,单链与适体杂交并吸附到磁珠上,在磁铁作用下,用TE缓冲液洗涤复合物3次,以去除没有结合的适体和单链,最后重新分散在100 μL的TE缓冲液中,4 ℃储存备用。
1.3.3 检测将一定量的待测VEGF样品加入上述溶液中,37 ℃条件下,孵化1 h。将反应溶液置于磁场下,移取70 μL上清液,加入到含100 μL 50 mmol/L的尿素底物液和10 μL 0.04%的酚红试剂的试管中(初始pH 5.5),混匀稀释至1.1 mL,反应10 min。
1.3.4 结果分析用肉眼或紫外分光光度计对实验结果进行分析,计算λ=560 nm处的紫外吸收峰值对待测VEGF进行间接测定。
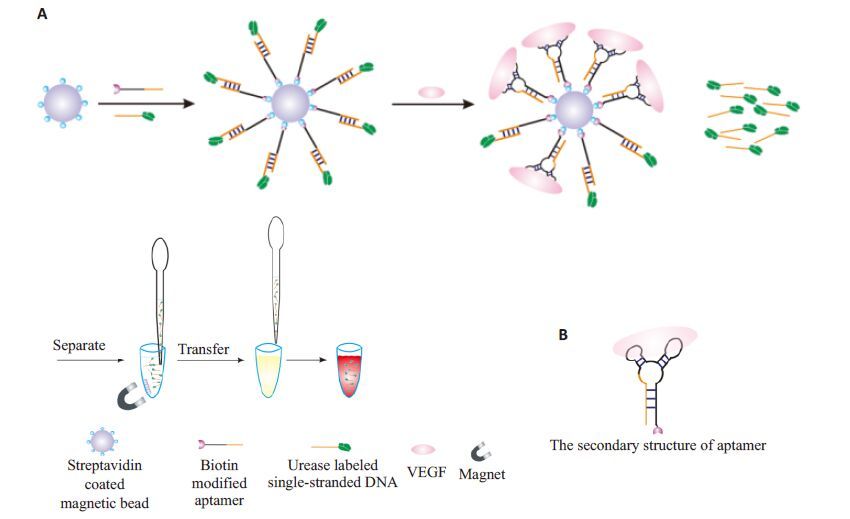
2 结果 2.1 比色方法的检测原理本文以酚红作为指示剂,研制用于VEGF检测的比色方法。图 1 为该方法的检测原理图:筛选出特异的VEGF适体,在其一端修饰生物素,另一端与标记脲酶的单链DNA结合,通过生物素-亲和素的特殊识别作用固定在链霉亲和素修饰的磁珠上。当VEGF存在时,适体与其结合形成2个茎环结构(图 1B),使得标记脲酶的单链DNA从适体上释放出来。经磁分离,取适量上清液,加入到含一定量的尿素和酚红试剂的底物液中。上清液中的脲酶水解尿素产生氨,使得溶液的pH值升高,导致酚红的颜色由黄色变为红色。由此,通过溶液颜色的改变以及其紫外吸收的变化来实现VEGF的灵敏检测。
|
图 1 肿瘤标志物VEGF检测反应原理示意图 Figure 1 Schematic illustration of the colorimetric method for VEGF detection. A: Flow chart of the proposed sensor; B: The secondary structure of aptamer |
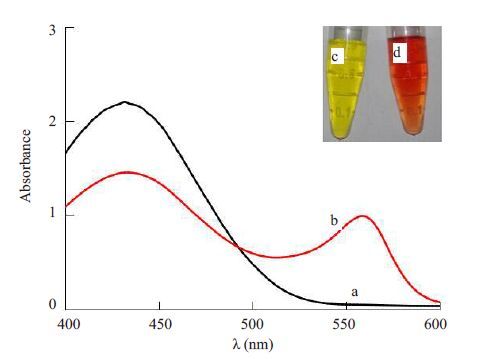
用紫外法验证方法的可行性。结果如图 2所示,当体系中不存在VEGF时,酚红的底物液只在λ=430 nm出现一较强的紫外吸收峰(图 2a),且溶液的颜色是黄色(图 2c)。但是当体系中加入一定量的VEGF后,经磁分离,转移出的上清液可使酚红底物液的颜色由黄色变为红色(图 2d),而λ=430 nm处的紫外吸收峰值降低且在λ=560 nm处出现了新的吸收峰(图 2b)。实验结果表明,该检测策略可以实现对VEGF的灵敏检测。
|
图 2 方法的可行性分析 Figure 2 Feasibility analysis of the proposed sensor based on UV spectral characterizations before (a) and after (b) the addition of VEGF. The inset shows the difference in the colors of the solution before (c) and after (d) the addition of VEGF. |
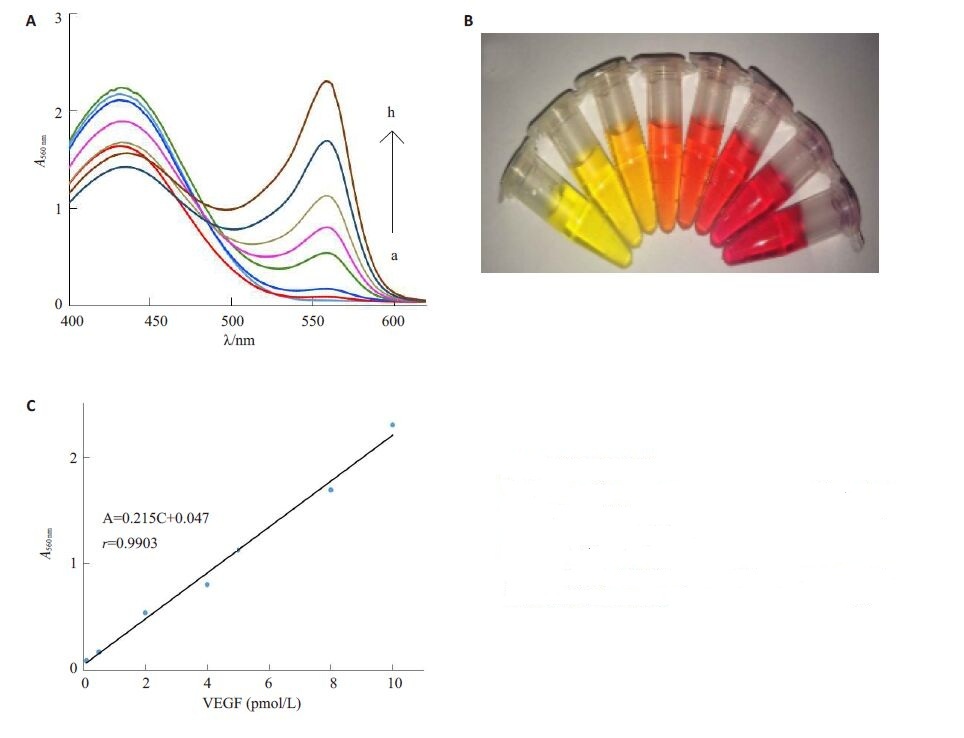
将不同浓度的VEGF(0.1,0.5,2,4,5 ,8,10 pmol/L)加入到体系中,分别测定其酚红的紫外吸收值变化,并绘制标准曲线。如图 3所示,体系在λ=560 nm处的紫外吸收峰随VEGF浓度的增加而逐渐增强(图 3A),且溶液颜色也随VEGF浓度的增加而由黄色渐变为红色(图 3B)。VEGF浓度(C)在0.1~10 pmol/L范围内,体系的紫外吸收与其浓度呈良好的线性关系(图 3C)。线性方程为A=0.215C-0.047,r=0.9903,检测限达0.06 pmol/L。通过平行测定8组5 pmol/L VEGF来评估该检测体系的重现性,相对标准偏差(RSD)为2.89%。
|
图 3 方法的线性研究 Figure 3 Linearity of the results of VEGF detection using the proposed sensor. A: UV curves for different VEGF concentrations (a-h: 0, 0.1, 0.5, 2, 4, 5, 8, and 10 pmol/L, respectively); B: Color changes of the solution for the corresponding VEGF concentration; C: Relationship between VEGF concentrations and absorbance values. |
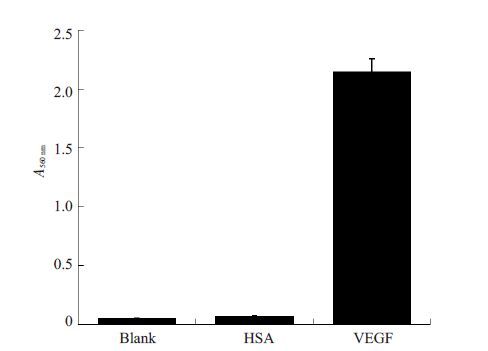
为了考察方法的选择性。在相同实验条件下,分别往体系中加入相同浓度的HSA和VEGF(5 pmol/L)进行紫外吸收光谱测量,并做空白对照。如图 4所示,在加入VEGF后表现出显著的紫外吸收,而空白和HSA只产生很弱的紫外吸收,几乎可以忽略不计。表明该方法对VEGF的检测具有较好的选择性。
|
图 4 HSA和VEGF检测以及空白的紫外吸收 Figure 4 UV absorption in samples spiked with HAS (5 pmol/L) and VEGF (5 pmol/L) and in the blank sample detected with this system. |
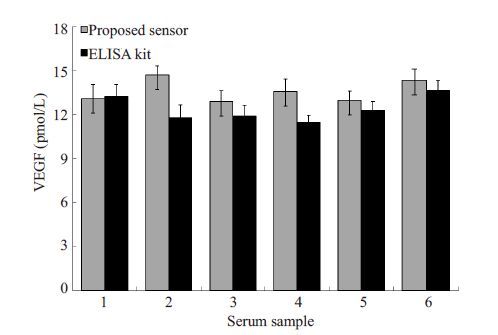
为了验证该方法是否可用于实际复杂生物样品中的VEGF浓度的检测。本实验选择6例人肺癌血清样本,如图 5所示,用本方法检测出的人肺癌患者血清中的VEGF浓度与ELISA方法检测出的结果基本一致,说明该方法的准确性较高,在临床VEGF检测中具有潜在的应用前景。
|
图 5 本方法和ELISA方法测定血清样本中VEGF的浓度 Figure 5 VEGF concentrations in serum samples detected by the aptamer-based method and ELISA. |
采用同步盲法。分别采用本方法和ELISA方法同步盲法对10例血清样本中的VEGF含量进行测定,并进行临床性能比对。结果如表 1所示,从两种方法所测定的结果可以看出,只有1例血清检测结果的数据相差较大,其他几乎一致,说明本方法有较高的有效性和敏感性,其准确率为90%,具有临床参考价值。
| 表 1 两种方法检测VEGF的结果 Table 1 Results of VEGF detection using two methods (pmol/L) |
核酸适体是一系列单链核酸分子,可以是DNA也可以是RNA,具有类似抗体的功能,能特异结合蛋白质或其他小分子物质,具有严格的识别能力和高度的亲和力[18-19]。与抗体相比,核酸适体具有更多的优势,比如一旦被筛选出就可以大量合成,而且筛选周期短,批次间无差别;对温度变化不敏感,易于存储;化学修饰简单等。所以,核酸适体是成为最具前景的抗体替代品,已被广泛地应用于生物领域[20-21]。众所周知的,指数富集配体系统进化技术是筛选核酸适体的最有效方法,可以筛选获得多个特异性结合较强的适体。有研究发现,形成多个茎环结构的多价核酸适体比以单链形式与靶标结合的适体具有更大的优势,它可以改善多价分子间即茎环间的相互作用力以显著提高分子识别元件的性能[22-23]。核酸通过化学或者杂交作用可以很容易地形成多价结构,从而改善核酸适体的亲和性。本研究根据文献报道[17],对其4种多价核酸适体2G19、2G19-二价、SL5-二价、SL5-三价进行筛选,确定了适体2G19为本策略的最佳核酸适体,可以有效提高VEGF的检测灵敏度。这可能是由于适体识别VEGF形成2个茎环结构(图 1B),使得结合更加稳定,检测效果更好。
本研究引入磁珠微纳米技术,可使检测技术进一步微型化、集成化与自动化,减少其对实验者的技术要求。生物磁珠是一种内含纳米磁性粒子的高分子微球,具有粒径小、表面积大、偶联容量高、悬浮稳定性好等特点,可用作分析物的载体,其大的表面积有效提高定量分析的灵敏度[24];也可在其表面修饰不同的识别元件,以其特殊的生物亲和性来捕获不同的靶标分子[25]。更甚者,可利用磁场控制磁珠,使体系中的靶分子与干扰物质分离,实现靶标的灵敏选择性检测。本研究通过对磁珠的加入量进行优化,确定了10 μmol/L适体溶液中最佳磁珠用量是0.1 mg/mL。磁珠表面捕获适体探针的覆盖度,对体系检测的灵敏度影响很大。磁珠用量少,覆盖度过高,适体过于密集会影响适体与VEGF的结合,从而使单链不能从适体上脱落,导致检测信号降低,造成漏诊;磁珠用量多,覆盖度过低,会产生非特异吸附作用,造成误诊。本研究对磁珠加入量进行梯度优化,从而确定了其最佳用量。
本研究所采用的显色方法是根据溶液pH的变化使得酚红的颜色发生改变来判断VEGF的存在与否以及含量多少。释放出的脲酶,可水解尿素产生氨,使得溶液的碱性增强,从而导致酚红的颜色发生变化。尽管“大中心、大检验”的传统方法具有一定的优势,但其存在操作繁琐,易受环境因素的干扰,假阳性和假阴性的现象仍不可避免等局限性,阻碍了这些技术在实际生活中的推广应用。而且,目前基于核酸适体的比色技术主要是使用辣根过氧化物酶来进行显色测定的,本研究则是利用脲酶水解尿素,产生pH值的改变来达到颜色变化,也就是说我们的方法也可以应用pH计来实现检测,这不仅扩展了pH计的应用范围,也为以后研制便携式的检测器提供参考价值。本研究中核酸适体不仅具有抗体的特殊识别功能,而且性质较稳定。其次磁珠作为载体,其大的比表面积可标记大量的核酸适体,从而增大与待测VEGF的结合率,继而增强检测信号。而且,表面固定适体和脲酶的磁珠在磁场作用下可与未结合到磁珠表面的适体和脲酶单链分离开来,减少假阳性的发生;VEGF存在时,适体上结合的脲酶标记单链脱落到溶液中,经磁场作用,与磁珠分离,进一步减少假阳性的发生。最后,采用pH值变化的酚红显色方法可以非常方便地观察检测结果及分析其检测信号。
本研究通过盲法检测,考察本方法检测结果对比ELISA方法的准确性及可比性。结果显示,本方法的准确率为90%,说明本方法具有临床应用价值。众所周知,ELISA方法是采用抗原与抗体的特异反应来实现目标物的检测,具有操作简单、敏感性高、半微量、超微量定量分析等优点。然而,ELISA方法也存在一定的缺陷,比如使用的抗体易受温度影响,容易变性,储存时间短;易受其他物质干扰,导致结果的假阳性和假阴性等。而本方法具有更高的灵敏度;所使用核酸适体结构稳定,易于储存。虽然目前核酸适体的应用还不成熟,但是相信随着研究工作的不断深入,方法的不断改进,这种核酸适体分析技术将更好地应用于临床中。
总之,本研究筛选合适的核酸适体,以磁珠为载体,以酚红为指示剂,利用溶液pH值的变化从而使酚红的颜色发生不同程度变化的原理,构建了一种新颖的比色检测技术,实现对VEGF进行可视化的灵敏检测;同时,本研究可与pH计技术结合,研制便携式的检测器,具有无需固定场所、无需专业人员、结果立等可取等优势[26]。因此,该检测方法具有较好的应用前景,可为临床肿瘤的监测、治疗、预后等提供依据。
| [1] | Ryeom S, Folkman J. Role of endogenous angiogenesis inhibitors in Down syndrome[J]. J Craniofac Surg, 2009, 20 (Suppl 1): 595-6. DOI: 10.1097/SCS.0b013e3181927f47. |
| [2] | 牛蕾. 胃癌组织中VEGF和ILK的表达及意义[J]. 中国当代医药, 2015, 22 (20): 47-9. |
| [3] | 樊代明. 肿瘤研究前沿[M]. 第四军医大学出版社, 2012: 202-4. |
| [4] | Thompson DF, Eborall W, Dinsmore A, et al. Development and validation of a NANOGoldTM immunoassay for the detection of vascular endothelial growth factor(VEGF)in human serum using inductively coupled plasma mass spectrometry[J]. Rapid Commun Mass Spectrom, 2010, 24 (7): 927-32. DOI: 10.1002/rcm.v24:7. |
| [5] | 黄静, 李燕萍, 薛刚, 等. 血清VEGF-C、VEGF-D及VEGFR-3联合 TSH检测在甲状腺乳头状癌诊断中的价值[J]. 南方医科大学学报, 2014 (12): 1814-7. |
| [6] | Zhang J, Yin L, Wu J, et al. Detection of serum VEGF and MMP-9 levels by Luminex multiplexed assays in patients with breast infiltrative ductal carcinoma[J]. Exp Ther Med, 2014, 8 (1): 175-80. |
| [7] | 刘菲, 李学智, 付妮妮, 等. 短刺法对兔膝骨关节炎软骨细胞Sox9、 VEGF 和ColⅩ表达的影响[J]. 南方医科大学学报, 2016, 36 (7): 997-1003. |
| [8] | Vernes M, Meng G. Detection and quantification of VEGF isoforms by ELISA[J]. Methods Mol Biol, 2015, 1332 (7): 25-37. |
| [9] | Tuerk C, Gold L. Systematic evolution of ligands by exponential enrichment: RNA ligands to bacteriophage T4 DNA polymerase[J]. Science, 1990, 249 (4968): 505-10. DOI: 10.1126/science.2200121. |
| [10] | Kim S, Chung J, Song Y, et al. Aptamer cocktails: enhancement of sensing signals compared to single use of aptamers for detection of bacteria[J]. Biosens Bioelectron, 2014, 54 (8): 195-8. |
| [11] | Xie S, Chai Y, Yuan Y, et al. Development of an electrochemical method for Ochratoxin A detection based on aptamer and loop-mediated isothermal amplification[J]. Biosens Bioelectron, 2014, 55 (3): 324-9. |
| [12] | Zhao S, Ma W, Xu L, et al. Ultrasensitive SERS detection of VEGF based on a self-assembled Ag ornamented-AU pyramid superstructure[J]. Biosens Bioelectron, 2015, 68 (6): 593-7. |
| [13] | Zhang H, Li M, Li C, et al. G-quadruplex DNAzyme-based electrochemiluminescence biosensing strategy for VEGF165 detection: Combination of aptamer-target recognition and T7 exonuclease-assisted cycling signal amplification[J]. Biosens Bioelectron, 2015, 74 (8): 98-103. |
| [14] | Hsu L, Lien W, Wang W, et al. Immobilization of aptamer-modified Gold nanoparticles on BiOCl nanosheets: Tunable peroxidase-like activity by protein recognition[J]. Biosens Bioelectron, 2016, 75 (6): 181-7. |
| [15] | Chang C, Chen Y, Chuang L, et al. Aptamer-based colorimetric detection of proteins using a branched DNA cascade amplification strategy and unmodified Gold nanoparticles[J]. Biosens Bioelectron, 2016, 78 (4): 200-5. |
| [16] | Fu XM, Liu ZJ, Cai SX, et al. Electrochemical aptasensor for the detection of vascular endothelial growth factor (VEGF) based on DNA-templated Ag/Pt bimetallic nanoclusters[J]. Chin Chem Letters, 2016, 27 (6): 920-6. DOI: 10.1016/j.cclet.2016.04.014. |
| [17] | Fukaya T, Abe K, Savory N, et al. Improvement of the VEGF binding ability of DNA aptamers through in silico maturation and multimerization strategy[J]. J Biotechnol, 2015, 212 (8): 99-105. |
| [18] | Hermann T, Patel DJ. Adaptive recognition by nucleic acid aptamers[J]. Science, 2000, 287 (5454): 820-5. DOI: 10.1126/science.287.5454.820. |
| [19] | 郑静, 何品刚, 方禹之. 核酸适体生物传感器[J]. 化学进展, 2009, 21 (4): 732-8. |
| [20] | Ma H, Liu J, Ali M, et al. Nucleic acid aptamers in Cancer research, diagnosis and therapy[J]. Chem Soc Rev, 2015, 44 (5): 1240-56. DOI: 10.1039/C4CS00357H. |
| [21] | Zhao Z, Fan H, Zhou G, et al. Activatable fluorescence/MRI bimodal platform for tumor cell imaging via MnO2 nanosheetaptamer nanoprobe[J]. J Am Chem Soc, 2014, 136 (32): 11220-3. DOI: 10.1021/ja5029364. |
| [22] | Ahmad M, Xiao Y, Soh T. Selection is more intelligent than design: improving the affinity of a bivalent ligand through directed evolution[J]. Nucleic Acids Res, 2012, 40 (22): 11777-83. DOI: 10.1093/nar/gks899. |
| [23] | Nonaka Y, Yoshida W, Abe K, et al. Affinity improvement of a VEGF aptamer by in silico maturation for a sensitive VEGFdetection system[J]. Anal Chem, 2013, 85 (2): 1132-7. DOI: 10.1021/ac303023d. |
| [24] | ZhanW, Bard J. Electrogenerated chemiluminescence. 83. Immunoassay of human C-reactive protein by using Ru(bpy)3(2 + )-encapsulated liposomes as labels[J]. Anal Chem, 2007, 79 (2): 459-63. DOI: 10.1021/ac061336f. |
| [25] | Arai T, Sato T, Kanoh H, et al. Organic-inorganic hybrid polymerencapsulated magnetic nanobead catalysts[J]. Chemistry, 2008, 14 (3): 882-5. DOI: 10.1002/(ISSN)1521-3765. |
| [26] | Xie S, Yuan Y Song Y, et al. Using the ubiquitous pH meter combined with a loop mediated isothermal amplification method for facile and sensitive detection of nosema bombycis genomic DNA PTP1[J]. Chem Commun (Camb), 2014, 50 (10): 15932-5. |
 2017, Vol. 37
2017, Vol. 37

