主动脉夹层发病急、病情凶险,往往需要深低温停循环手术,Stanford A型主动脉夹层的有效治疗手段是手术干预,弓部重建与术中出血一直是心外科医生面临的难点,直接关系手术成功率与并发症的发生率。由于主动脉弓在解剖及病理改变上较为复杂,弓部重建的最优术式始终存在争议。目前得到广泛认可的弓部重建方法是采用四分叉人工血管加支架象鼻置入术行全弓置换(孙氏手术),但该术式操作比较复杂,吻合口多,实际应用起来风险较大,学习曲线时间长。部分学者认为过于复杂的术式会增加手术后的早期风险,简化手术可有效挽救患者生命,降低术后病死率和并发症发生率。徐志云[1]、谷天祥[2]及高长青[3]等采用相对简化的术式,在处理弓部时,做一类似右半弓替换但范围更大的切口,自大弯侧无名动脉开口近端至小弯侧左锁骨下动脉开口对应位置,经此切口植入术中支架,并将术中支架近端与降主动脉近端行腔内吻合,再将弧形切口与修剪适配的近端人工血管吻合。孙立忠等[4]提出了简化的孙氏手术,即保留头臂血管的孙氏手术,在无名动脉近端斜行切开主动脉弓,植入支架血管,支架血管近端完全覆盖三分支开口,楔形修剪大弯侧人工血管,完全显露无名动脉和左颈总分支开口,将人工血管近端与主动脉壁全层吻合,再与近端人工血管行端端吻合,最后将左锁骨下动脉分支开口与左颈总动脉做端侧吻合。本质上这些改良术式是岛状吻合法重建主动脉弓的延续,在适应证选择得当的情况下均取得了满意的治疗效果。我们在此基础上采用了更为简化的术式,即保留自体头臂血管、主动脉弓成形加支架象鼻手术治疗主动脉夹层。保留头臂血管的主动脉弓成形加支架象鼻术减少了吻合口的数量,简化了手术操作程序,缩短了停循环时间,易于掌握。我们采用该术式治疗23例Stanford A型主动脉夹层患者,现总结手术近中期效果报道如下。
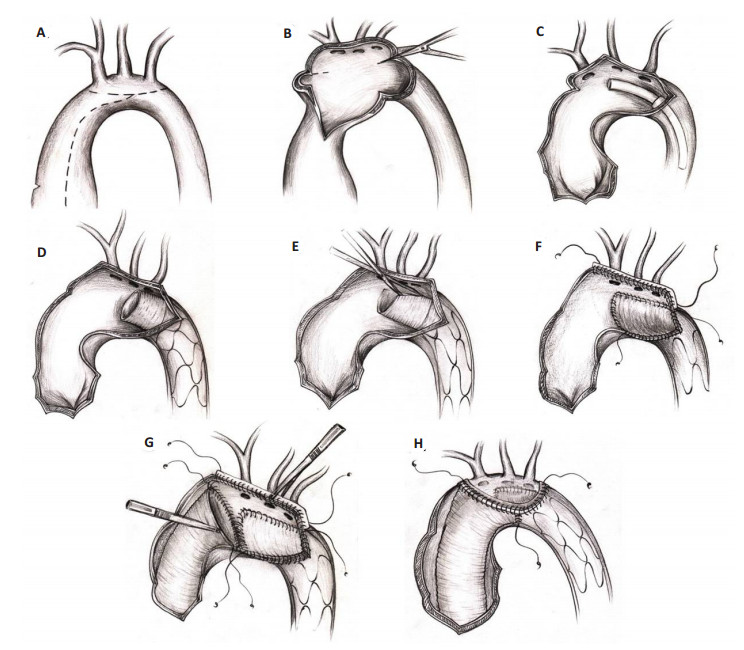
1 资料和方法2013年1月~2014年12月选择主动脉夹层Stanford A型(头臂血管内膜完整)的患者23例,其中男16例,女7例。年龄31~72(56.5±12.3)岁;手术方式:主动脉弓降部处理均为全弓部成形术+胸降主动脉支架象鼻术;升主动脉处理:升主动脉置换术15例,Bentall手术6例,David手术2例,合并冠状动脉旁路移植术3例。采用经典选择性顺行脑灌注和深低温停循环方法,经腋动脉或股动脉插管,上、下腔或右房插管常规建立体外循环,降温至鼻咽温32 ℃后阻断升主动脉,剖开升主动脉,左、右冠状动脉灌注心肌保护液液,在持续降温过程中实施主动脉根部操作。鼻咽温度到达18 ℃时,停循环,阻断头臂血管,选择性脑灌注。沿主动脉弓长轴头臂血管下切开主动脉弓部(图 1A),显露头臂血管开口,主动脉残端成形,修剪撕裂的内膜组织,保留整个主动脉外膜组织,头臂血管开口部分修剪成半岛状作为吻合缘(图 1B),在夹层的内膜与外膜两侧各加一毛毡条,连续缝合,按“三明治”法加固半岛状头臂血管游离缘,闭合分离的夹层,完成主动脉弓顶部头臂血管开口部分的重建(图 1F)。降主动脉真腔中植入Cronus支架血管(图 1C),隔绝假腔,确保支架血管钢丝骨架区位于左锁骨下动脉开口远端,采用合适的角度斜行修剪大弯侧Cronus支架血管无钢丝骨架区,确保无骨架区人工血管未对头臂干、左颈总动脉、左锁骨下动脉开口造成遮挡(图 1D),同时使修剪后的Cronus支架血管近端尽量与主动脉弓降部残端契合(图 1E),再将Cronus支架血管近端无钢丝区与弓部、降主动脉起始部的主动脉壁全层吻合,完成降主动脉起始部的处理(图 1F)。然后修剪升主动脉人工血管远心端(主动脉根部及升主动脉的处理根据主动脉窦部病变程度选择升主动脉置换术、Bentall手术、以及David手术);最后再将弓顶部半岛状头臂血管游离缘、降主动脉起始部、升主动脉人工血管远端这三部分做连续吻合(图 1G),完成弓部重建(图 1H)。开放循环后,再完成升主动脉外膜瘤壁对升主动脉人工血管的包裹。
|
图 1 全弓部成形术+胸降主动脉支架象鼻术手术步骤 Figure 1 Fig.1 Procedure of brachiocephalic artery-sparing aortic arch repair combined with stent-graft elephant trunk technique. A: The ascending aorta and the transverse arch were dissected and exposed. B: The anterior wall of the aortic arch was incised longitudinally up to the origin of the descending aorta. C, D: The surgical stent graft was implanted into the lumen of the distal aorta, while the proximal edge of the metallic stent (not the stent-free sewing edge) was positioned between the origin of the left subclavian artery and the descending aorta. E: To avoid blocking of the origin of brachiocephalic arteries, the stent-free sewing edge was pulled, and the spiral-shaped Dacron graft could be straightened to approximately 3.0 cm in length. The straightened prosthetic graft was trimmed to match the estimated shape of the aortic arch wall containing the origin of the brachiocephalic arteries. F: The trimmed stent-free sewing edge was sutured to the autologous aortic arch wall adjacent to the origin of the brachiocephalic arteries using a continuous suture line. Thus the residual aortic arch wall and the trimmed stent-free sewing edge commonly formed a large irregular rounded opening. G, H: The distal end of a woven Dacron graft (which was anastomosed to the aortic root) was anastomosed to the descending aorta containing the residual aortic arch wall and the surgical graft. |
本组住院期间无死亡,术中体外循环时间(209±52)min,升主动脉阻断时间(85±21)min,选择性脑灌注时间(28±15)min;术后24 h胸引流量(570±263)mL,无再次开胸止血病例。3例患者术后出现急性肾功能衰竭行床边连续性肾替代治疗,均治愈出院;短暂的神经系统并发症(延迟苏醒)2例;1例患者术后出现一过性截瘫(脊髓休克),术后6个月完全康复;败血症l例,血培养证实为细菌感染,治愈出院。23例患者出院前、后均复查全主动脉增强CT,显示人工血管通畅,支架血管未见位移及内瘘发生,头臂血管及远端假腔明显缩小或消失(图 2、3)。
|
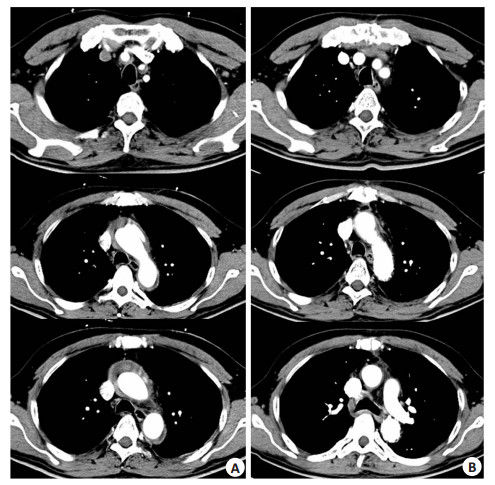
图 2 患者术前术后CTA对比 Figure 2 Three-dimensional computed tomography before and after surgery in a patient with type A aortic dissection. A: Before the operation; B: After the operation. |
|
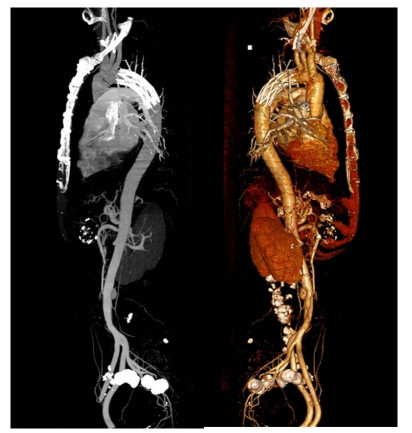
图 3 患者术后CTA重建影像 Figure 3 Three-dimensional computed tomography reconstruction of acute type A dissection after surgery. |
术后随访6~18个月,恢复良好,随访期间无死亡,未发生因夹层进展需再次手术,未发生心内膜炎等并发症以及有临床意义的血栓栓塞事件。2例发生二尖瓣中度关闭不全,因患者自身原因,未再次手术治疗。
3 讨论Stanford A型主动脉夹层发病凶险,死亡率高,有文献报道,自发病起每过1 h病死率增加1%,48 h内死亡率高达30%~50% [5-7]。一经诊断,均应手术治疗,如未接受外科治疗,患者2~4周内的死亡率可达75% [8]。外科手术是急性A型主动脉夹层目前最有效治疗手段,但手术风险高,手术死亡率达20% [9]。随着手术技术的不断改进,体外循环、麻醉、围手术期监护和生命支持系统等整体技术水平的进步,A型主动脉夹层患者的外科手术生存率和远期生存率得到一定程度的提高。然而涉及主动脉弓部的手术死亡率仍可达10%以上[10],同时主动脉弓部重建的手术方式一直存在争议。Stanford A型主动脉夹层目前较为公认的弓部重建方式是采用四分叉人工血管加支架象鼻置入术行全弓置换(孙氏手术)[11-13]。但这种手术方式在实际操作中有时必须面对吻合口出血难以控制的极端情况,特别是超急性期内的急诊手术,由于血管组织脆弱,极易发生撕裂,大量出血给手术带来极大的风险;同时由于头臂血管吻合口在弓部以外,无法实施腔内包裹及心房内引流技术,实际操作时手术时间较长,风险大。
虽然目前对Stanford A型主动脉夹层弓部重建术式仍无一致的意见,但是有公认的指导原则,即消除动脉夹层的破口和假腔,重建主动脉的连续性和完整性,防止夹层继续进展。在上述原则的指导下,我们力求用最简单、有效、安全的方式达到解剖重建主动脉弓的目的,结合岛状重建主动脉弓与保留头臂血管孙氏手术这两种术式的优点,本组患者采取保留头臂血管的策略,处理并利用升主动脉和主动脉弓部血管残端,做适当的修剪、加固成形,做为弓部重建的一部分;尽可能保留弓部大弯侧血管组织及头臂血管开口,通过此切口充分暴露降主动脉开口,并释放支架,同时利用一个吻合口完成弓部的重建。此方法与孙氏手术不同,节省了2个吻合口。大大简化了手术操作,深低温停循环时间可以缩短至30 min以内,减轻脑部和其他并发症的发生及死亡率[14-16];特别适用于弓部分支血管起始部未受累以及少数受累不严重的患者。
Stanford A型主动脉夹层动脉瘤内膜破口一般起始于升主动脉近端,剥离部位起自升主动脉根部,向主动脉远端延伸至降主动脉。但亦可起始于主动脉弓甚至胸降主动脉,逆行分离至主动脉根部和向远端分离累及主动脉的其他部位。我们根据主动脉夹层破口的位置及头臂血管内膜的完整性、弓部大弯侧后壁是否存留夹层未累及的血管壁这三个因素来决定是否采用保留头臂血管的方式重建主动脉弓部。本组23例患者,头臂血管内膜均完整,采用三明治技术加固成型后可封闭假腔;弓部大弯侧的后壁均存留有部分正常血管组织(头臂血管开口下),可做弓部重建的后部;15例破口位于升主动脉,5例位于升主动脉小弯侧,2例位于大弯侧,1例位于降主动脉。岛状移植技术的主要问题是一旦吻合口的后壁发生出血,无法显露,止血极为困难。我们采取严格把握指征的策略,保留主动脉弓部大弯侧组织,便于血管外膜对整个升主动脉及弓部人工血管的包裹,加固止血方便。本组23例均未发生吻合口出血,吻合时间和脑部缺血时间明显缩短。近年来多位学者的报道也证实分支吻合法与岛状吻合法在早期病死率、合并症发生率、远期再次手术率等方面差异无统计学意义[17-20]。虽然保留头臂血管的策略不能用于所有的Stanford A型主动脉夹层的患者,但是在掌握好适应证的情况下,完全可以取得满意的治疗效果。保留头臂血管的主动脉弓成形加支架象鼻术具有以下三个方面的优势,首先该术式可以保留全部自体头臂血管,减少远期栓塞的发生,显著降低再手术的风险;其次减少了吻合口的数量,简化了操作,大大缩短停循环时间,减少相关并发症的发生;同时有利于术者使用主动脉外膜对人工血管以及吻合口进行包裹,便于使用内引流技术控制出血,降低死亡率。我们认为在采用保留头臂血管的主动脉弓成形加支架象鼻术时,应符如下的原则:第一,严格筛选病例,头臂血管内膜完整且不能合并遗传性结缔组织病,本组病例头臂血管开口内膜完整,无撕脱,探查管腔通畅;对头臂血管严重受累,探查时发现内膜不完整的患者应采用全弓置换术。第二,应注意升主动脉人工血管形状的修剪,长度、大小、弧度要与弓部残端、支架血管近段匹配,保证重建后的弓部无扭曲、变形。本组23例患者术后随访总体效果满意,出院后多次复查全主动脉CTA提示人工血管通畅,支架血管未见位移及内瘘发生,头臂血管及远端假腔明显缩小或消失。
总之,Stanford A型主动脉夹层手术,特别是深低温停循环下弓降部重建手术,选择合适的病例尽量行简化的手术策略可减少围术期死亡和并发症的发生。保留头臂血管的主动脉弓成形加支架象鼻术是治疗Stanford A型主动脉夹层安全、有效的方法,近期效果良好,适于推广。
| [1] | 徐志云, 宋智钢, 陆方林, 等. 改良支架"象鼻"手术治疗Stanford A型主动脉夹层的临床应用[J]. 第二军医大学学报, 2006, 27 (9): 992-4. |
| [2] | 谷天祥, 于洋, 师恩祎, 等. 改良"次全弓置换加支架象鼻手术治疗Stanford A型主动脉夹层[J]. 中国胸心血管外科临床杂志, 2012, 19 (1): 4-7. |
| [3] | 肖苍松, 高长青, 吴扬, 等. 急性DeBakey I型主动脉夹层的弓部手术及近中期结果[J]. 中国胸心血管外科杂志, 2014, 30 (5): 293-5. |
| [4] | Zhu JM, Qi RD, Chen L, et al. Surgery for acute type A dissection using total arch replacement combined with stented elephant trunk implantation: Preservation of autologous brachiocephalic vessels[J]. J Thorac Cardiovasc Surg, 2015, 150 (1): 101-5. DOI: 10.1016/j.jtcvs.2015.03.002. |
| [5] | Braverman C. Aortic dissection: prompt diagnosis and emergency treatment are critical[J]. Cleve Clin J Med, 2011, 78 (10): 685-96. DOI: 10.3949/ccjm.78a.11053. |
| [6] | Mészáros I, Mórocz J, Szlávi J, et al. Epidemiology and clinicopathology of aortic dissection[J]. Chest, 2000, 117 (5): 1271-8. DOI: 10.1378/chest.117.5.1271. |
| [7] | David TE, Armstrong S, Ivanov J, et al. Surgery for acute type A aortic dissection[J]. Ann Thorac Surg, 1999, 67 (6): 1999-2001. DOI: 10.1016/S0003-4975(99)00353-7. |
| [8] | Moon MR. Approach to the treatment of aortic dissection[J]. Surg Clin North Am, 2009, 89 (4): 869. DOI: 10.1016/j.suc.2009.05.003. |
| [9] | Tsai T, Trimarchi S, Nienaber A. Acute aortic dissection: perspectives from the International Registry of Acute Aortic Dissection (IRAD)[J]. Eur J Vasc Endovasc Surg, 2009, 37 (2): 149-59. DOI: 10.1016/j.ejvs.2008.11.032. |
| [10] | Tsagakis K, Pacini D, Di Bartolomeo R, et al. Arch replacement and downstream stent grafting in complex aortic dissection: first results of an international registry[J]. Eur J Cardiothorac Surg, 2011, 39 (1): 87-93. DOI: 10.1016/j.ejcts.2010.03.070. |
| [11] | Sun L, Qi R, Zhu J, et al. Total arch replacement combined with stented elephant trunk implantation: a new "standard" therapy for type a dissection involving repair of the aortic arch[J]. Circulation, 2011, 123 (9): 971-8. DOI: 10.1161/CIRCULATIONAHA.110.015081. |
| [12] | Katayama A, Uchida N, Katayama K, et al. The frozen elephant trunk technique for acute type A aortic dissection: results from 15 years of experience[J]. Eur J Cardiothorac Surg, 2015, 47 (2): 355-60. DOI: 10.1093/ejcts/ezu173. |
| [13] | Shrestha M, Fleissner F, Ius F, et al. Total aortic arch replacement with frozen elephant trunk in acute type A aortic dissections: are we pushing the limits too far[J]. Eur J Cardiothorac Surg, 2015, 47 (2): 361-6. DOI: 10.1093/ejcts/ezu185. |
| [14] | Westaby S, Saito S, Katsumata T. Acute type A dissection: conservative methods provide consistently low mortality[J]. Ann Thorac Surg, 2002, 73 (3): 707-13. DOI: 10.1016/S0003-4975(01)03449-X. |
| [15] | Shiono M, Hata M, Sezai A, et al. Validity of a limited ascending and hemiarch replacement for acute type A aortic dissection[J]. Ann Thorac Surg, 2006, 82 (5): 1665-9. DOI: 10.1016/j.athoracsur.2006.05.112. |
| [16] | Bakaeen G, Chu Danny, Huh J, et al. Outcomes of circulatory arrest procedures for the treatment of thoracic aortic disease at a veterans facility[J]. Am J Surg, 2010, 200 (5): 581-4. DOI: 10.1016/j.amjsurg.2010.07.010. |
| [17] | Shrestha M, Martens A, Behrendt S, et al. Is the branched graft technique better than the en bloc technique for total aortic arch replacement[J]. Eur J Cardiothorac Surg, 2014, 45 (1): 181-6. DOI: 10.1093/ejcts/ezt357. |
| [18] | Di Eusanio M, Schepens MA, Morshuis WJ, et al. Separate grafts or en bloc anastomosis for arch vessels reimplantation to the aortic arch[J]. Ann Thorac Surg, 2004, 77 (6): 2021-8. DOI: 10.1016/j.athoracsur.2003.10.094. |
| [19] | Karck M, Chavan A, Khaladj N, et al. The frozen elephant trunk technique for the treatment of extensive thoracic aortic aneurysms: operative results and follow-up[J]. Eur J Cardiothorac Surg, 2005, 28(2): 286-90; discussion 290. |
| [20] | 叶鹏, 陈勇, 曾庆乐, 等. 血管缝合器预缝合技术完全经皮穿刺途径完成主动脉腔内修复术后的股动脉中长期随访结果[J]. 南方医科大学学报, 2014, 34 (5): 747-50. |
 2017, Vol. 37
2017, Vol. 37

