2. 南方医科大学国际病代谢中心, 广东广州 510515 ;
3. 东莞南方医大代谢医学研发有限公司, 广东东莞 523000 ;
4. 南方医科大学神经生物教研室, 广东广州 510515 ;
5. 美国加州大学洛杉矶医学院胰腺病中心, 美国加州 90095
2. International Center for Metabolic Diseases, Southern Medical University, Guangzhou 510515, China ;
3. Dongguan SMU Metabolic Medicine R & D Inc, Dongguan 523000, China ;
4. Department of Neurobiology, School of Basic Medical Sciences, Southern Medical University, Guangzhou 510515, China ;
5. UCLA Center for Excellence in Pancreatic Disease, David Geffen School of Medicine, University of California, Los Angeles, California 90095, USA
全球糖尿病发病率正处于快速增长期,根据国际糖尿病联盟(IDF)最新的公布的第七版糖尿病数据显示,2015年全球糖尿病患者人数4.15亿,患病率8.8%。全球糖尿病患病率呈快速上升趋势,预计2040年糖尿病患者数将达6.42亿,患病率将上升至10.4%。中国糖尿病患者数2015年达1.096亿,居全球首位,预计到2040年中国糖尿病患者数将达1.507亿[1]。糖尿病常引起严重并发症,除血管病变、视网膜病、肾病和外周神经病变等传统并发症外,近来糖尿病脑病也越来越引起人们的注意[2]。糖尿病脑病在临床表现为认知功能障碍、痴呆、精神性疾患等,并且其发病隐匿,不易察觉[3]。随着糖尿病并研究的逐步深入,已经发现糖尿病与认知障碍之间有明显的相关性,是诱发AD(Alzheimer's Disease)的一个危险因素[4]。在成年糖尿病患者中,常常伴有一定学习和记忆功能障碍,并且阿尔茨海默病发病率的风险显著增高2~3倍[3]。糖尿病患者常伴发抑郁症, 而抑郁症等不良情绪对糖尿病的代谢控制及转归有消极影响,因此控制糖尿病脑病对于糖尿病的治疗有重要的意义。目前用于改善学习与记忆功能的药物主要有他克林、卡巴拉汀、加兰他敏、多奈哌齐、美金刚等,它们主要通过以乙酰胆碱前体、乙酰胆碱酯酶抑制剂和选择性胆碱能受体激动剂的方式,暂时性缓解疾病症状,寻找能有效防治糖尿病脑病的药物具有非常重要的意义[5]。
胰高血糖素样肽-1(GLP-1)是由肠壁L-细胞分泌的激素,其作用包括刺激葡萄糖依赖性胰岛素分泌,促进胰岛素生物合成,降低血糖,保护胰岛B细胞,改善T2DM的症状[6]。此外,近年发现它还能促进神经细胞的增殖和神经发生,抑制神经细胞凋亡。例如,Gault报道[7]GLP-1不仅直接调节神经递质的释放和LTP(synaptic plasticity)的形成,而且能保护由β-淀粉样蛋白片段诱导的突触LTP损伤。目前认为GLP-1及其类似物的这种作用可能与其能保护脑细胞和增加脑血流量有关[8-9],对于GLP-1对于脑部的保护作用的已经有一定研究[10-12],但有关其保护的分子机理尚不清楚。
本研究通过GLP-1治疗糖尿病模型动物,观察GLP-1改善糖尿病引起的大鼠学习与记忆功能的损伤及其可能的机理。
1 材料和方法 1.1 材料 1.1.1 实验动物选取6~8周的SD雄性大鼠,体质量160~180 g购买自南方医科大学动物实验中心, 合格证号SCXK(粤)2011-0015。所有动物操作均依照制度动物保健和使用委员会的指导方针。
1.1.2 主要试剂GLP-1自上海波肽生物公司合成(500 mg,纯度>95%),链脲佐菌素(STZ)购自sigma公司(批号S0130-1G)。抗Arc抗体购自santa cruz公司(sc-15325),抗β-actin抗体购自博世德公司(BM1623),羊抗兔二抗购自弗德生物公司(FDR007),荧光定量PCR试剂盒购自TAKARA公司(RR047A, RR820A),水合氯醛、甲醛购自广州金华大化学试剂有限公司,所有化学试剂均为分析纯度。
1.1.3 仪器Applied Biosystems 7500荧光定量PCR仪(美国ABI),安准血糖检测仪(长沙三诺生物传感技术有限公司),2001植入式胶囊渗透压缓释泵(美国Alzet公司),酶标仪(美国Biorad),水迷宫仪器购买自上海移数公司,鼠博士行为学软件用于水迷宫数据分析。
1.2 实验方法 1.2.1 分组和给药雄性SD大鼠27只于实验前适应性喂养1周后,随机分为3组,每组9只。对照组大鼠常规饲料喂养,糖尿病大鼠参照沈亚非[13]等的方法制备糖尿病大鼠模型,采用高脂高糖饲料喂养,1个月后,大鼠腹腔注射链脲佐菌素40 mg/kg,3 d后监测血糖,连续2 d血糖均高于16.7 mmol/L认定为2型糖尿病。糖尿病大鼠喂养25 d后被随机分成模型组和GLP-1组,模型组糖尿病大鼠不做治疗处理。GLP-1组通过皮下手术包埋植入式渗透压泵灌注GLP-1(30 pmal/kg/min),连续给药7 d。
1.2.2 Morris水迷宫水迷宫实验参照Wang等[14]的方法。试验简述如下:水迷宫在一个直径160 cm的圆形黑色水池中进行,水温保持在25±2 ℃,一个12 cm直径透明圆形平台放置在水下2 cm。定位航行定在每天下午2点进行,连续5 d。实验时,已经提前1 h适应的大鼠被面朝池壁分4个象限放入水中,动物60 s内寻找到平台的时间记录为逃避潜伏期。在60 s内没有找到平台的大鼠,则用小木棍引导至平台,并让平台上停留15 s,让其记忆空间标记物,记录逃避潜伏期为60 s。成功在60 s内到达平台动物同样让其在平台休息15 s。试验结束。每只大鼠每次游泳时候的路线和逃避潜伏期都会被记录下来。
在定位航行实验完成后24 h,进行空间探索实验,我们把平台移除,让大鼠在原来平台对侧象限入水,在水池中游泳60 s,记录大鼠游泳的路线,计算通过原来平台的次数和在原来平台象限的时间百分比。
1.2.3 荧光定量PCR检测基因mRNA转录水平荧光定量PCR检测基因mRNA转录水平:大鼠迅速断头后,头部沿着中线剪开皮肤,再剪刀向上挑着把颅骨剪开,到嗅区空洞处向左向右各剪1刀,然后用镊子把颅骨扒开,迅速把脑部放到冰冻的PBS中,用镊子分离大脑海马区组织。切碎研磨采集的大鼠海马区组织,提取各组总RNA,测定浓度,各取1 μg总RNA用于RT-QPCR检测,引物序列如表 1所示,检测方法参照试剂盒说明书。
| 表 1 大鼠来源引物序列 Table 1 Primer sequences from rats |
自采集大鼠的海马组织中提取蛋白质。每100 mg大鼠大脑组织加入1 mL RIPA裂解液,充分研磨裂解,12 000 g离心15 min,将上清转移到干净无菌的离心管中,BCA法测定蛋白的浓度,用裂解液调整蛋白浓度一致,取20 μL调整好蛋白浓度样品,加入5 μL的5×还原性的SDS-PAGE上游缓冲液,混匀,沸水煮样品10 min使其变性。上胶100 V恒压20 min,下胶180 V 50 min的SDS-PAGE(10%胶)电泳后,200 mA恒流90 min转膜,把膜取出后置于5% BSA封闭2 h,之后把膜放置稀释后一抗中,4 ℃孵育过夜。次日,把膜用TBST洗4次后,置于稀释后2抗中(1:5000),摇床中室温孵育1 h。把膜在TBST洗4次后,在膜上加入ECL发光液发光,最后在暗室中曝光显影条带。
1.2.5 免疫组化检测Arc在大鼠海马区表达变化及定位石蜡切片脱蜡至水:依次将切片放入二甲苯Ⅰ15 min-二甲苯Ⅱ15 min无水乙醇Ⅰ10 min-无水乙醇Ⅱ10 min-95%酒精5 min-90%酒精5 min~80%酒精5 min-70%酒精5 min-蒸馏水洗。抗原修复:组织切片置于盛满EDTA抗原修复缓冲液(PH8.0)的修复盒中于微波炉内进行抗原修复。中火8 min,停火8 min,然后中低火7 min,此过程中应防止缓冲液过度蒸发,切勿干片。自然冷却后将玻片置于PBS(pH7.4)中在脱色摇床上晃动洗涤3次,每次5 min。阻断内源性过氧化物酶:切片放入3%过氧化氢溶液,室温避光孵育25 min,将玻片置于PBS(PH7.4)中在脱色摇床上晃动洗涤3次,每次5 min。加一抗:切片稍甩干后用组化笔在组织周围画圈(防止抗体流走),在圈内滴加用3% BSA室温封闭30 min,甩掉BSA滴加按一定比例稀释好的一抗覆盖组织。切片平放于湿盒内4 ℃孵育过夜。加二抗:玻片置于PBS(pH7.4)中在脱色摇床上晃动洗涤3次,每次5 min。切片稍甩干后在圈内滴加组化试剂盒内与一抗相应种属的二抗(HRP标记)覆盖组织,室温孵育50 min。DAB显色:玻片置于PBS(PH7.4)中在脱色摇床上晃动洗涤3次,每次5 min。切片稍甩干后在圈内滴加新鲜配制的DAB显色液,显微镜下控制显色时间,阳性为棕黄色,自来水冲洗切片终止显色。复染细胞核:Harris苏木素复染3 min左右,自来水洗,1%的盐酸酒精分化数秒,自来水冲洗,氨水返蓝,流水冲洗。脱水封片:将切片依次放入70%酒精5 min-80%酒精5 min-90%酒精5 min-95%酒精5 min-无水乙醇Ⅰ5 min-无水乙醇Ⅱ5 min-二甲苯Ⅰ5 min-二甲苯Ⅱ5 min中脱水透明,将切片从二甲苯拿出来稍晾干,中性树胶封片。
1.2.6 统计分析应用SPSS 20.0软件进行统计分析。水迷宫实验采用two-way ANOVA,bonferroni法对组别进行检验分析,其他实验采用one-way,bonferroni法对组别进行检验分析,以P < 0.05认为差异有统计学意义。
2 结果 2.1 2型糖尿病动物模型成功建立,动物出现显著的糖尿病病症在采用高糖高脂饲喂大鼠4周后腹腔注射链脲佐菌素,注射链脲佐菌素3 d后,连续空腹血糖检测达到25.8±3.1 mmol/L(表 2),高于糖尿病标准值16.7 mmol/L,连续空腹血糖检测,其中显示血糖一直高于16.7 mmol/L,并且大鼠具有典型的多饮、多食、多尿、尿液混浊、消瘦等糖尿病病,表明2型糖尿病大鼠模型制作成功。
| 表 2 注射STZ后大鼠空腹血糖值 Table 2 Fast blood glucose in rats after STZ injection (mmol/L, Mean±SD, n=9) |
采用高糖高脂STZ诱导方法制备糖尿病动物模型后,我们参照文献报道方法,采用Morris水迷宫实验观察3组大鼠(正常大鼠、糖尿病大鼠、GLP-1处理组大鼠)在水池内游泳并找到藏在水下逃避平台的能力,判断GLP-1的保护作用。
(1) 定位航行实验是用于测量大鼠学习和记忆能力的经典方法。如表 3所示,各组之间的潜伏期在前2 d没有观察到显著区别(P>0.05),但自第3天起,DM组的潜伏期明显比Normal组潜伏期延长(P < 0.05),该趋势持续到第4天和第5天,显示STZ诱导的DM组大鼠的学习记忆功能自第3天后表现出明显受损。而同时接受GLP-1处理的糖尿病大鼠,其第3天的潜伏期显著低于糖尿病组(P < 0.05),与Normal组差异不显著(P>0.05)。这种现象在第4天和第5天都持续观察到,说明GLP-1能减轻糖尿病对大鼠学习功能的破坏,保护大鼠的学习功能(表 3)。大鼠在定位航行实验中的游泳速度,各组游泳速度没有显著差异,说明动物自主运动能力没有差异(表 4)。
| 表 3 Morris水迷宫实验定向航行实验检测大鼠逃避潜伏期 Table 3 Escape latency of rats in place navigation in Morris water maze test (s, Mean±SD, n=9) |
| 表 4 Morris水迷宫实验定向航行实验大鼠游泳速 Table 4 Velocity of swimming in place navigation in Morris water maze test (cm/s, Mean±SD, n=9) |
(2) 空间探索实验用于测量大鼠在学会寻找平台后,对平台位置记忆的保持能力。定位航行实验结束后24 h,撤去平台,从原平台对面象限中央放入水中,记录其在水池中游泳轨迹,计算60 s内通过原平台的次数,以及在原平台象限的保留时间。在本实验中,与Normal组穿过原平台次数相比,DM组次数显著减少,显示DM组的记忆功能损伤。而GLP-1组通过平台次数高于DM组,统计分析显示有显著性差别(P < 0.05),基本接近Normal组水平(P>0.05),表 5展示了各组大鼠在目标象限的时间百分比数字。统计分析显示DM组与正常对照组之间有显著性差异(P < 0.05),说明糖尿病大鼠有明显的记忆能力障碍,而GLP-1处理组百分比显著好于DM组百分比(P < 0.05),与Normal组接近(P> 0.05),表明GLP-1能减轻糖尿病引起的记忆功能损伤。
| 表 5 穿越原平台次数(次)及停留原平台所在象限停留时间百分比 Table 5 Number of crossing the original platform and time percentage in the target quadrant (Mean±SD, n=9) |
取各组大鼠的大脑海马区组织,Real-time PCR方法分析记忆相关基因在大鼠大脑海马区mRNA的转录水平,以进一步了解糖尿病大鼠脑损伤和GLP-1保护作用的分子机制。PKC,PKA和ERK1/2是细胞内与细胞增殖、分化和凋亡最密切的常见信号通路;Arc作为PKC,PKA,ERK1/2信号通路下游的分子,能够调控APP,PS1,BACE1等分子的表达和修饰,从而调控Aβ的产生[15]。与正常组相比,糖尿病大鼠大脑细胞内PKC,PKA,ERK1/2的表达均有增高(P < 0.05),同时诱导Arc,APP,PS1,BACE1的表达升高(P < 0.05),这些变化是引起糖尿病大鼠脑学习与记忆功能障碍的主要信号途径(表 6)。而GLP-1处理能够抑制PKC,PKA和ERK1/2,以及其下游的Arc,APP,PS1,BACE1升高(P < 0.05)。表明GLP-1是通过抑制这条通路分子的表达来实现对脑细胞功能的保护。
| 表 6 荧光定量PCR检测大鼠海马区中mRNA表达RQ Table 6 Relative mRNA expressions of genes related with cognitive function in the hippocampus of the rats(Mean±SD) |
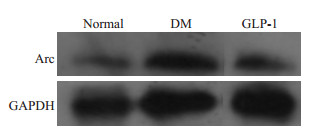
为了在蛋白水平进一步证实ARC的作用,我们从各组大鼠大脑海马区组织提取蛋白,进行Western blotting实验。DM组的Arc表达显著高于Normal组,而GLP-1组ARC表达比DM组要低(图 1)。这些结果同PCR结果相吻合,即ARC在糖尿病大脑细胞中表达增高,GLP-1处理后糖尿病大鼠海马区ARC的表达下降。
|
图 1 WB检测Arc在各组大鼠海马区表达 Figure 1 Detection of Arc expression in the hippocampus of the rats by Western blotting. |
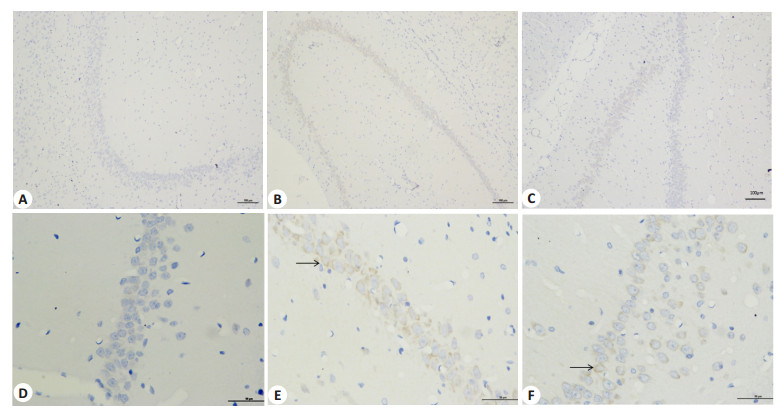
Arc为神经突触后蛋白,Arc的变化与AD的发生有密切联系。我们采用免疫组化方法进一步证实ARC的变化和作用。图 2中表明Arc蛋白在大鼠海马区的表达位置及含量。图中蓝色染色为海马区细胞,黄褐色为Arc在细胞中的蛋白表达位置。在正常组细胞中几乎观察不到明显黄褐色的Arc表达,而DM组中细胞膜的上黄褐色明显增多,显示ARC蛋白表达增多。与DM组相比,GLP-1组中细胞膜的黄褐色有所下降。该结果同上述的PCR和蛋白印迹方法相互吻合,表明ARC是影响脑细胞功能的重要分子,GLP-1可能是通过抑制糖尿病诱导的ARC过高表达,达到保护大鼠学习与记忆功能的作用。
|
图 2 免疫组化检测Arc在大鼠海马区表达变化及定位 Figure 2 Immunohistochemistry of Arc expression in the hippocampus of the rats in different groups (A, B, C: original magnification: ×100; D, E, F: ×400). A, D: Normal group; B, E: DM group; C, F: GLP-1 group. |
本研究通过GLP-1治疗糖尿病模型动物,定量分析了糖尿病大鼠的认知障碍和GLP-1对其保护作用。结果显示GLP-1治疗能够改善2型糖尿病的学习与记忆功能障碍,其效果可能是通过调控细胞的PKC,PKA, ERK1/2通路,抑制Arc的表达而实现的。
研究GLP-1对大脑的保护作用是近年来新出现的研究动态,报道不多,且各研究组在模型选择和观察指标上也不尽统一。Han等[11]使用向啮齿动物脑室内注射注射Aβ(4 μL,4 nmoL)的方式诱导脑损伤模型,并采用脑室内注射GLP-1类似物利拉鲁肽的方法观察GLP-1的作用,这种方式同糖尿病自然状态有显著差异。在本研究中我们采用高脂高糖链脲佐菌素诱导了2型糖尿病大鼠模型,这是糖尿病研究最为广泛使用的动物模型,并选用经典Morris水迷宫实验评价了大鼠的学习和记忆功能,然后采用空间探索实验观察了大鼠的记忆能力。结果显示DM组大鼠的学习记忆功能表现出明显受损,而GLP-1能减轻糖尿病对大鼠学习功能的破坏,保护糖尿病大鼠的学习功能。空间探索实验发现DM组通过原平台次数显著少于正常组,而GLP-1组通过平台次数基本接近Normal组水平,说明糖尿病影响了大鼠的记忆能力,GLP-1能减轻糖尿病引起的记忆功能损伤。在本实验中,我们观察到高糖高脂STZ诱导的2型糖尿病大鼠在发病4周后即可出现的学习与记忆功能障碍,大大早于Wang等[16]报道的糖尿病大鼠发病4个月后出现学习与记忆功能障碍的时间节点。我们首次发现GLP-1对高脂高糖链脲佐菌素诱导2型糖尿病引起的学习与记忆功能障碍有改善作用,这与Bromfim等采用GLP-1类似物艾塞那肽在APP/PS1突变鼠中的观察的学习与记忆功能障碍改善现象类似[10],证明GLP-1也是保护糖尿病脑功能的有效药物。
为了进一步搞清楚GLP-1是如何保护大脑组织的,我们观察了大脑细胞中相关基因的表达,以期勾画出GLP-1作用的信号转导途径。PKC、PKA、ERK1/2是细胞内与细胞增殖、分化和凋亡最密切的常见信号通路,已经有报道指出PKC、PKA、ERK1/2在糖尿病中会被激活,参与一系列的信号通路变化[17-19]。有报道认为糖尿病大鼠在会出现Aβ累积,海马萎缩,神经突触丢失等AD样病理变化[16]。Arc是一种可塑性蛋白,其参与着学习和记忆的进行,有研究发现,Arc在Aβ的产生中起着重要作用[20-22],在AD模型大鼠中,信号通路PKA,PKC,ERK激活Arc的表达,能引起Aβ的升高[18]。有研究认为GLP-1类似物的保护作用可能是通过调节JNK-IRS1通路[10],或Camp-PKC通路发生作用[11],但尚无法把GLP-1通路与Aβ累积等病理改变联系起来。在神经细胞中,APP通过β分泌酶BACE1和γ分泌酶PS1的连续的剪切最终产生Aβ [23-24],当这种有神经毒性的物质出现堆积时,会引起神经系统的病理学变化[15, 23, 25]。本实验系统观察了糖尿病大鼠大脑海马区PKA、PKC、ERK、APP、BACE1、Arc、PS1 mRNA水平上的变化,发现糖尿病大鼠(DM)的PS1、PKC、PKA、ERK1/2、BACE1、APP、Arc基因比正常组(Normal)表达增高(P < 0.05),完善了糖尿病脑学习与记忆功能损伤的分子机制。本研究还观察到GLP-1组中PS1,PKC,PKA,ERK1/2,BACE1,APP,Arc的mRNA水平比DM组中转录要低(P < 0.05),提示GLP-1正是通过抑制高糖高脂STZ诱导的该信号通路激活,而达到保护脑学习与记忆功能的作用。本结果大大细化了此前有关GLP-1在中枢神经系统中调节PKA,PKC等信号分子变化[26],更清楚地勾画出GLP-1的信号转导通路。
| [1] | Medscape. IDF Atlas:about 415 million adults worldwide have diabetes[Z], 2015. http://www.medscape.com/viewarticle/855296 |
| [2] | Strachan MW, Frier BM, Deary IJ. Type 2 diabetes and cognitive impairment[J]. Diabet Med,2003, 20 (1) : 1-2. DOI: 10.1046/j.1464-5491.2003.00855.x. |
| [3] | Velayudhan L, Poppe M, Archer N, et al. Risk of developing dementia in People with diabetes and mild cognitive impairment[J]. Br J Psychiatry,2010, 196 (1) : 36-40. DOI: 10.1192/bjp.bp.109.067942. |
| [4] | Zhou H, Lu W, Shi Y, et al. Impairments in cognition and restingstate connectivity of the hippocampus in elderly subjects with type 2 diabetes[J]. Neurosci Lett,2010, 473 (1) : 5-10. DOI: 10.1016/j.neulet.2009.12.057. |
| [5] | Sebastiao I, Candeias E, Santos MS, et al. Insulin as a bridge between type 2 diabetes and alzheimer Disease-How Anti-Diabetics could be a solution for Dementia[J]. Front Endocrinol(Lausanne),2014, 5 : 110. |
| [6] | Drucker DJ, Nauck MA. The incretin system:glucagon-like peptide-1 receptor agonists and dipeptidyl peptidase-4 inhibitors in type 2 diabetes[J]. Lancet,2006, 368 (9548) : 1696-705. DOI: 10.1016/S0140-6736(06)69705-5. |
| [7] | Gault VA, Holscher C. GLP-1 agonists facilitate hippocampal LTP and reverse the impairment of LTP induced by beta-amloid[J]. Eur J Pharmacol,2008, 587 (1-3) : 112-7. DOI: 10.1016/j.ejphar.2008.03.025. |
| [8] | Holscher C. Incretin analogues that have been developed to treat type 2 diabetes hold promise as a novel treatment strategy for Alzheimer's disease[J]. Recent Pat CNS Drug Discov,2010, 5 (2) : 109-17. DOI: 10.2174/157488910791213130. |
| [9] | Eqefjord L, Gejl M, Moller A, et al. Effects of liraglutide on neurodegeneration, blood flow and cogniton in Alzheimer's disease protocol for a controlled, randomized double-blinded trial[J]. Dan Med J,2012, 59 (10) : A4519. |
| [10] | Bomfim TR, Forny-Germano L, Sathler LB, et al. An anti-diabetes agent protects the mouse brain from defective insulin signaling caused by Alzheimer's disease-associated Aβ oligomers[J]. J Clin Invest,2012, 122 (4) : 1339-53. DOI: 10.1172/JCI57256. |
| [11] | Han WN, Hölscher C, Yuan L, et al. Liraglutide protects against amyloid-β protein-induced impairment of spatial learning and memory in rats[J]. Neurobiol Aging,2013, 34 (2) : 576-88. DOI: 10.1016/j.neurobiolaging.2012.04.009. |
| [12] | Xu W, Yang Y, Yuan G, et al. Exendin-4, a glucagon-like peptide-1 receptor agonist, reduces Alzheimer disease-associated tau hyperphosphorylation in the hippocampus of rats with type 2 diabetes[J]. J Investig Med,2015, 63 (2) : 267-72. DOI: 10.1097/JIM.0000000000000129. |
| [13] | 沈亚非, 徐焱成. 高糖高脂膳食和链脲佐菌素诱导2型糖尿病模型的建立[J]. 实用诊断与治疗杂志,2006, 20 (9) : 649-50. |
| [14] | Wang X, Wang LP, Tang H, et al. Acetyl-L-carnitine rescues scopolamine-induced memory deficits by restoring insulin-like growth factor II via decreasing p53 oxidation[J]. Neurophamacology,2014, 76 (PtA) : 80-7. |
| [15] | Cheng X, Wu J, Geng M, et al. Role of synaptic activity in the regulation of amyloid beta levels in Alzheimer's disease[J]. Neurobiol Aging,2014, 35 (6) : 1217-32. DOI: 10.1016/j.neurobiolaging.2013.11.021. |
| [16] | Wang QJ, Yin J, Song YF, et al. Brain aging and AD-like pathology in streptozotocin-induced diabetic rats[J]. J Diabetes Res,2014, 2014 : 796840. |
| [17] | Yoshino Y, Ishisaka M, Tsujii S, et al. Glucagon-like peptide-1 protects the murine hippocampus against stressors via Akt and ERK1/2 signaling[J]. Biochem Biophys Res Commun,2015, 458 (2) : 274-9. DOI: 10.1016/j.bbrc.2015.01.098. |
| [18] | Du LL, Xie JZ, Cheng XS, et al. Activation of sirtuin 1 attenuates cerebral ventricular streptozotocin-induced tau hyperphosphorylation and cognitive injuries in rat hippocampi[J]. Age (Dordr),2014, 36 (2) : 613-23. DOI: 10.1007/s11357-013-9592-1. |
| [19] | Jolivalt CG, Hurford R, Lee CA, et al. Type 1 diabetes exaggerates features of Alzheimer's disease in APP transgenic mice[J]. Exp Neurol,2010, 223 (2) : 422-31. DOI: 10.1016/j.expneurol.2009.11.005. |
| [20] | Lyford GL, Yamagata K, Kaufmann WE, et al. Arc, a growth factor and activity-regulated gene, encodes a novel cytoskeletonassociated protein that is enriched in neuronal dendrites[J]. Neuron,1995, 14 (2) : 433-45. DOI: 10.1016/0896-6273(95)90299-6. |
| [21] | Wallace CS, Lyford GL, Worley PF, et al. Differential intracellular sorting of immediate early gene mRNAs depends on signals in the mRNA sequence[J]. J Neurosci,1998, 18 (1) : 26-35. |
| [22] | Steward O, Worley PF. Selective targeting of newly synthesized Arc mRNA to active synapses requires NMDA receptor activation[J]. Neuron,2001, 30 (1) : 227-40. DOI: 10.1016/S0896-6273(01)00275-6. |
| [23] | Pedrós I, Petrov D, Allgaier M, et al. Early alterations in energy metabolism in the hippocampus of APPswe/PS1dE9 mouse model of Alzheimer's disease[J]. Biochim Biophys Acta,2014, 1842 (9) : 1556-66. DOI: 10.1016/j.bbadis.2014.05.025. |
| [24] | Roshan R, Ghosh T, Gadgil M, et al. Regulation of BACE1 by miR-29a/b in a cellular model of Spinocerebellar Ataxia 17[J]. RNA Biol,2012, 9 (6) : 891-9. DOI: 10.4161/rna.19876. |
| [25] | De Strooper B, Annaert W. Proteolytic processing and cell biological functions of the amyloid precursor protein[J]. J Cell Sci,2000, 113 (Pt 11) : 1857-70. |
| [26] | Li Y, Duffy KB, Ottinger MA, et al. GLP-1 receptor stimulation reduces amyloid-beta peptide accumulation and cytotoxicity in cellular and animal models of Alzheimer's disease[J]. J Alzheimers Dis,2010, 19 (4) : 1205-19. |
 2016, Vol. 36
2016, Vol. 36
