近年来临床上针对HCV直接抗病毒药物(direct-acting antiviral agents, DAAs)的广泛应用,为丙型肝炎的治愈带来了巨大的希望,今后有可能取代聚乙二醇干扰素(PegIFN)加利巴韦林(ribavirin, RBV)P/ R原有标准方案,成为一种新的标准治疗[1]。基因1型患者使用P/R治疗,其疗效欠佳,而选择用DAA治疗使持续病毒学应答率提高到90% [2]。在我国流行的HCV基因型为1、 2、 3、 6型,其中以1b亚型为主。作为首个NS5A抑制剂药物daclatasvir和强效NS3A蛋白酶抑制剂asunaprevir联合使用24周,对P/R无法耐受和无应答的基因1b型慢性丙型肝炎患者的SVR率分别为87.4%、 80.5% [3]。目前我国还没有批准DAA类药物上市,本文就1例基因1b型慢性丙型肝炎(CHC)患者使用daclatasvir与asunaprevir联合治疗24周,并进行24周随访,以期为今后我国患者的应用提供一些帮助。
1 病例资料 1.1 一般资料李某,女性,44岁,家庭主妇。2013年10月24日因妊娠30周来我院产科门诊,检测抗-HCV阳性,HCV RNA载量1.95×108 IU/mL,ALT 33 U/L,AST 27 U/L;于2014年1月6日妊娠37周时,复测ALT 67 U/L,AST 52 U/L,HCV RNA载量2.73×106 IU/mL;无厌油、乏力、恶心、呕吐、食欲减退、腹胀、尿黄等不适,未使用药物治疗。1999年曾因产后大出血行输血治疗,丈夫身体健康,抗-HCV阴性。2014年12月自行去日本一家医院就诊,确诊为HCV基因1b型。在日本医生建议下,于2015年1月起联合daclatasvir 60 mg,qd和asunaprevir 100 mg,bid治疗,疗程24周;随后一直在我院感染科定期监测血液学、生化学、 HCV RNA及不良反应,随访至结束治疗后24周。
体格检查: T: 36.6℃;BP: 122/68 mmHg;P: 80次/分;R: 18次/分。
无贫血貌,皮肤、巩膜无黄染,无皮下出血点及瘀斑,无肝掌、蜘蛛痣,全身浅表淋巴结未触及肿大,胸廓无畸形,双肺未见异常。心界无扩大,律齐整,各瓣膜听诊区未闻及病理性杂音。腹软,未见胃肠蠕动波,无压痛及反跳痛,肝脾肋下未触及,肝肾区无叩击痛。
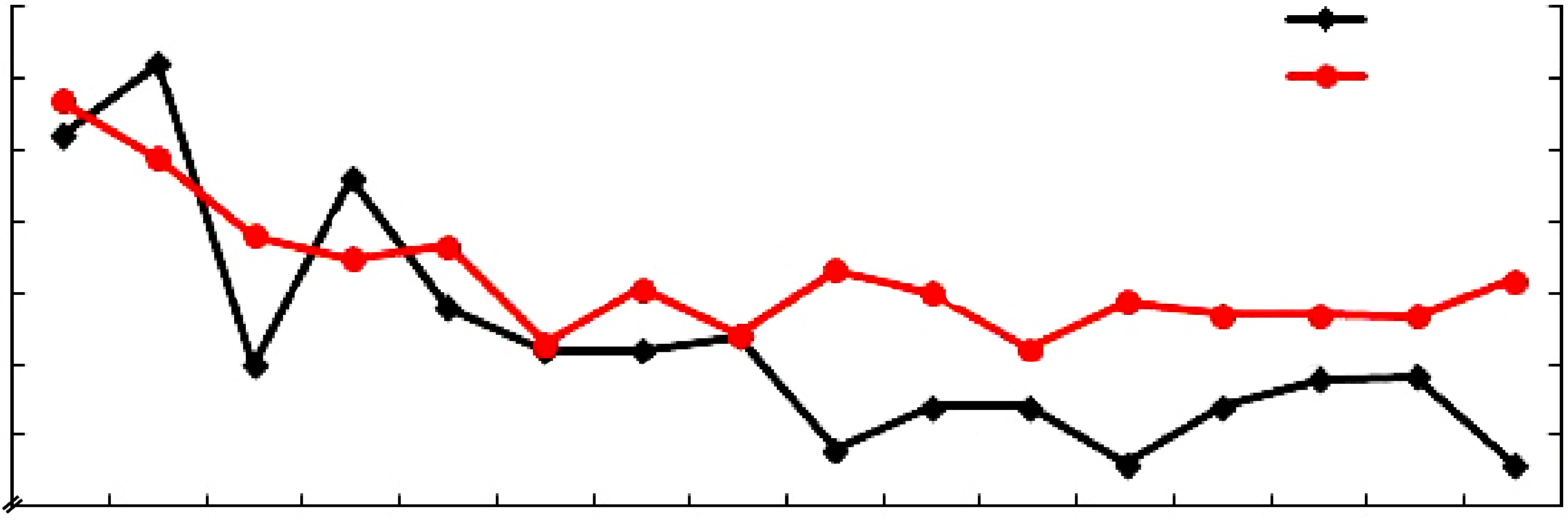
1.2 治疗与随访结果在治疗期间及随访6个月,患者无头痛、发热、腹泻、乏力、皮疹、鼻咽炎等常见不良反应,治疗及随访期间凝血功能及转氨酶正常;于治疗第3周(即15 d)时,出现总胆红素轻度升高,第5周起恢复正常,直到随访结束;于第17周时,出现血红蛋白(Hb)轻度下降,至随访结束时,波动在100~110 g/L之间,期间未进行促红细胞生成素等药物治疗。于第4周末(28 d)时检测HCV RNA转阴,于12周、 24周时复测HCV RNA均为阴性,直到随访结束6月;结束治疗后24周时,使用罗氏combas试验检测HCV RNA为阴性(< 15 IU/mL)。本例患者为临床治愈。
|
图 1 Daclatasvir和asunaprevir联合治疗期间总胆红素及血红蛋白的动态变化 Figure 1 Changes of serum total bilirubin and hemoglobin in the patient during combination treatment with daclatasvir plus asunaprevir. |
越来越多的DAAs用于CHC的临床治疗,现有的研究表明DAAs可以提高疗效,并获得持久的病毒清除能力[4]。2014年2月FAD通过的daclatasvir与asunaprevir联合方案用于治疗基因1b型CHC患者。然而,目前我国针对HCV感染的标准治疗局限于P/R方案,尚无使用daclatasvir与asunaprevir联合方案治疗基因1b型CHC患者的报道。
2012年Chayama等[5]首次报道了无IFN抗HCV方案,该研究纳入10例P/R无应答的基因1b型CHC患者,予daclatasvir+asunaprevir治疗24周,治疗结束随访至24周时的SVR率高达100%。2014年一项三期临床研究表明,这2种药物联合治疗24周对基因1b型CHC初治、既往对PegIFN联合RBV无应答或不能耐受患者的SVR分别达90%、 82%;且不同性别、年龄、民族、生理指标、 IL28B基因型的SVR没有差异,肝硬化患者和非肝硬化患者SVR相似[6]。目前daclatasvir + asunaprevir联合方案对所有基因1b型患者疗程均为24周。此2种药物联合方案展示了比PegIFN a和(或)RBV治疗时更短的疗程、更高的SVR率、更少的血液学毒性和不良事件的发生率,及更好的耐受能力[4-6]。联合治疗期间最常出现的不良反应为头痛、发热、腹泻、乏力、皮疹、鼻咽炎,为轻到中度,可有转氨酶及胆红素的升高、血红蛋白下降,常呈可逆性,治疗停止后可恢复正常;仅1%的患者因无法耐受不良反应而停药[4-6]。
本例HCV基因1b型青年女性患者使用该联合方案治疗24周,HCV RNA在第4周末转阴,随访至治疗结束后6个月,无病毒学突破和复发,为临床治愈。患者对此药耐受良好,未出现头痛、发热、腹泻、乏力、皮疹、鼻咽炎等常见的不良反应,却表现为胆红素一过性升高,同时血红蛋白轻度下降,且停药6月仍然未恢复正常水平,其原因不明,需进一步观察,并引起临床上重视。总之,基因1 b型HCV感染者通过此联合方案治疗能获得较高的病毒应答率,同时具有不良反应少、耐受力好等优点,这一方案有可能为我国基因1b型慢性丙型肝炎患者治疗开创了新的途径。
| [1] |
国家"重大新药创制"科技重大专项"重大疾病新药临床评价研究综合技术平台建设"课题组. 丙型肝炎直接抗病毒药物临床试验评价专家建议[J].
中华肝脏病杂志,2016, 24 (3) : 161-4.
( 0) 0)
|
| [2] |
WHO. Guidelines for the screening, care and treatment of persons with chronic hepatitis C infection: Updated version. Geneva: World Health Organization. 2016, Apr.
( 0) 0)
|
| [3] |
Kumada H, Suzuki Y, Ikeda K, et al. Daclatasvir plus asunaprevir for chronic HCV genotype 1b infection[J].
Hepatology,2014, 59 (6) : 2083-91.
DOI: 10.1002/hep.v59.6. ( 0) 0)
|
| [4] |
Suzuki Y, Ikeda K, Suzuki F, et al. Dual oral therapy with daclatasvir and asunaprevir for patients with HCV genotype 1b infection and limited treatment options[J].
J Hepatol,2013, 58 (4) : 655-62.
DOI: 10.1016/j.jhep.2012.09.037. ( 0) 0)
|
| [5] |
Chayama K, Takahashi S, Toyota J, et al. Dual therapy with the nonstructural protein 5A inhibitor, daclatasvir, and the nonstructural protein 3 protease inhibitor, asunaprevir, in hepatitis C virus genotype 1b-infected null responders[J].
Hepatology,2012, 55 (3) : 742-8.
DOI: 10.1002/hep.24724. ( 0) 0)
|
| [6] |
Manns M, Pol S, Jacobson IM, et al. All-oral daclatasvir plus asunaprevir for hepatitis C virus genotype 1b: a multinational, phase 3, multicohort study[J].
Lancet,2014, 384 (9954) : 1597-605.
DOI: 10.1016/S0140-6736(14)61059-X. ( 0) 0)
|
 2016, Vol. 36
2016, Vol. 36
