骨质疏松以及由此产生的脆性骨折是严重影响老年人群身体健康,甚至危及生命的疾病,因此而产生的生活失能问题给家庭和社会造成极大的压力。超过50%的骨质疏松性骨折发生在脊柱,以胸腰段多见。目前,骨质疏松性脊柱骨折以椎体成形术(PVP)为主要治疗方法,该方法具有止痛效果好,恢复快等特点,但是不能提高全身骨质量,患者新发骨折率高[1],手术费用较高。而且,部分患者存在PVP禁忌,如体内存留金属而无法进行核磁共振(MRI)确定责任椎,椎体后方骨质不完整存在骨水泥渗漏进入椎管的高风险,患者无手术意愿等。以往对该类患者的治疗措施是长期卧床,对症处理,由此产生了肺部、泌尿系的严重并发症危及生命[2],同时相当部分患者出现椎体骨坏死(Kummel病)[3-4],背痛不能缓解,长期活动困难[5-6]。特立帕肽[重组人甲状旁腺素PTH(1-34)]是我国目前可用的唯一促进骨形成的抗骨质疏松药物,它可以提高重度骨质疏松患者的全身骨量。动物实验表明它能够促进骨折愈合[7]。我们尝试使用特立帕肽保守治疗骨质疏松性脊柱骨折并分析6个月临床随访资料,发现了该方法具有促进骨折愈合和提高全身骨量的双重作用,具有替代PVP的潜力,该保守治疗方法的系统观察国内外尚无报道。
1 材料和方法 1.1 临床资料随访2013年3月~2014年6月因骨质疏松脊柱骨折而接受特立帕肽保守治疗的患者12例,均为绝经后女性,年龄73±4.8岁,11例骨折由MRI检查证实,1例通过症状、体征和CT扫描分析确认,并在随访时证实。单个椎体骨折患者5例,双椎体骨折5例,三椎体骨折2例。骨折椎体数:胸椎9个,腰椎12个。
1.2 治疗方法询问患者发生骨折的原因,是否有肿瘤病史。询问并填写生存质量量表(ODI),进行疼痛VAS评分(以床上翻身时的疼痛程度为计分标准)。检查胸腰椎X光片,腰椎第2、3、4椎体骨密度,MRI或者CT;抽血化验碱性磷酸酶(ALP)、I型胶原N端前肽(P1NP)、Ⅰ型胶原羧基末端肽(beta-CTX)和钙离子。根据sFDA批准的使用说明,排除肿瘤可能性(无相关的病史、ALP正常)和钙离子异常后,开始使用特立帕肽,20 μg,皮下注射,1次/d;同时补充钙尔奇D,0.6 g/d,分两次嚼服;早期疼痛的控制主要依赖于止痛剂,疼痛明显不能忍受即服用路盖克,但每天不超过2片。不要求患者卧床。
1.3 随访治疗的第1个月末,电话随访,主要完成疼痛VAS评分和ODI生存量表。6个月复诊时门诊完成VAS评分、ODI量表。复查胸、腰椎X线测量并比较椎体前后壁高度的比值,腰椎第2、3、4椎体骨密度;其中6例完成MRI复查。抽血检查P1NP、beta-CTX。
1.4 统计学分析使用SPSS13.0软件分析数据,计量资料用均数±标准差来表示,采用配对t检验进行组间比较。P < 0.05被认为差异有统计学意义。
2 结果 2.1 患者的一般情况所有患者均完成随访,无新发骨折。没有发现直立性低血压,血钙异常等不良事件。
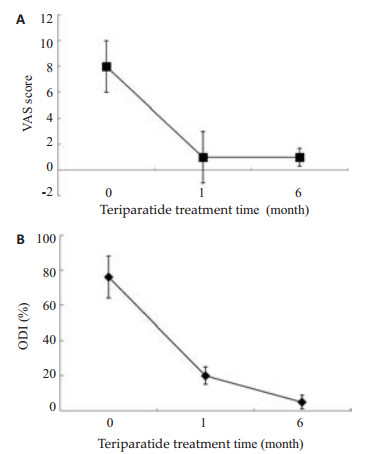
2.2 患者疼痛情况和生存质量床上翻身痛是骨质疏松性脊柱骨折患者较为典型的症状,所以我们将疼痛程度的VAS评分限定为患者床上翻身时最明显的疼痛。从图 1可以看出,骨折发生后疼痛剧烈,平均VAS评分8±2分。在使用特立帕肽治疗后1周,患者疼痛逐步减轻,止痛药的使用频率逐渐减少,至3~4周,不再需要止痛剂,此时的VAS评分为1±2分。与之对应,患者从骨折后的疼痛严重影响日常生活(76±12)%恢复到日常生活自理(20±5)%。到6个月时,患者疼痛进一步改善,生活质量进一步提高,可以参加比较活跃的社会活动[ODI评分(5±4)%]。
|
图 1 接受特立帕肽®治疗的骨质疏松脊柱骨折患者疼痛和生活质量随访 Figure 1 VAS score and quality of life of the patients with osteoporotic vertebral frature after Teriparatide® treatment. |
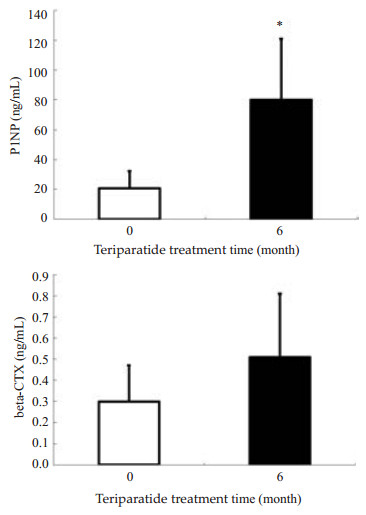
如图 2所示,使用特立帕肽后,代表骨形成的指标P1NP从20.9±11.4 ng/mL上升至80.0±41.2 ng/mL(P < 0.05),提示患者的成骨代谢增加,而显示骨吸收的beta-CTX也出现的上升趋势,本组病例中,beta-CTX的变化无显著性。
|
图 2 使用特立帕肽后患者骨代谢指标的改变 Figure 2 Levels of P1NP and bata-CTX in serum of the patients after teriparatide therapy (P < 0.05 vs before therapy). |
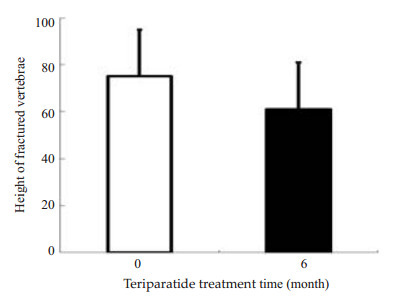
伤椎椎体在骨折发生后的进一步塌陷(或楔形变)是骨质疏松性骨折的常见影像学表现,特立帕肽保守治疗能否有效防止椎体塌陷是临床关注的问题之一。通过测量可以看出(图 3),患者伤椎后柱的高度维持良好(数据未在本文中显示),前后柱高度比值百分数从受伤时的(75±20)%下降至(61±20)%,椎体塌陷不显著。
|
图 3 患者接受特立帕肽治疗6个月后伤椎高度的变化 Figure 3 Change of the height of the fractured vertebrea after the 6-month teriparatide treatment. |
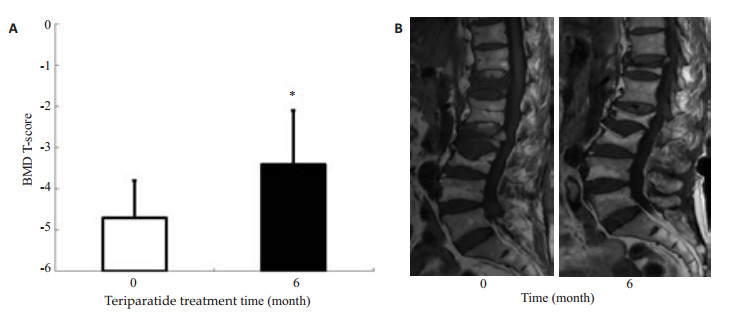
已经证明,特立帕肽可以显著提高患者骨密度,本文观察到的结果支持上述结论(图 4A),6个月的治疗可有效提高骨密度值,但骨密度仍低于-2.5。与患者临床症状(疼痛和生活质量)相一致的是,MRI复查结果显示患者骨折椎体T1像由低信号变成等信号,标志骨折愈合(图 4B,胸12、腰3、腰3椎体为骨折椎体)。
|
图 4 接受特立帕肽治疗6个月后患者骨密度(A)和骨折椎体影像学(B)的改变 Figure 4 Change of bone mass densitometry (A) and MRI images (B) of the fractured vertebrea in patients after the 6-month teriparatide therapy. *P < 0.05 vs before therapy. |
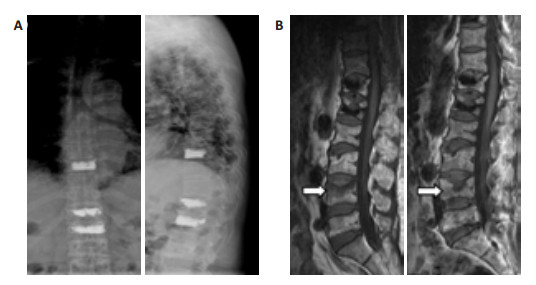
蔡女士,64岁,因腰背痛在某医院3个月内先后两次经MRI诊断为脊柱骨质疏松性骨折,分别行胸9、胸12、腰1椎体椎体成形术,术后腰背疼痛有所减轻,但仍感腰背酸痛,行走5 min即腰背痛难忍,需坐下休息。3 d前患者无明显诱因突发腰部疼痛,弯腰和床上翻身困难,体检:腰4棘突压痛和叩击痛明显。腰椎MRI显示腰4新鲜骨折(T1相低信号),椎体变形不明显(图 5A)。
|
图 5 典型病例图 Figure 5 X-ray before therapy (A) and MRI scanning (B) in a representative case of osteoporotic spinal fracture. A: X ray in thoracic and lumbar spine after PVP operation before teriparatide therapy; B: MRI images of the patient before (left) and after (right) teriparaide treatment. |
经过本文前述治疗方法。1月后腰背痛明显好转,半年时患者已经能连续行走,从事做饭等家务劳动。6个月时随访,体检:腰4棘突压痛和叩击痛消失。腰椎MRI显示腰4骨折愈合(T1等信号),椎体变形不明显(图 5B)。椎体前后壁高度无明显降低,仅在椎体中央形成schmorl结节样改变。
3 讨论本文分析12例骨质疏松性骨折(OVF)采用特立帕肽保守治疗的患者的随访资料,旨在评价该治疗方法的初步效果,期望为OVF患者的治疗寻找一种新的治疗方法,兼顾“标”(疼痛)和“本”(骨质疏松),获得理想的短期和长期效果。
骨质疏松以骨小梁变细、断裂、数量减少为主要骨质结构特征,致骨强度显著降低,抗外力能力减弱,轻微异常受力即出现脆性骨折,脊柱骨折(OVF)占骨质疏松性骨折的50%以上。在70岁以上的老年人中,每年每100人中约20人发生脊柱骨折。骨折发生之后,剧烈疼痛,活动困难严重影响老年人的生活质量。在PVP手术出现之前,主要采取以制动和止痛为主要手段的保守治疗方法。一项OVF发生后长达1年的临床观察发现,骨折发生后3周,患者的疼痛程度和生活能力同骨折时比无显著变化;骨折后3月,患者疼痛程度和生活能力好转10%~15%;1年后的情况和3月随访基本相同[5]。与临床症状相对应的是患者的影像学表现,37%的OVF伤椎内出现裂缝,13.5%的OVF伤椎内进一步变成空腔(kummel病),最终形成塌陷,脊髓受压,神经功能损害[3-4, 8]。由于疼痛症状长期不能得到缓解,部分患者长时间卧床,肺炎、心梗、深静脉血栓等疾病的发生率显著升高,OVF对症保守治疗的死亡率也升高,最近的一项临床调查发现,接受对症保守治疗的OVF患者,5年的生存率低于50%,死亡发生与OVF显著相关[9]。因此,针对OVF患者的对症保守治疗效果并不理想。
椎体成形术(PVP)或球囊成形术(PKP或BV)为OVF的治疗带来了革命性的进步。PVP技术是将穿刺针经椎弓根穿入骨折椎体,然后将高分子材料(骨水泥)由穿刺套筒注入椎体,填塞骨折空间,起到支撑作用;骨水泥凝固过程中出现短暂的高温(可达80 ℃)可以破坏痛觉神经末梢,具有优良的止痛作用,患者术后在很短的时间内恢复活动能力。BV是在PVP基础上发展而来的方法,在完成穿刺套筒的放置后,先用球囊扩张的方法恢复椎体的高度,再填充骨水泥到球囊撑开的空间内。PVP和BV均有良好的止痛作用,大大降低患者的死亡率[9]。最新文献统计了超过1百万的患者发现,PVP治疗的患者死亡率较BV高25%,保守治疗的死亡率较BV高55%[2]。但是,PVP或BV的目的是支撑病椎和止痛,仅仅处理个别的椎体,不能够解决全身骨质疏松的问题,不能有效避免其他椎体的新发骨折[10-12],甚至出现骨水泥填充椎的再骨折,增加临近节段骨折的风险[10];而且与骨质疏松相关的患者全身骨痛和关节痛等症状不能改善,因而患者的整体生活质量无法在骨折前的基础上进一步提升[1]。另外,部分患者不愿意接受手术治疗,或者体内存在金属内植物不能获得MRI的确定诊断,或者骨折椎体位于上胸椎穿刺困难;在某些病例,PVP和BV技术并不能有效止痛。尽管PVP或BV技术具有明显的治疗OVF的效果,但是该类技术需要其他辅助手段来解决骨质疏松的问题,增加了医疗费用,依然不够理想。
2002年,特立帕肽开始用于骨质疏松的治疗,增加骨量,预防新发骨折,减轻全身骨痛,其临床疗效得到大量临床资料的肯定[13]。已经证明,特立帕肽具有显著的促进骨折愈合的作用[7]。我们根据中国国家食品药品监督局(sFDA)的要求,选择绝经后严重骨质疏松的女性患者,排除相应的禁忌症后,使用特立帕肽保守治疗该类患者的骨质疏松脊柱骨折,评价患者的症状、生活质量和椎体形态,对部分患者复查MRI了解骨折愈合情况,探讨该方法的可行性。
本文的研究提示,接受特立帕肽治疗的患者1个月时疼痛明显减轻,6个月后生活质量明显提高,全身骨量提高,患者骨折椎体无显著的塌陷。骨折相关的症状体征消失,获得的MRI影像学资料证实骨折愈合。
评价OVF的治疗效果的指标包括控制疼痛的时效和椎体形态的维持(防止塌陷压迫神经),最终达到维持或提升患者生活质量的目的。与保守治疗相比,特立帕肽保守治疗具有满意的止痛效果,但其时效性较PVP或BV差,特立帕肽的止痛效果建立在促进骨折愈合的基础上,只有骨折愈合达到一定程度,疼痛才能消失。那么,患者活动不受限制,病椎愈合过程中依然受力,特立帕肽治疗是否导致椎体塌陷和裂隙形成呢?我们的随访没有发现治疗前后椎体高度的明显改变,唯一的一例椎体塌陷的患者开始治疗时已经出现的明显的椎体内空腔。维持椎体高度稳定的原因可能是:骨折压缩后短时间内椎体的抗压性已经达到一定的阈值,进一步塌陷的可能性变小。以后的塌陷与长期不愈合、骨吸收有关。特立帕肽的使用加速了骨愈合时间,使病椎在出现塌陷前愈合,维持了椎体的稳定性。最后我们也观察到特立帕肽的促骨合成作用,该作用提升全身骨量,缓解骨痛,治疗骨质疏松。实验中测得血液中的骨合成指标P1NP的明显增高与以往的研究相同,骨吸收指标beta-CTX变化不明显可能与患者骨折后一段时间内的beta-CTX水平升高有关。我们认为,特立帕肽保守治疗具有明显的效果。
如何以最小的代价做到兼顾标本的整体治疗一直是临床工作者思考的问题,我们的初步研究表明,特立帕肽保守治疗可以有效兼顾骨折的处理和骨质疏松的治疗,为OVF患者提供整体治疗手段,尤其在PVP或者BV存在禁忌的病例,该方法具有明显的优势。大样本的、严格前瞻性的、合理对照的研究尚需进一步开展。
| [1] |
Kim KW, Cho KJ, Kim SW, et al. A nation-wide, outpatient-based survey on the pain, disability, and satisfaction of patients with osteoporotic vertebral compression fractures[J].
Asian Spine J,2013, 7 (4) : 301-7.
DOI: 10.4184/asj.2013.7.4.301. ( 0) 0)
|
| [2] |
Edidin AA, Ong KL, Lau E, et al. Morbidity and mortality after vertebral fractures:comparison of vertebral augmentation and nonoperative management in the Medicare population[J].
Spine (Phila Pa 1976),2015, 40 (15) : 1228-41.
DOI: 10.1097/BRS.0000000000000992. ( 0) 0)
|
| [3] |
Hasegawa K, Homma T, Uchiyama S, et al. Vertebral pseudarthrosis in the osteoporotic spine[J].
Spine (Phila Pa 1976),1998, 23 (20) : 2201-6.
DOI: 10.1097/00007632-199810150-00011. ( 0) 0)
|
| [4] |
Mckiernan F, Faciszewski T. Intravertebral clefts in osteoporotic vertebral[J].
Arthritis Rheum,2003, 48 (5) : 1414-9.
DOI: 10.1002/(ISSN)1529-0131. ( 0) 0)
|
| [5] |
Suzuki N, Ogikubo O, Hansson T. The course of the acute vertebral body fragility fracture:its effect on pain, disability and quality of Life during 12 months[J].
Eur Spine J,2008, 17 (10) : 1380-90.
DOI: 10.1007/s00586-008-0753-3. ( 0) 0)
|
| [6] |
Bornemann R, Hanna M, Kabir K, et al. Continuing conservative care versus crossover to radiofrequency kyphoplasty:a comparative effectiveness study on the treatment of vertebral body fractures[J].
Eur Spine J,2012, 21 (5) : 930-6.
DOI: 10.1007/s00586-012-2148-8. ( 0) 0)
|
| [7] |
Campbell EJ, Campbell GM, Hanley DA. The effect of parathyroid hormone and teriparatide on fracture healing[J].
Expert Opin Biol Ther,2015, 15 (1) : 119-29.
DOI: 10.1517/14712598.2015.977249. ( 0) 0)
|
| [8] |
Tsujio T, Nakamura H, Terai H, et al. Characteristic radiographic or magnetic resonance images of fresh osteoporotic vertebral fractures predicting potential risk for nonunion:a prospective multicenter study[J].
Spine (Phila Pa 1976),2011, 36 (7) : 1229-35.
( 0) 0)
|
| [9] |
Lavelle EA, Cheney R, Lavelle WF. Mortality prediction in a vertebral compression fracture population:the ASA physical status score versus the charlson comorbidity index[J].
Internation J of Spine Surg,2015, 9 (6) : 63.
( 0) 0)
|
| [10] |
Lavelle WF, Cheney R. Recurrent fracture after vertebral kyphoplasty[J].
Spine J,2006, 6 (5) : 488-93.
DOI: 10.1016/j.spinee.2005.10.013. ( 0) 0)
|
| [11] |
Rho YJ, Choe WJ, Chun YI. Risk factors predicting the new symptomatic vertebral compression fractures after percutaneous vertebroplasty or kyphoplasty[J].
European Spine J,2012, 21 (5) : 905-11.
DOI: 10.1007/s00586-011-2099-5. ( 0) 0)
|
| [12] |
Nieuwenhuijse MJ, Putter H, Van Erkel AR, et al. New vertebral fractures after percutaneous vertebroplasty for painful osteoporotic vertebral compression fractures:a clustered analysis and the relevance of intradiskal cement leakage[J].
Radiology,2013, 266 (3) : 862-70.
DOI: 10.1148/radiol.12120751. ( 0) 0)
|
| [13] |
Keaveny TM, Donley DW, Hoffmann PF, et al. Effects of teriparatide and alendronate on vertebral strength as assessed by finite element modeling of QCT scans in women with osteoporosis[J].
J Bone Miner Res,2007, 22 (1) : 149-57.
( 0) 0)
|
 2016, Vol. 36
2016, Vol. 36
