2. 南方医科大学 药学院,广东 广州 510515
2. School of Pharmaceutical Science, Southern Medical University, Guangzhou 510515, China
腹、盆腔疾病术后粘连是临床剖腹术后常见并发症,其发生率高达90%以上[1],是腹部慢性疼痛、腹胀、女性不孕和肠梗阻等的主要原因[2]。对于这种几乎不可避免的腹膜病变,临床上较为成熟的预防手段除减少手术损伤与异物残留外,便是使用机械屏障防止损伤面相互接触。目前已有多个腹部局部使用的产品(仍缺乏口服与注射给药产品)获得美国FDA批准(Seprafilm®、Interceed®、ADEPT®),但由于存在使用人群受限、容易引起腹膜炎与皮肤瘘等缺陷,特别是在手术关腹前使用,易导致手术的成败,始终未能有效推广与使用[3]。因此,研发有效防治术后腹膜粘连的药物是目前医药科研领域一项重大课题。
目前认为,术后腹膜粘连发生主要由早期手术创伤(异物刺激)诱发炎症反应所致。机体在抵抗炎症效应及伤口自愈过程中,过表达的转化生长因子-β(TGF-β)诱导成纤维细胞过度增殖与胶原合成;同时打破腹膜纤溶系统平衡,使过度生成的胶原纤维无法被机体组织正常溶解与代谢,最终导致纤维蛋白在受损部位沉积形成粘连。纤维溶解酶作为体内纤维蛋白降解的重要参与者,其活化主要依靠纤溶酶原在纤溶酶原活化因子(PA)作用下可转化为纤维溶解酶。PA为丝氨酸蛋白酶,属于内蛋白酶家族,包括组织纤溶酶原活化因子(tPA)与尿激酶样纤溶酶原活化因子(u-PA)。纤溶酶原活化因子抑制剂(PAI)是PA的拮抗剂,对tPA与u-PA均有不同程度的抑制作用。因此,PA和PAI之间的相互作用决定了腹膜腔纤溶系统的活性,而PA和PAI-1的蛋白水平可反映纤维蛋白沉积和降解之间的平衡[4]。
丹参酮ⅡA磺酸钠(STS)是丹参有效成分丹参酮ⅡA经磺酸化成盐后而得到的水溶性物质,与丹参酮Ⅱ A相比,其具备更好的水溶性和成药性,临床主要用于治疗心绞痛、冠心病、心肌梗死等疾病。最近研究显示: STS能够抑制TGF-β诱导心房成纤维细胞向成肌纤维细胞分化,从而降低心肌重构的风险[5];我们前期研究发现,丹参能抑制大鼠粘连成纤维细胞的增殖与胶原合成[6],并且丹参酮IIA具有抗炎、改善纤维化防治大鼠术后腹膜粘连形成[4, 7]等作用。这表明两者在改善纤维化形成方面具备相似的药理作用。由此推断丹参酮IIA磺酸钠可能具备防治术后腹膜粘连的潜质。因此,本实验通过术后腹腔注射丹参酮ⅡA磺酸钠,观察其对大鼠术后腹膜粘连的防治作用,并探讨其可能的药理作用机制。
1 材料和方法 1.1 材料SD大鼠,SPF级饲养,雄性,体质量180~220 g,南方医科大学动物实验中心购置,许可证号: SCXK粤2011-0015。实验前置于实验室内适应环境1周,室温18~22 ℃,相对湿度50%~70%。自由饮水、进食。
1.2 药品与试剂丹参酮IIA磺酸钠注射液(西安鸿生生物技术有限公司,含量98.0%);tPA/PAI联合检测ELISA试剂盒(Abcam,美国);tPA活性发色底物法检测试剂盒(Athens Research and Technologies,美国);戊巴比妥钠(SIGMA,美国);生理盐水(辰欣药业股份有限公司)。
1.3 仪器SpectraMax M5多功能酶标仪(Molecular Device,美国);正置显微镜(莱卡DMI4000B)
1.4 实验方法 1.4.1 大鼠粘连模型制备与分组采用多因素法制备大鼠腹膜粘连模型[8]。75只大鼠术前12 h禁食不禁水。0.1%戊巴比妥钠30 mg/kg腹腔注射麻醉大鼠,麻醉后将大鼠仰卧固定,腹部脱毛,消毒皮肤后,取下腹部正中切口约2 cm,提出盲肠,置于无菌纱布上约5 min,使浆膜干燥,以解剖刀片轻刮整个盲肠浆膜10遍,造成轻度渗血,再滴1滴无水乙醇于创面上,大鼠双侧腹壁每隔0.5 cm结扎少量组织,每侧结扎2~3个缺血局灶。回纳盲肠,关闭腹腔。造模后,大鼠随机分为模型组(n=15)、高剂量组(n=15)、中剂量组(n=15)、低剂量组(n=15)和空白组(n=15),高、中、低剂量组分别腹腔注射剂量为20、10、5 mg/kg的STS,模型对照组与空白对照组分别给予等体积生理盐水,连续腹腔注射给药7 d。
1.4.2 粘连分级评价各组大鼠均于术后7 d采取脊椎脱臼法处死,开腹暴露腹腔,参考Nair等[9]制定的5级分类法,采用肉眼观察法对粘连程度进行分级评定(表 1)。
| 表 1 大鼠粘连分级评价指标 Table 1 Grading of adhesions in rats according to the criteria of Nair et al |
术后7 d,各组大鼠腹腔内注射0.5 mL生理盐水,0.5 h后收集腹腔液,调节pH至3.9,离心取上清液,4 ℃冰箱保存。参照试剂盒说明书计算样品tPA活性值。
1.4.4 腹膜组织中tPA/PAI-1检测取术后7 d大鼠腹壁结扎组织100 mg,制成匀浆,然后置于-20 ℃过夜。反复冻融2次处理破坏细胞膜后,离心取上清液进行检测。参照试剂盒说明操作,测定组织中tPA/PAI-1的值。
1.4.5 免疫组织化学法检测腹膜组织中TGF-β1和Collgen-Ⅰ的表达腹膜结扎组织常规石蜡包埋,切片。分别经脱蜡、水化、双蒸水洗涤、抗原修复后,室温封闭,随后孵育TGF-β1和Collgen-I一抗过夜。室温孵育二抗DAB显色,苏木素复染,盐酸酒精分化,反蓝,烘干,中性树脂封片。
正置显微镜分析每张切片阳性细胞平均光密度,以细胞质膜呈棕黄色为阳性。Image-Pro Plus 6.0软件分析,每张切片随机选取5个视野测定,测定图像平均光密度值(IOD/Area),确定阳性细胞的表达。
1.4.6 伤口愈合强度实验为评价STS是否影响术后伤口愈合,20只大鼠术前12 h禁食不禁水。0.1%戊巴比妥钠30 mg/kg腹腔注射麻醉大鼠,麻醉后将大鼠仰卧固定,腹部脱毛,消毒皮肤后,取下腹部正中切口约2 cm,提出结肠,在近盲肠2 cm处剪断,随后将两横断面缝合,回纳结肠,关闭腹腔。造模后,大鼠随机分为模型组(n=5)、STS高剂量组(n=5)、中剂量组(n=5)、低剂量组(n=5),高、中、低剂量给药浓度分别为20、10、5 mg/kg,模型对照组给予等量生理盐水,腹腔注射给药,连续7 d。7 d后处死大鼠,取出结肠,以缝合部位为中点截取4 cm左右结肠段,一端结扎,另一端接电子压力充气泵,将结肠段没入水中,以1~2 mL/s速度缓慢充入氮气,测定伤口接合处破裂时的压力数进行比较。
1.4.7 统计学方法应用SPSS 19.0对数据进行统计处理。组间粘连分级比较采用多个独立样本非参数秩和检验的Kruskal-Wallis秩和检验;其余各实验数据比较采用单个重复测量因素方差分析。计量资料统计结果用均数±标准差表示,检验标准α=0.05。
2 结果 2.1 粘连评分腹部手术后第7天,各组动物均存活。各组腹膜粘连粘连程度分级比较情况见表 2。模型组大鼠均发生3级以上粘连,STS高、中、低剂量组粘连程度较轻,甚至无粘连。多个独立样本非参数检验结果显示:大鼠各给药组与模型对照组比较,粘连程度均显著性降低(P < 0.05)。STS不同给药组间粘连程度随给药浓度增加,粘连程度降低,呈现剂量依赖关系。
| 表 2 各组腹膜粘程度连评分值 Table 2 Intra-abdominal adhesion scores of the 4 groups (n=15) |
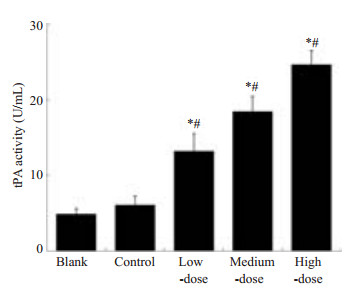
术后7 d腹腔液中tPA活性测定值见图 1。结果显示,STS高、中、低剂量组tPA活性显著高于模型组和空白组(P < 0.05)。与模型组相比,高、中、低剂量组tPA活性分别增加了309%、206%和114%。
|
图 1 术后7 d腹腔液中tPA的活性 Figure 1 tPA activity in the peritoneal tissues at 7 days after the operation. *P < 0.05 vs control; #P < 0.05 vs blank control. |
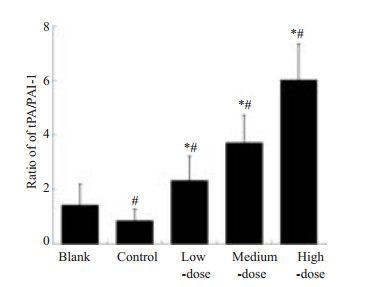
各组tPA/PAI-1蛋白水平见图 2。发生腹膜粘连的大鼠模型,其tPA与PAI-1蛋白水平失衡,而STS可逆转这一效应。与模型组相比,STS高、中、低剂量组tPA/ PAI-1水平显著提高(P < 0.05)。而模型组tPA/PAI-1的值显著低于空白组(P < 0.05)。
|
图 2 tPA/PAI-1蛋白水平 Figure 2 Ratio of tPA/PAI at 7 days after the operation. *P < 0.05 vs control; #P < 0.05 vs blank. |
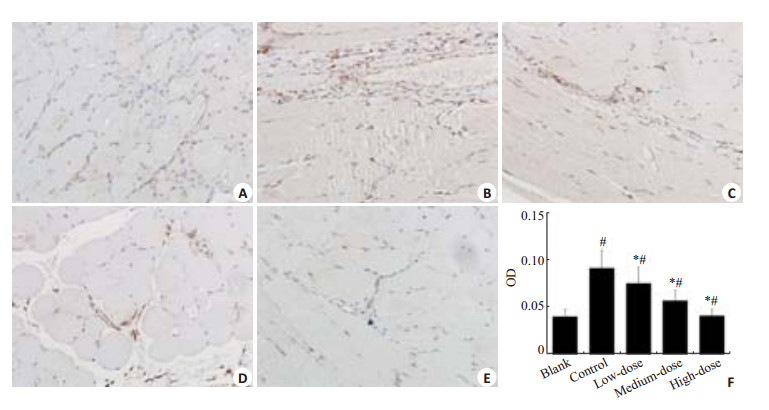
TGF-β1免疫组化半定量结果见图 3。结果显示:给药7天后,STS高、中、低剂量组腹膜组织中TGF-β1蛋白水平较模型组显著降低(P < 0.05)。STS高剂量组与空白组相比无统计学差异。STS不同给药组间随给药浓度增加,蛋白表达水平降低,呈剂量依赖关系。
|
图 3 腹膜组织中TGF-β1的表达 Figure 3 TGF-β1 expression in the peritoneal tissues at 7 days after the operation (Immunohistochemistry). A: Blank group; B: Control group; C: Low-dose group; D: Medium-dose group; E: High-dose group; F: Quantitative analysis of optic density from 5 randomly selected fields. The results are presented as Mean±SD. *P < 0.05 vs control; #P < 0.05 vs blank. |
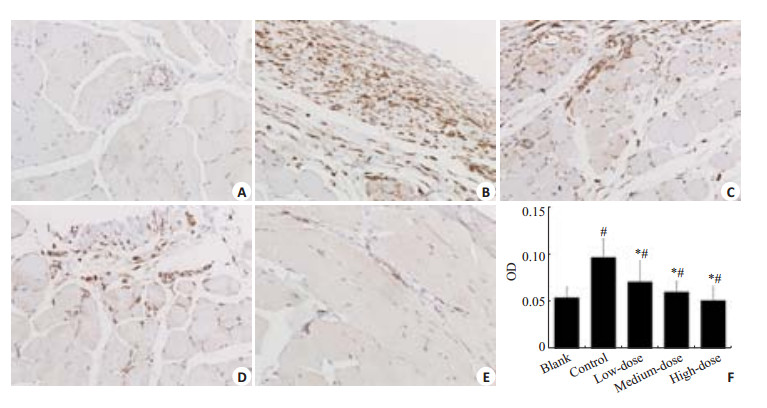
Collgen-Ⅰ免疫组化半定量结果见图 4。与模型组相比,STS高、中、低剂量组腹膜组织中TGF-β1蛋白水平显著降低(P < 0.05)。STS高剂量组Collgen-I水平与空白对照相似。
|
图 4 腹膜组织中CoI-1的表达 Figure 4 CoI-1 expression in the peritoneal tissues at 7 days after the operation (Immunohistochemistry). A: Blank group; B: Control group; C: Low-dose group; D: Medium-dose group; E: High-dose group; F: Quantitative assay of optic density from 5 randomly selected fields (Mean±SD). *P < 0.05 vs control; #P < 0.05 vs blank. |
STS高、中、低剂量伤口所承受压力值与模型组相比,并无显著性差异。该结果表明,连续腹腔给予STS防治术后腹膜粘连并不会影响伤口愈合。
3 讨论术后腹膜粘连是目前临床剖腹手术后亟待解决的一个重大难题。研究显示[10],术后粘连的主要成因是腹膜纤溶活性降低,纤维蛋白在受损部位沉积所致。腹膜在受到损伤或异物刺激早期,大量吞噬细胞迁移至创面部位,诱导成纤维细胞向损伤部位大量迁移,并释放各种生长因子与蛋白酶,其中最重要的生长因子之一TGF-β1能促进成纤维细胞的过量增殖及毛细血管长入,并大量合成胶原、纤维结合素、氨基葡聚糖等细胞外基质(ECM)取代纤维蛋白,随后分化为ECM合成能力更强的成肌纤维细胞,随着成肌纤维细胞的逐渐消失,最终形成以胶原蛋白为主的纤维性覆盖面[7]。本研究表明,模型组腹膜组织中Collgen-I和TGF-β1的表达量显著高于正常对照组与给药组(图 3)。
正常生理状态下,腹膜纤溶系统会自动激活,纤溶酶原在会被PA激活从而转化为纤维溶解酶,溶解代谢过量的ECM。然而,活化的TGF-β分子通过与膜受体结合,激活胞内TGF-β/Smads信号转导通路,导致下游PAI-1的表达量增加[11]。作为体内PA最主要的活性抑制剂,PAI-1的上调导致腹膜内tPA表达下降,降低腹膜内纤溶系统活性,最终诱发粘连带的形成[12-13]。本研究发现,当腹腔给予不同剂量的STS后,缺血局灶处TGF-β1的表达量降低(图 3),tPA/PAI-1的水平显著升高(图 2),上调了腹腔液中tPA的活性(图 1),降低缺血局灶处Collgen-I表达,起到防治术后腹膜粘连的作用。此外,有研究显示,过量表达的tPA有导致伤口愈合缓慢甚至无法愈合的现象发生[14-15]。为了考察腹腔注射STS是否会影响伤口的愈合,我们进行了伤口愈合强度实验,实验结果表明:各剂量组的STS与模型组相比,并未发生伤口愈合强度下降,这说明STS防治粘连发生是安全的。
以上结果显示: STS可防治术后腹膜粘连的发生,并且不会影响术后伤口愈合。机理可能通过降低腹膜在受到损伤或异物刺激时过量表达的TGF-β1,从而下调其对TGF-β/Smads信号转导通路激活作用,降低下游PAI-1的过表达,上调腹膜纤溶系统活性,最终实现防治术后腹膜粘连发生、发展与形成。
| [1] |
Schnüriger B, Barmparas G, Branco BC, et al. Prevention of postoperative peritoneal adhesions: a review of the literature[J].
Ame J Surg,2011, 201 (1) : 111-21.
DOI: 10.1016/j.amjsurg.2010.02.008. ( 0) 0)
|
| [2] |
Ward BC, Panitch A. Abdominal adhesions: current and novel therapies[J].
J Surg Res,2011, 165 (1) : 91-111.
DOI: 10.1016/j.jss.2009.09.015. ( 0) 0)
|
| [3] |
Ten Broek RP, Stommel MW, Strik C, et al. Benefits and harms of adhesion barriers for abdominal surgery: a systematic review and meta-analysis[J].
Lancet,2014, 383 (9911) : 48-59.
DOI: 10.1016/S0140-6736(13)61687-6. ( 0) 0)
|
| [4] |
Wang C, Li X, Meng X, et al. Prevention of experimental postoperative peritoneal adhesions through the intraperitoneal administration of tanshinone IIA[J].
Planta Med,2014, 80 (12) : 969-73.
DOI: 10.1055/s-00000058. ( 0) 0)
|
| [5] |
Yang L, Hu J, Hao HZ, et al. Sodium tanshinone IIA sulfonate attenuates the transforming growth factor-β1-induced differentiation of atrial fibroblasts into myofibroblasts in vitro[J].
Int J Mol Med,2015, 35 (4) : 1026-32.
( 0) 0)
|
| [6] |
曾煦欣, 王春霞, 王芳, 等. 丹参对大鼠粘连成纤维细胞增殖与胶原合成的作用研究[J].
中华中医药杂志,2011 (8) : 839-41.
( 0) 0)
|
| [7] |
Qin F, Ma Y, Li X, et al. Efficacy and mechanism of tanshinone IIA liquid nanoparticles in preventing experimental postoperative peritoneal adhesions in vivo and in vitro[J].
Int J Nanomedicine,2015, 10 (8) : 3699-716.
( 0) 0)
|
| [8] |
王春霞, 曾煦欣, 黄乐松, 等. 常通口服液对肠粘连大鼠病理影响[J].
中药材,2009, 32 (7) : 1105-7.
( 0) 0)
|
| [9] |
Nair SK, Bhat IK, Aurora AL. Role of proteolytic enzyme in the prevention of postoperative intraperitoneal adhesions[J].
Arch Surg,1974, 108 (6) : 849-53.
DOI: 10.1001/archsurg.1974.01350300081019. ( 0) 0)
|
| [10] |
Esposito AJ, Heydrick SJ, Cassidy MR, et al. Substance P is an early mediator of peritoneal fibrinolytic pathway genes and promotes intra-abdominal adhesion formation[J].
J Surg Res,2013, 181 (1) : 25-31.
DOI: 10.1016/j.jss.2012.05.056. ( 0) 0)
|
| [11] |
Holmdahl L, Kotseos K, Bergström M, et al. Overproduction of transforming growth factor-beta1 (TGF-beta1) is associated with adhesion formation and peritoneal fibrinolytic impairment[J].
Surgery,2001, 129 (5) : 626-32.
DOI: 10.1067/msy.2001.113039. ( 0) 0)
|
| [12] |
Shimomura M, Hinoi T, Ikeda S, et al. Preservation of peritoneal fibrinolysis owing to decreased transcription of plasminogen activator inhibitor-1 in peritoneal mesothelial cells suppresses postoperative adhesion formation in laparoscopic surgery[J].
Surgery,2013, 153 (3) : 344-56.
DOI: 10.1016/j.surg.2012.07.037. ( 0) 0)
|
| [13] |
Aarons CB, Cohen PA, Gower A, et al. Statins (HMG-CoA reductase inhibitors) decrease postoperative adhesions by increasing peritoneal fibrinolytic activity[J].
Ann Surg,2007, 245 (2) : 176-84.
DOI: 10.1097/01.sla.0000236627.07927.7c. ( 0) 0)
|
| [14] |
Brochhausen C, Schmitt VH, Planck CN, et al. Current strategies and future perspectives for intraperitoneal adhesion prevention[J].
J Gastrointest Surg,2012, 16 (6) : 1256-74.
DOI: 10.1007/s11605-011-1819-9. ( 0) 0)
|
| [15] |
Parker MC, Ellis H, Moran BJ, et al. Postoperative adhesions: ten-year follow-up of 12 584 patients undergoing lower abdominal surgery[J].
Dis Colon Rectum,2001, 44 (6) : 822-9.
DOI: 10.1007/BF02234701. ( 0) 0)
|
 2016, Vol. 36
2016, Vol. 36
