急性冠脉综合征(ACS)按发病时心电图表现分为ST段抬高性(STE-ACS)和非ST段抬高性(NSTEACS) [1],与STE-ACS相比,NSTE-ACS临床表现和检查结果具明显多样性[2-4],部分患者早期诊断存在困难。探索有效的NSTE-ACS诊断和评价方法,对减少不必要手术风险、改善心肌缺血、挽救存活心肌具有重要意义。
多巴酚丁胺负荷超声(DSE)是冠心病缺血心肌诊断和预后评价的重要工具[5],目前临床DSE结果判定多基于肉眼观察和半定量的室壁运动积分(wall motion score, WMS)。超声二维斑点追踪(2D-STE)作为量化评价心肌形变的方法,近年已应用于冠心病诊断和功能评估[6-7],但其无法追踪心肌真实的“跨平面”空间运动,多切面的图像采集过程使心脏整体形变分析无法在同一心动周期内完成,这明显影响参数的准确性和可重复性。三维斑点追踪(3D-STE)技术克服了上述局限,使我们能在单心动周期内获取心脏完整的空间运动信息[8],本研究应用3D-STE对早期NSTE-ACS危险评分中低危的患者负荷前后左室心肌形变进行评价,并探讨DSE前后3D-STE参数对NSTE-ACS的诊断价值。
1 资料与方法 1.1 研究对象和分组研究对象:根据病史、临床症状、ECG、实验室检查等初步诊断为NSTE-ACS并拟行冠脉造影(Coronary angiography,CAG)的我科住院患者,入院时对患者进行NSTE-ACS的GRACE评分[9]。主要入选标准:左室射血分数(LVEF) >50%,GRACE评分为低危和中危(GRACE分值≤140),窦性心律,既往未行冠脉再血管化治疗。主要排除标准:ACS急性期,血流动力学不稳定,陈旧心梗,严重瓣膜病,房颤,左束支传导阻滞以及存在无法进行负荷超声检查的其他因素。向患者说明试验相关内容并签署知情同意书。
研究共入选患者54例,其中初诊为UA 36例、NSTEMI 18例,完成一般资料收集。入院后3 h内行DSE检查,完成检查后2 d内行CAG,根据CAG结果将研究对象分为A组(非NSTE-ACS组)和B组(NSTE-ACS组)。
1.2 仪器西门子SC2000彩色多普勒超声诊断仪(美国),4Z1c容积探头,探头频率1~4 MHz。配备eSie LVA左心分析软件。西门子工作站配备3D-mechanics分析软件。
1.3 试验方法和主要参数采集 1.3.1 多巴酚丁胺负荷超声及图像采集启用SC2000负荷超声模式,患者左侧卧位,连接电极同步记录ECG,左室心尖四腔切面采集超声图像。显示完整左室实时三维全容积图像(real-time three-dimensional echocardiography, RT3DE)后,调整取样框深度、扇面大小和图像显示模式,以增加图像空间和时间分辨率(容积帧频>25 Hz)。
微量泵经左前臂静脉泵入多巴酚丁胺注射液,初始剂量为5 μg·kg-1·min-1,间隔3 min逐次增加负荷剂量至10 μg·kg-1·min-1和峰值20 μg·kg-1·min-1,峰值负荷3 min后终止DSE。静息状态和各负荷阶段末记录12导联ECG和血压。出现以下情况提前终止DSE:心电图提示典型心肌缺血或严重心律失常;心率>130次/min;胸痛发作;严重高血压(SBP>180 mmHg和/或DBP>100 mmHg)以及其他不可耐受症状。
静息状态下和各负荷阶段末嘱患者呼气末屏气进行图像采集,每阶段采集图像3次,每次存储3个心动周期。
1.3.2 DSE室壁运动分析启用DSE并帧比较模式,eSie LVA左心分析软件将各阶段左室三维图像切分显示为心尖四腔、三腔、二腔长轴和二尖瓣瓣环、乳头肌、心尖短轴图像,将各阶段同一切面二维图像进行并帧比较,调整取样线使心内膜边界清楚显示。
采用ASE标准[10]对左室16节段运动进行室壁运动计分(Wall Motion Score):1分,正常;2分,运动减弱;3分,无运动;4分,矛盾运动;5分,室壁瘤。取16节段计分均值计算左室室壁运动积分指数(wall motion score index,WMSI)。
各阶段LVEF应用eSie LVA软件对三维图像分析获取。
1.3.3 3D-STE分析及主要参数应用西门子工作站3D-mechanics软件读取存储的静息状态和峰值负荷时左室实时三维图像,软件自动将全容积图像切分显示为左室长轴和短轴切面(见上),调整取样线清楚显示心内膜边界,设置时间起始点为左室舒张末期(二尖瓣关闭时,MC)。
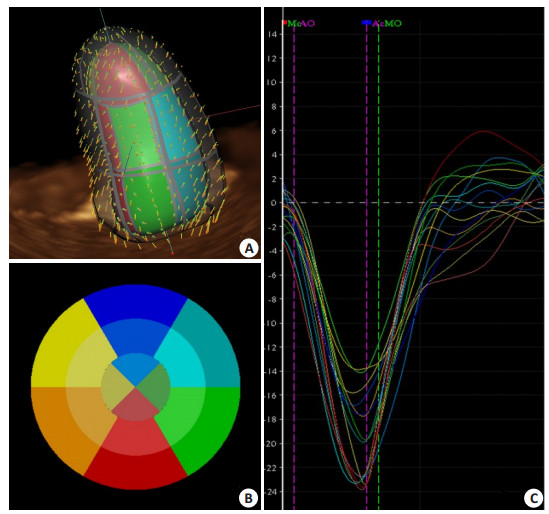
选取左室舒张末帧(MC)和收缩末帧(主动脉瓣关闭时,AC),心尖四腔切面手动标记二尖瓣瓣环室间隔、侧壁和左室心尖三点后,软件自动追踪心内膜在心动周期内运动轨迹,逐帧观察,必要时手动调整心内膜边界。软件经计算后显示左室16节段3D-STE参数曲线,并以三维速度向量模式(vector velocity imaging, VVI)显示左室壁运动(图 1)。追踪曲线明显偏移节段手动调整心内膜边界后再次分析,仍有2个以上节段追踪不理想者排除出研究。软件将左心室壁分为心内膜下、中间、心外膜下三层。由于心内膜下心肌对CAD冠脉狭窄引起的缺血最敏感,研究选用心内膜下心肌的3DSTE参数。
|
图 1 3D-STE左室16节段整体长轴应变(GLS)分析示意图 Figure 1 Analysis of left ventricular 16-segment global longitudinal strain by 3D-STE. A: 3D vector velocity imaging of the left ventricle; B: Left ventricular 16-segment model; C: Longitudinal strain curves of left ventricular 16 segments. |
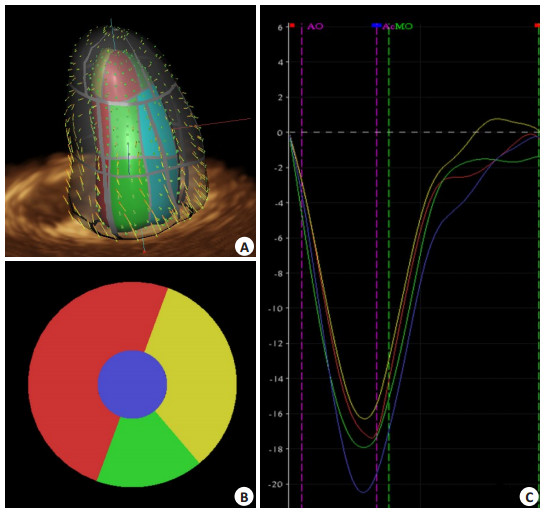
主要参数:左室整体长轴应变(global longitudinal strain, GLS)和整体环向应变(global circumferential strain, GCS)取左室16节段收缩末期峰值应变的均值(图 1),静息状态和峰值负荷时GLS和GCS分别记为GLSrest、GLSpeak、GCSrest、GCSpeak。此外,将左室16节段按冠状动脉3支主要血管灌注区域[7]分为前降支(LAD)、右冠(RCA)、左旋支(LCX)和心尖部(LV apical)4个灌注区,灌注区整体长轴应变(territory longitudinal strain, TLS)和整体环向应变(territory circumferential strain, TCS)取各灌注区收缩末期峰值应变的均值(图 2),静息状态和峰值负荷TLS和TCS分别记为TLSrest、TLS peak、TCSrest、TCSpeak。上述各参数均取3个心动周期平均值,3D-STE参数均为负值,表明收缩期心肌缩短,负值越大表明收缩期心肌整体形变越大。
|
图 2 3D-STE左室灌注区整体环向应变(TCS)分析示意图 Figure 2 Analysis of left ventricular territory circumferential strain by 3D-STE. A: 3D Vector velocity imaging of LV; B: Left ventricular perfusion territory model; C: Circumferential strain curves of left ventricular 4 perfusion territories. |
所有患者在完成DSE检查后2日内行CAG,以冠脉三支主要血管一支以上存在明显狭窄(管腔狭窄率>50%)为冠心病诊断标准。存在明显狭窄的血管根据病变情况,进行相应的血运重建治疗(球囊扩张、支架植入术等)。
1.5 重复性检验分别随机选取10名研究对象静息状态及峰值负荷时三维全容积图像,共20份图像资料,间隔3日由同一操作者及另一名操作者分别再次对图像进行左室3D-STE分析并获取GLS、GCS、TLS、TCS参数,观察者内变异性和观察者间变异性应用组内相关系数(ICC)进行评估,并绘制Bland-Altman分析图。
1.6 统计方法应用SPSS 20.0和Medcalc 14.8统计软件进行分析,计量资料以均数±标准差表示,两组间比较采用独立样本t检验,率的比较采用卡方检验。应用受试者工作曲线(ROC)评价静息和峰值负荷时3D-STE参数诊断NSTE-ACS的价值,根据Youden指数确立各参数的最适诊断标准,并计算敏感性、特异性、阳性预测值和阴性预测值,ROC曲线间的比较应用Delong法。以P < 0.05为差异有统计学意义。
2 结果 2.1 基本资料所有患者均完成DSE检查,无胸痛及其他不良事件发生。54例患者中,5例因声窗欠佳、3D-STE追踪不理想等原因排除,最终入组患者49例。在一般资料比较中,两组患者LVEF%、GRACE评分等无明显差异(表 1)。
| 表 1 一般资料的比较 Table 1 Demographic data and clinical characteristics of the two groups |
49例患者中17例无明显冠脉狭窄(A组);32例存在明显的冠脉狭窄(B组),其中单支病变9例,双支病变16例,三支或左主干病变7例。
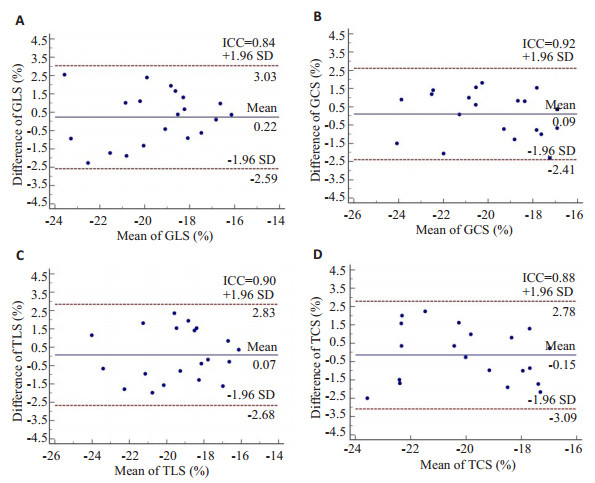
2.3 重复性检验在重复性检验中,3D-STE参数GLS、GCS、TLS、TCS观察者内和观察者间均有满意的重复性,ICC分别为0.86、0.87、0.80、0.83(观察者内)和0.84、0.92、0.90、0.88 (观察者间)。观察者间一致性的Bland-Altman分析见(图 3)。
|
图 3 3D-STE参数观察者间重复性检验Bland-Altman图及组内相关系数(ICC) Figure 3 Bland-Altman plots of interobserver variability of 3D-STE measurements and intraclass correlation coefficient (ICC). A: Global longitudinal strain (GLS); B: Global circumferential strain (GCS); C: Territory longitudinal strain (TLS); D: Territory circumferential strain (TCS). |
两组患者静息状态下LVEF无明显差异,DSE时LVEF均出现上升,峰值负荷时B组LVEF明显低于A组(P < 0.01,表 2)。静息和峰值负荷LVEF诊断NSTEACS的ROC分析:ROC曲线下面积(AUC)分别为0.61和0.72 (P < 0.05)。
| 表 2 静息和峰值负荷时超声参数 Table 2 EEchocardiographic parameters at rest and at peak-dose stage |
静息状态存在室壁运动异常(WMA)者24例,异常运动节段共67个,其中运动减弱55个,无运动或矛盾运动12个。在DSE中,67个节段中WMS降低22个,WMS双向反应(biphasic response,低剂量负荷降低高剂量负荷增加) 29个,增加或无变化16个。新出现WMA 24个节段。
B组静息和峰值负荷时WMSI均大于A组,静息和峰值负荷WMSI诊断NSTE-ACS的AUC分别为0.75和0.72,两者无显著差异(P > 0.05,表 2)。
2.5 DSE 3D-STE分析结果左室16节段整体应变:静息状态下两组GLS无明显差异,B组GCS值大于A组(P < 0.01);DSE时,A组GLS、GCS数值减小,B组GLS、GCS数值增大,但变化均未达统计学意义(P > 0.05);峰值负荷时A组GLS、GCS值均明显小于B组(P < 0.01,表 2)。
左室灌注区整体应变:静息状态下B组TLS、TCS值均明显大于A组(P < 0.05);DSE时,B组TLS值出现明显增大(P < 0.05),A组TLS、TCS数值降低,B组TCS数值增加,但变化均未达统计学意义(P > 0.05);A组峰值负荷时TLS、TCS值均明显小于B组(P < 0.01,表 2)。
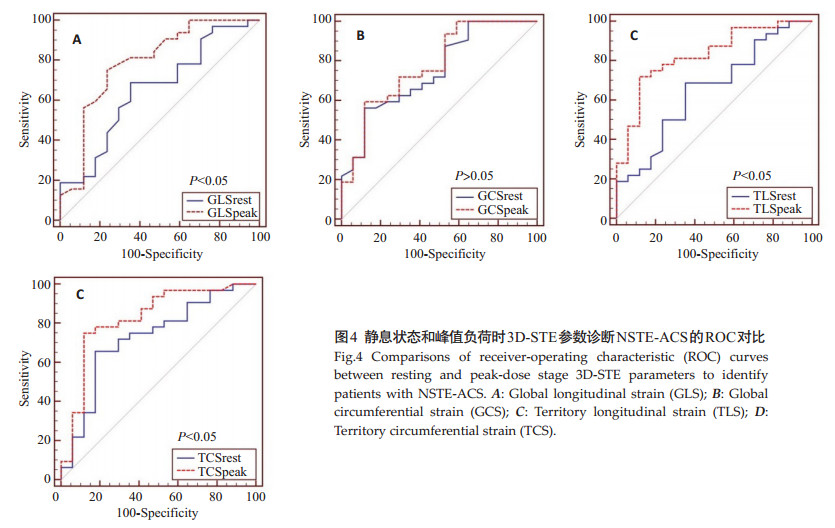
静息和峰值负荷时GLS、GCS、TLS、TCS诊断NSTE-ACS的ROC分析中,AUC分别为0.67和0.80 (P < 0.05),0.75和0.79 (P > 0.05),0.66和0.83 (P < 0.01),0.72和0.82 (P < 0.05)(表 3,图 4)。3D-STE参数的ROC曲线比较中,TLSpeak、TCSpeak诊断NSTE-ACS的价值最高(AUC 0.83和0.82,与其他参数相比P < 0.05)。各参数诊断NSTE-ACS的最适标准及其敏感性、特异性、PPV、NPV (表 3)。
| 表 3 3D-STE参数诊断NSTE-ACS的ROC分析结果 Table 3 Receiver-operating characteristic curve analyses of 3D-STE parameters at rest and at peak-dose stage to identify patients with NSTE-ACS |
|
图 4 静息状态和峰值负荷时3D-STE参数诊断NSTE-ACS的ROC对比 Figure 4 Comparisons of receiver-operating characteristic (ROC) curves between resting and peak-dose stage 3D-STE parameters to identify patients with NSTE-ACS. A: Global longitudinal strain (GLS); B: Global circumferential strain (GCS); C: Territory longitudinal strain (TLS); D: Territory circumferential strain (TCS). |
流行病学资料表明,目前临床ACS患者中近70%为不稳定心绞痛(UA)和非ST抬高性心梗(NSTEMI) [1],且呈继续上升趋势,UA和NSTEMI患者中远期的心血管事件发生率和死亡率明显高于STE-ACS。由于UA和NSTEMI的冠脉病理、临床表现、治疗策略等相近,最新指南[2]中以NSTE-ACS替代了以往使用的UA/NSTEMI。多项研究表明,对NSTE-ACS患者进行早期明确诊断,并对病变血管选择合适的血运重建策略,可显著改善患者临床预后[11]。
NSTE-ACS早期治疗策略的选择建立在患者明确诊断和心血管事件危险评估基础上。由于NSTE-ACS临床表现和冠脉病理具多样化特点,ECG、心肌损伤标志物等检查存在诊断敏感性和特异性欠佳的问题[12],部分患者早期确诊较为困难。一部分非NSTE-ACS患者进行了诊断性的CAG检查,这增加了患者经济负担和发生手术并发症的风险。
GRACE评分是临床权威和广泛应用的NSTEACS早期危险分层方法,是患者早期治疗策略选择的重要依据[2]。本研究中NSTE-ACS组和非NSTE-ACS组间GRACE评分并无明显差异,在CAG检查结果中,部分NSTE-ACS患者多支冠脉存在严重病变,DSE结果也提示NSTE-ACS组存在明显缺血存活心肌(见后),这表明部分NSTE-ACS患者心血管事件风险难以通过早期危险评分系统做出有效判别。因此,对于NSTE-ACS患者,尤其是危险评分为中低危者,需要探索更有效便捷的诊断和临床风险评价方法。
3.2 二维负荷超声结果和意义超声心动图因其无创、便捷、经济等特点使NSTEACS患者能在入院早期进行整体和局部心功能评估。其中,负荷超声以其技术特点在冠心病早期临床诊断、危险分层和预后评价方面具有重要的临床意义[13]。常规负荷超声及结果评价以二维超声的WMSI为基础,本研究应用RT3DE获取标准二维切面并对DSE各阶段图像进行并帧比较[14],大大缩短了图像采集和分析时间,提高了评价结果准确性。
静息状态下两组间LVEF无明显差异,DSE中LVEF均出现上升,但B组变化明显低于A组,这表明NSTE-ACS患者存在左室收缩储备功能的明显下降。通过DSE也提高了LVEF诊断NSTE-ACS的价值(峰值负荷的AUC明显上升)。B组WMSIrest明显高于A组,虽然在DSE中出现了新的WMA节段,但B组WMSIpeak及AUC并未出现明显变化,在DSE中,我们观察到部分静息WMA节段出现了收缩运动的明显改善(持续或双向反应),这提示在B组NSTE-ACS患者的WMA节段中有相当数量的存活心肌(顿抑心肌和冬眠心肌) [5, 15]。存活心肌是重要的危险分层判别标准[2],对这部分患者应该采取更加积极的早期干预策略。
3.3 3D-STE负荷超声结果和意义3D-STE的应用,使我们能真正对心肌三维空间的形变运动进行评估,也大大缩短了图像获取时间。应变是评价心肌主动形变功能的STE参数,定义为心动周期内心肌变化长度与初始长度的比值(%),其不受邻近心肌被动牵拉影响,这使NSTE-ACS患者(尤其存在WMA时)整体和节段心肌功能的评价更为准确。按心肌的走形和舒缩运动方向,左室心肌应变可分为长轴应变(LS),环向应变(CS)和径向应变(RS),既往研究表明LS、CS指标具有满意的可重复性[16]。RS由于需同时追踪内外两层心肌组织的运动轨迹,受左室壁厚度、心外膜边界不易追踪等影响,可行性和重复性较差[17]。综合以上因素,本研究选取LS和CS为心脏功能评价指标。研究的重复性检验中,LS、CS参数均有理想的可重复性(ICC均大于0.8)(图 3)。
左室整体应变(Global strain, GS)作为左室整体形变功能的指标建立在左室16节段划分基础上。左室灌注区应变(Territory strain, TS)按冠脉三支血管相对固定的供血区域对左室16节段应变做了进一步细分,Grenne的CAD相关研究表明[6],2D-STE的TS参数能对CAD闭塞血管做出早期诊断,但目前很少有基于3D-STE TS的CAD研究报道。本研究同时选择GS和TS参数,意从不同的观察角度评估NSTE-ACS心脏功能变化。
静息状态下,NSTE-ACS组GCS、TCS值明显高于非NSTE-ACS组,提示我们NSTE-ACS组左室心内膜下心肌环向形变功能的降低更为明显,诊断价值的ROC曲线比较中,各参数的AUC并无明显差异。两组间LS和CS的差别在负荷试验时进一步加大,DSE峰值负荷时,3D-STE参数的诊断价值较静息状态下明显增加,上述变化以TLS和TCS最为显著。综合比较本研究中LVEF,WMSI和3D-STE参数的NSTE-ACS诊断价值,结果显示TLSpeak和TCSpeak是最理想的诊断指标。
研究结果中,峰值负荷3D-STE指标的NSTE-ACS诊断价值明显优于WMSI,其诊断特异性很高(近90%),但敏感性尚不足(75%左右),分析有以下原因:(1) CAD心肌缺血后功能改变可能有多种表现形式,除了收缩形变能力(应变)的降低,既往研究还发现缺血心肌存在收缩延迟、收缩后收缩等失同步现象;(2)研究样本量较小,准确反映群体的参数分布需要大量样本;(3)结合我们以往研究经验[14],并从NSTE-ACS患者负荷试验的安全性考虑,研究选择小剂量的多巴酚丁胺。研究结果证明了其安全性和有效性,在此基础上,增加负荷剂量能否进一步提高3D-STE的诊断价值?这些方面是有待进一步研究。
| [1] | Yeh RW, Sidney S, Chandra M, et al. Population trends in the incidence and outcomes of acute myocardial infarction[J]. N Engl J Med,2010, 362 (23) : 2155-65. DOI: 10.1056/NEJMoa0908610. |
| [2] | Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes: executive summary: a report of the american college of cardiology/american heart association task force on practice guidelines[J]. Circulation,2014, 130 (25) : 2354-94. DOI: 10.1161/CIR.0000000000000133. |
| [3] | 高润霖. 我国急性冠状动脉综合征治疗的现状及存在问题[J]. 中华医学杂志,2009, 89 (36) : 2521-2. |
| [4] | Terkelsen CJ, Lassen JF, Norgaard BL, et al. Mortality rates in patients with ST-elevation vs. non-ST-elevation acute myocardial infarction: observations from an unselected cohort[J]. Eur Heart J,2005, 26 (1) : 18-26. |
| [5] | Pellikka PA, Nagueh SF, Elhendy AA, et al. American society of echocardiography recommendations for performance, interpretaion, and application of stress echocardiography[J]. J Am Soc Echocardiogr,2007, 20 (9) : 1021-41. DOI: 10.1016/j.echo.2007.07.003. |
| [6] | Grenne B, Eek C, Sjøli B, et al. Acute coronary occlusion in nonST-elevation acute coronary syndrome: outcome and early identification by strain echocardiography[J]. Heart,2010, 96 (19) : 1550-6. DOI: 10.1136/hrt.2009.188391. |
| [7] | Sarvari SI, Haugaa KH, Zahid W, et al. Layer-specific quantification of myocardial deformation by strain echocardiography May reveal significant CAD in patients with non-ST-segment elevation acute coronary syndrome[J]. JACC Cardiovasc Imaging,2013, 6 (5) : 535-44. DOI: 10.1016/j.jcmg.2013.01.009. |
| [8] | Xu TY, Sun JP, Lee AP, et al. Three-dimensional speckle strain echocardiography is more accurate and efficient than 2D strain in the evaluation of left ventricular function[J]. Int J Cardiol,2014, 176 (2) : 360-6. DOI: 10.1016/j.ijcard.2014.07.015. |
| [9] | Granger CB, Goldberg RJ, Dabbous O, et al. Predictors of hospital mortality in the global registry of acute coronary events[J]. Arch Intern Med,2003, 163 (19) : 2345-53. DOI: 10.1001/archinte.163.19.2345. |
| [10] | Lang RM, Bierig M, Devereux RB, et al. Recommendations for chamber quantification: a report from the American society of echocardiography's guidelines and standards committee and the chamber quantification writing group, developed in conjunction with the European association of echocardiography, a branch of the European society of cardiology[J]. J Am Soc Echocardiography,2005, 18 (12) : 1440-63. DOI: 10.1016/j.echo.2005.10.005. |
| [11] | Puymirat E, Taldir G, Aissaoui N, et al. Use of invasive strategy in non-ST-segment elevation myocardial infarction is a major determinant of improved long-term survival: FAST-MI (French Registry of Acute Coronary Syndrome)[J]. JACC Cardiovasc Interv,2012, 5 (9) : 893-902. DOI: 10.1016/j.jcin.2012.05.008. |
| [12] | Sanchis J, Bodí V, Núñez J, et al. Limitations of clinical history for evaluation of patients with acute chest pain, non-diagnostic electrocardiogram, and normal troponin[J]. Am J Cardiol,2008, 101 (5) : 613-7. DOI: 10.1016/j.amjcard.2007.10.024. |
| [13] | Shah BN, Balaji G, Alhajiri A, et al. Incremental diagnostic and prognostic value of contemporary stress echocardiography in a chest pain unit: mortality and morbidity outcomes from a realworld setting[J]. Circ Cardiovasc Imaging,2013, 6 (2) : 202-9. DOI: 10.1161/CIRCIMAGING.112.980797. |
| [14] | 徐勇, 刘峻松, 智光, 等. 实时三维多巴酚丁胺超声心动图负荷试验评估冠心病的临床观察[J]. 中华医学杂志,2012, 92 (39) : 2747-51. |
| [15] | Nihoyannopoulos P, Vanoverschelde JL. Myocardial ischaemia and viability: the pivotal role of echocardiography[J]. Eur Heart J,2011, 32 (7) : 810-9. DOI: 10.1093/eurheartj/ehr002. |
| [16] | Yamada A, Luis SA, Sathianathan D, et al. Reproducibility of regional and global longitudinal strains derived from twodimensional speckle-tracking and doppler tissue imaging between expert and novice readers during quantitative dobutamine stress echocardiography[J]. J Am Soc Echocardiogr,2014, 27 (8) : 880-7. DOI: 10.1016/j.echo.2014.04.016. |
| [17] | Serri K, Reant P, Lafitte M, et al. Global and regional myocardial function quantification by two-dimensional strain -Application in hypertrophic cardiomyopathy[J]. J Am Coll Cardiol,2006, 47 (6) : 1175-81. DOI: 10.1016/j.jacc.2005.10.061. |
 2015, Vol. 35
2015, Vol. 35
